
Белок состоит только из альфа-спиралей и не содержит бета-листы.
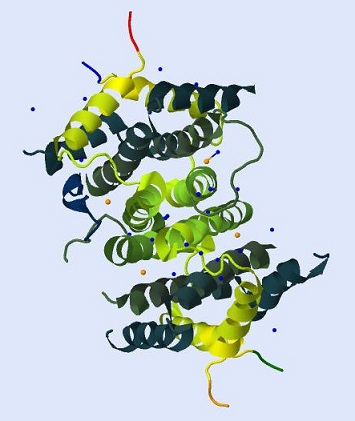
Общий вид белка показан на рисунке 1.
Рис.1 Цепи белка изменяют цвет с ярко-желтого на темно-синий по направлению от N-концов к С-концам. Кроме того, начало цепи A выделено красным цветом, B – оранжевым, C – зеленым и D – синим. Молекулы воды покрашены в синий цвет, ионы натрия в оранжевый.
Рассмотрим одну из альфа-спиралей цепи А в структуре YPJD_BACSU. Ее расположение в белке показано на рисунке 2. Эта альфа-спираль состоит из 14 аминокислотных остатков (с 5 по 18, как можно видеть по рисунку 3).
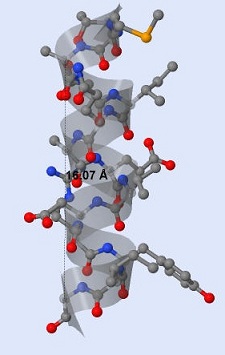
В спирали приблизительно 3.75 витков. Найдено расстояние между двумя атомами, лежащими по одну сторону спирали через 3 витка друг от друга (в данном случае это атомы с номерами 47 и 137). Чтобы найти шаг спирали, нужно разделить 16.07 на 3. Длина одного витка равна примерно 5.36 ангстрем. Стандартное значение шага спирали приблизительно равно 5.4 ангстрем. Вычисления строятся по рисунку 4.
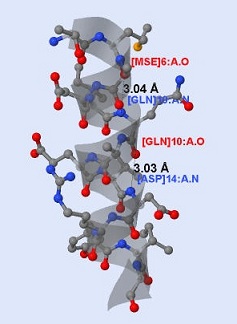
Всего аминокислотных остатка на виток спирали: 14 разделить на 3.75 = 3.73 . Аминокислотные остатки, если они находятся в середине спирали, образуют водородные связи между каждыми четвертыми остатками, например, 6 образует связь с 10, 10 - с 14, как можно увидеть на рисунке 5.
| Рис.2 Рассматриваемая альфа-спираль выделена красным цветом. | 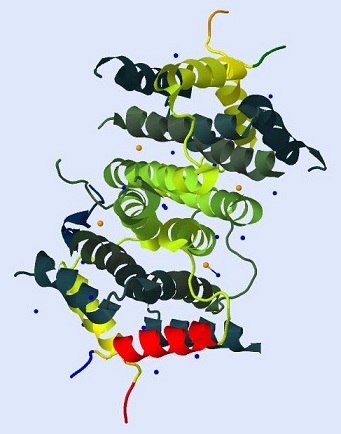
|
| Рис.3 Альфа-спираль цепи А белка YPJD. Стрелкой показано направление от N- к C-концу, кроме того спираль меняет свой цвет от желтого к темно-оранжевому в данном направлении. Подписаны номера первого и последнего аминокислотных остатков альфа-спирали. |

|
| Рис.4 Все атомы имеют свои стандартные цвета для программы Jmol. Атомы углерода - серые, азота - голубые, кислорода красные, фосфора - оранжевые и т.д. Для удобства подсчета видны полупрозрачные витки спирали в стиле cartoons. |
|
| Рис.5 Водородные связи показаны черными пунктирными линиями, рядом подписаны их длины, а также названия аминокислотных остатков, цепи, к которой они принадлежат, и атомов, между которыми, образуются водородные связи. |
|
В белке есть как альфа-спирали, так и бета-листы. Рассмотрим один такой бета-лист цепи А. В этом листе есть и параллельные и антипараллельные бета-тяжи, параллельные бета-тяжи образуют вогнутую/выпуклую поверхность.
| Рис.6 С возрастанием номера атома цвет листа меняется от темно-синего к красному через обратную радугу. В одной части листа стрелки, указывающие направление от N-конца к С-концу, смотрят в одну сторону (параллельные бета-тяжи), в другой же – в разные (антипараллельныe). |

|
В белке 4 остатка цистеина (окрашены в красный цвет), в каждой цепи по одному(у всех номера 76), они расположены далеко друг от друга, поэтому дисульфидных мостиков не образуется. Можно проверить командой select ssbonds(Jmol), таким образом, было доказано, что в белке нет солевых мостиков.
Солевые мостики образуются между боковыми цепями отрицательно заряженных аминокисот(Glu, Asp) и положительно заряженными аминокислотами (Arg, Lys и His).
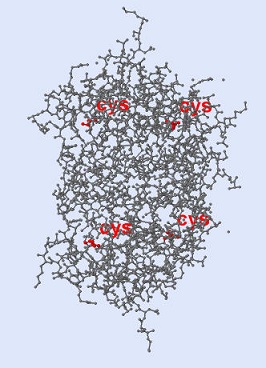
| Рис.7 Аминокислотные остатки цистеина окрашены в красный цвет, а также атомы главной цепи подписаны рядом названием аминокислоты. |
|
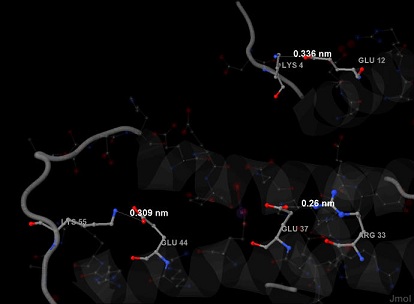
| Рис.8 Аминокислоты Glu, Asp, Arg, Lys и His видны на рисунке, но они были выделены полупрозрачно, так как между ними не образуются солевые мостики. Также показаны более крупно некоторые атомы кислорода у отрицательно заряженнных аминокислоты и атомы азота у положительно заряженных аминокислот, которые образуют связи, то есть расстояние между ними меньше, чем 3.5 ангстрем. На рисунке видно 3 солевых мостика, длины которых 3.36, 3.09 и 2.6 ангстрем. |
|
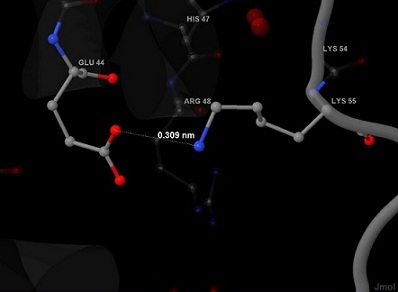
| Рис.9 Более детально показан солевой мостик между остатками №44 Glu и №91 Lys. Связь образуется между атомом кислорода (красный) у Glu и атомыом азота (синий) у Arg. Длина связи 3.09 ансгстрем. |
|