Введение
В базе PDB под кодом 3NTU хранится структура белка RadA из археи Methanococcus voltae PS. Этот белок участвует в репарации ДНК и гомологичной рекомбинации — процессе, при котором повреждённый участок ДНК восстанавливается по образцу похожей (гомологичной) последовательности.
RadA связывается с одноцепочечной ДНК и собирается в нуклеопротеиновый филамент (НФ). Внутри этой структуры происходит поиск гомологичных участков и обмен цепями между молекулами ДНК. При этом белок гидролизует АТФ, и его активность напрямую зависит от присутствия одноцепочечной ДНК.
Структурные характеристики
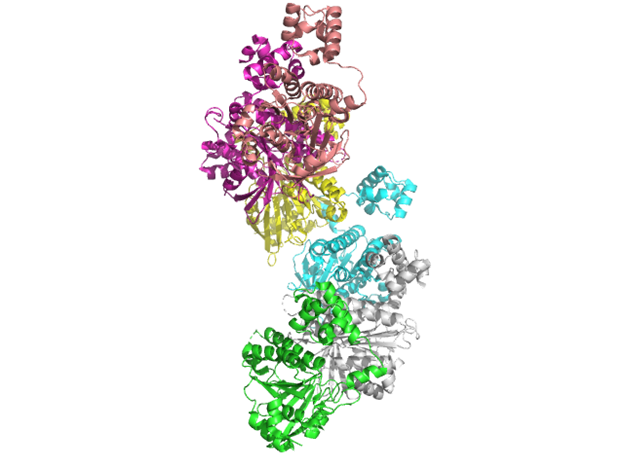
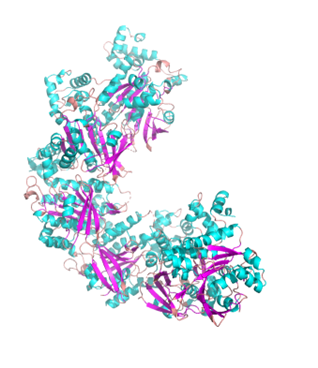
Асимметрическая единица данного белка представлена единственной полипептидной цепью А: заметны альфа-спирали, которые чередуются с бета-складчатыми листами. В состав биологической единицы (функциональной формы белка) входят 6 идентичных полипептидных цепей А, то есть в клетке археи данный белок — гомомерный гексамер, причем его единицы в пространстве располагаются по спирали.
Сравнение с UniProt
Полипептидную цепь можно найти в базе данных UniProt под идентификатором O73948. Сравнив последовательность на PDB с UniProt можно обнаружить 2 мутации: заменена 1-ая аминокислота (аспарагин на глицин) и 299-ая (аспартат на лизин).
В структуре PDB 3NTU модифицированные аминокислотные остатки отсутствуют.
Малые молекулы в структуре
В записи присутствуют три типа малых молекул:
- ANP (негидролизуемый аналог АТФ) — одна молекула находится на цепи А и занимает нуклеотид-связывающий центр.
- Ионы магния (MG) — два иона расположены на цепях C и D. Они координируются с фосфатными группами ANP и выступают в роли кофакторов.
- Ион натрия (NA) — один ион находится на цепи Е и, предположительно, попал в структуру из кристаллизационного буфера.
- Молекулы воды — располагаются как на поверхности белковых цепей, так и вблизи активного центра. Они играют важную роль в стабилизации третичной структуры белка и гидратации сайта связывания нуклеотида.
В структуре PDB 3NTU малые молекулы выполняют разные роли:
- ANP (негидролизуемый аналог АТФ) был добавлен искусственно вместо физиологической АТФ, чтобы зафиксировать белок в активном состоянии без протекания катализа.
- Ионы магния являются естественным кофактором RadA и необходимы для связывания нуклеотида; они присутствуют в клетке, но в кристалл были добавлены дополнительно для стабильности.
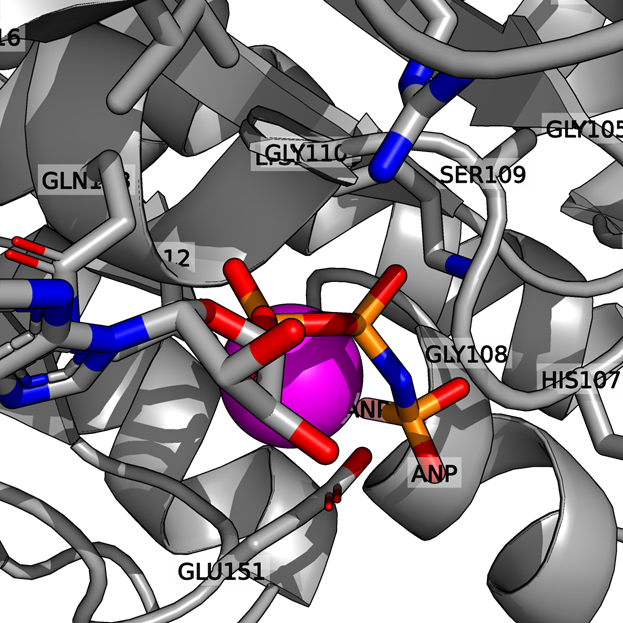
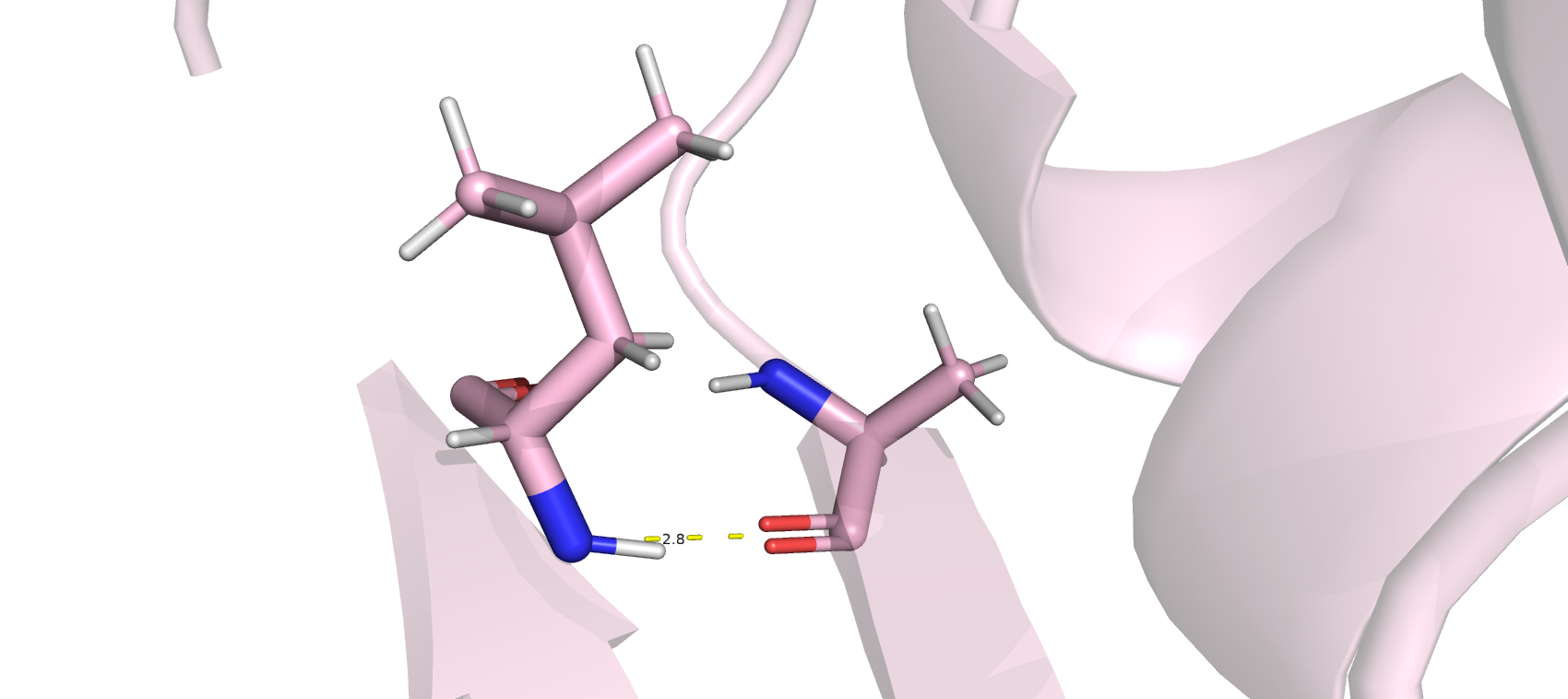
Взаимодействия в структуре белка
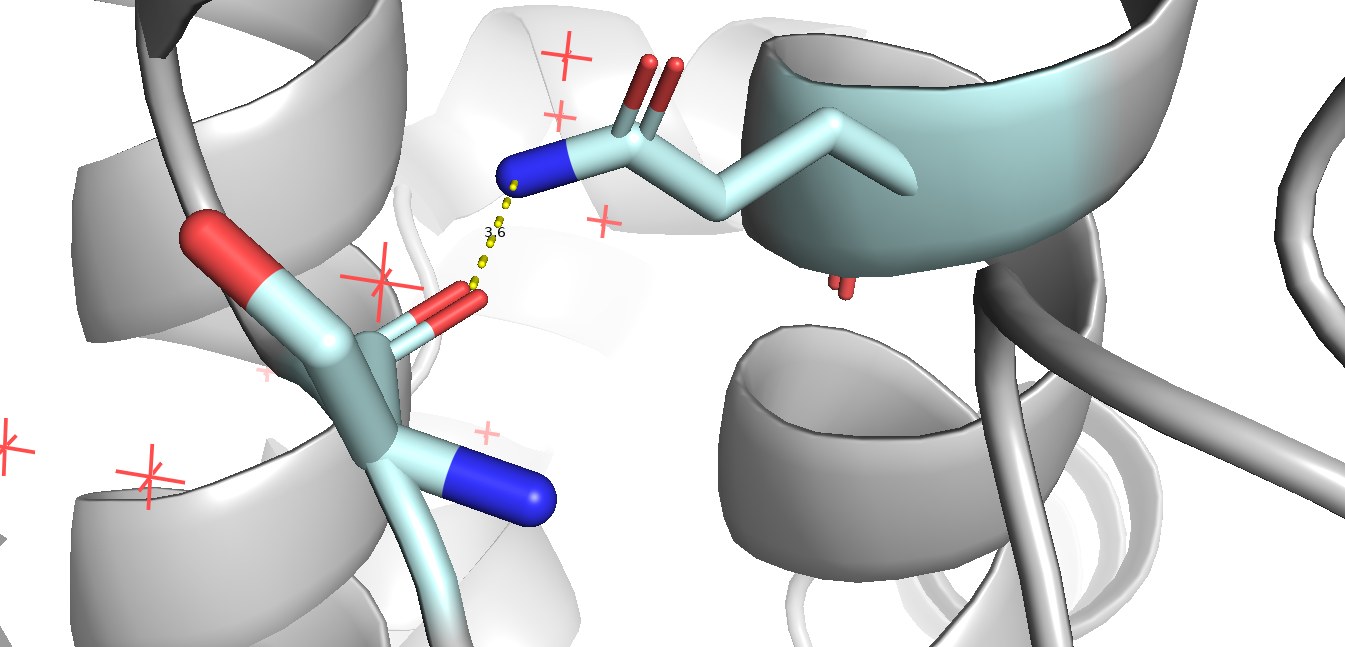
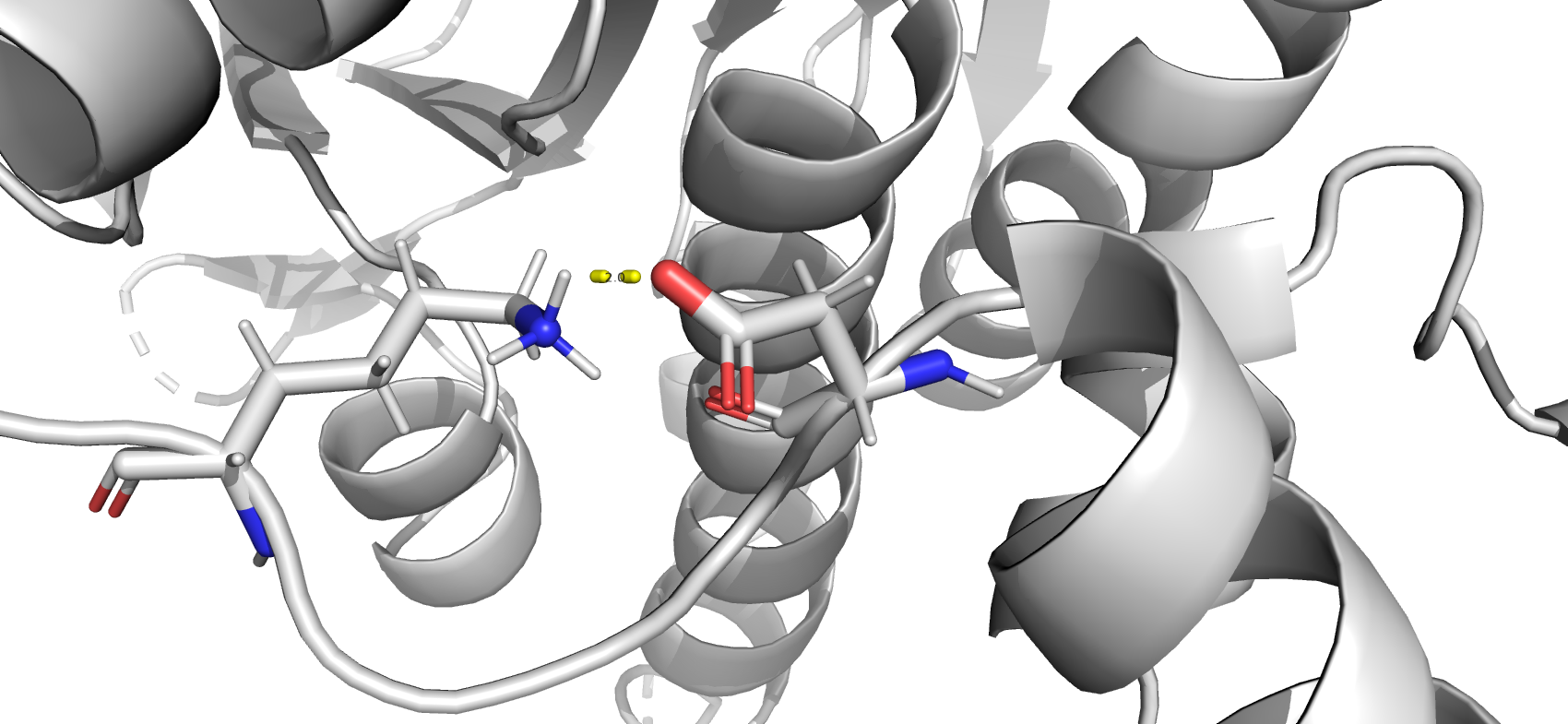
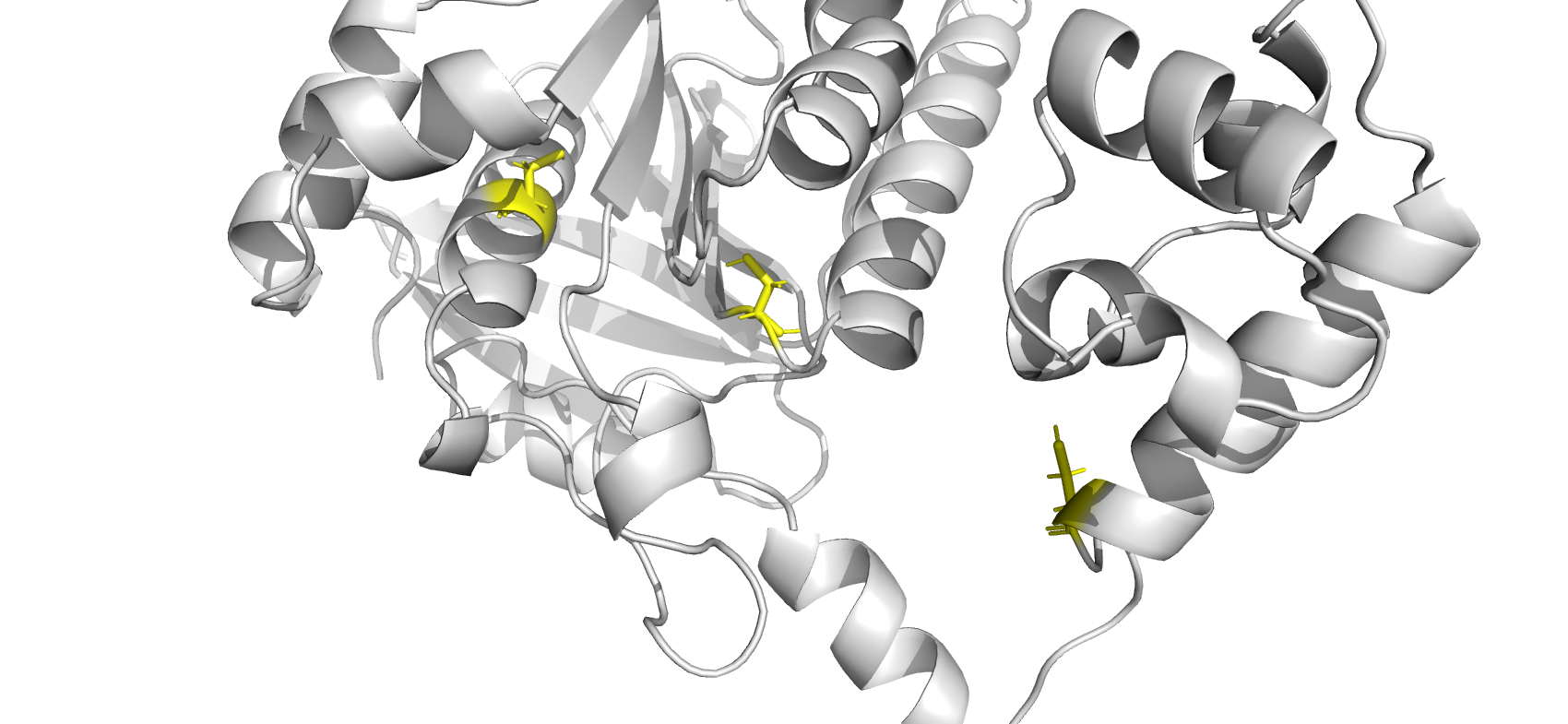
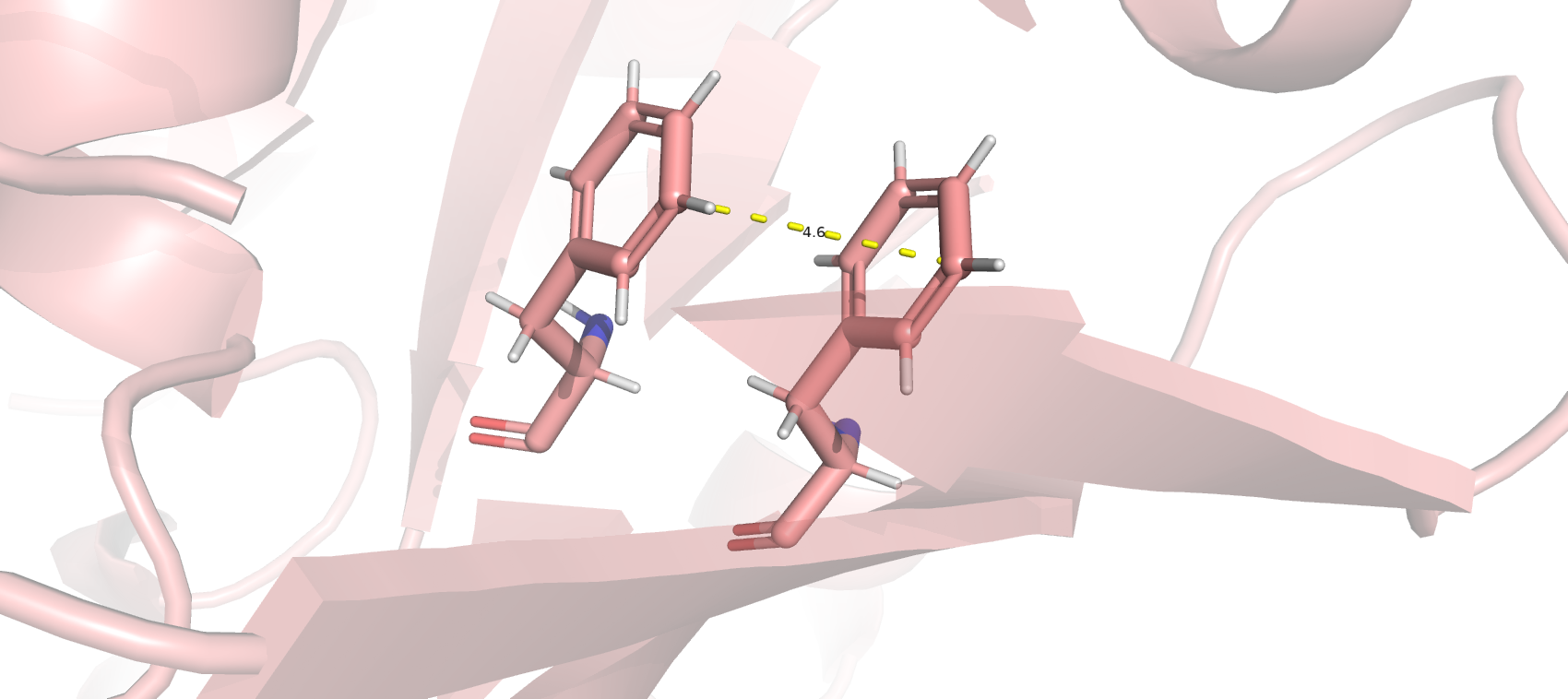
Ссылки на базы данных и файлы
Литература
- [1] PDB ID: 3NTU. Wu, Y., He, Y., Moya, I.A., Qian, X., Luo, Y. (2009). Crystal structure of RadA from Methanococcus voltae PS.
- [2] UniProt ID: O73948. RadA protein - Methanococcus voltae.
- [3] Chen, Z., Yang, H., & Pavletich, N.P. (2008). Mechanism of homologous recombination from the RecA-ssDNA/dsDNA structures. Nature, 453(7194), 489-494.