- Получение файлов со структурами
PDB-структура комплекса 1dh3 взята из банка PDB.
В банке Macromolecular Structure Database EBI содержится
описание биологической единицы. получены файлы 1dh3.pdb и 1dh3.mmol.
Описанные в них структуры идентичны (для других комплексов pdb-структура может быть частью
биологической единицы, остальные части симметричны).
- Исследование контактов между молекулами белка и нуклеиновой кислоты
Использованные множества:
- polar – полярные атомы белка
- hydrophobic – гидрофобные атомы белка
- polar_dna – полярные атомы ДНК
- hydrophobic_dna – неполярные атомы ДНК
- base – все атомы оснований ДНК
- mjg – атомы оснований ДНК, обращённые в большую бороздку ("major groove")
- mig – атомы оснований ДНК, обращённые в малую бороздку ("minor groove").
- tocompl – атомы оснований ДНК, образующие водородные связи с
комплиментарным основанием.
 |
 |
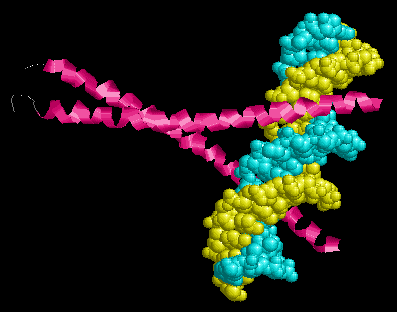
| Две белковые спирали лежат в большой бороздке ДНК |
Спирали белка контактируют друг с другом за счет гидрофобных взаимодействий.
Зеленым окрашены остатки лейцина, обеспечивающие связь двух субъединиц |
Рассмотрим контакт белка и ДНК.
| |
Полярные |
Гидрофобные |
Всего |
| Контакты белка с ... |
|
|
|
| ... остатками 2'-дезоксирибозы |
2 (по 1 в каждой цепи, идентичны) |
0 |
2 |
| ... остатками фосфорной кислоты |
6 атомов (5 остатков) в одной цепи и 8 (5) в другой
(связь с двумя атомами кислорода одного остатка читалась за одну) |
--- |
14 |
| ... остатками азотистых оснований со стороны большой бороздки |
2 атома (1 остаток) в одной цепи и 2 (2) в другой |
4 (по 2 в каждой цепи, идентичны) |
8 |
| ... остатками азотистых оснований со стороны малой бороздки |
0 |
0 |
0 |
Таким образом, больше всего в данной структуре полярных контактов. Гидрофильные остатки
белка взаимодействуют с остовом (большая часть этих взаимодействий – с остатками фосфорной
кислоты), а также с атомами оснований в большой бороздке. Скрипт face.txt
показывает, что молекулы белка лежат в большой бороздке ДНК. С малой бороздкой белок не
контактирует.
Контакты двух белковых цепей с ДНК в целом одинаковы, но есть незначительные различия (в
основном в контактах с остатками фосфорной кислоты). Но различия в взаимодействиях с
основаниями значимы.
- Поиск специфических контактов, обеспечивающих узнавание сайта в молекуле ДНК.
Специфические контакты будим искать среди восьми контактов белка с атомами основанй со стороны
большой бороздки.
Рассмотрим взаимодействие цепи C белка и ДНК. Аспарагин образует две водородные связи
с тимином и цитозином. Комплиментарное основание к тимину в основной цепи аденин.
Таким образом, связывается последовательность TCA. Важны также гидрофобные
взаимодействия.
Различия в контактах цепей белка заключаются в том, что аспарагин 293 повернут в разных цепях
по-разному. В цепи A он не может образовывать связь с вторым основанием ДНК.
Нос скорее всего этот поворот не играет роли, и реально положение аспарагина идентично.
Тогда получаем жесткую структуру из четырех атомов, образующих водородные связи друг с другом.
Также ее поддерживают гидрофобные взаимодействия близлежащих атомов.
В чепи A есть еще полярное взаимодействие аргинина с гуанином.
Таким образом, предполагаемый сайт узнавания:
5*-- TnnnnTCn --3*
3*-- nCTGnnnT --5*
в идеале для одной цепи:
5*-- TGACnTCA --3*
С ДНК взаимодействуют остатки белка:
аланин 296 и 297, аспарагин 293 и аргинин 301 в цепи A
аланин 296 и 297 и аспарагин 293 в цепи C.
- Описание функций исследованного белка
В банке UniProt найдено описание белка CREB1_MOUSE
из комплекса 1dh3. Это активирующий фактор транскрипции, связанный с цАМФ-чувствительным
элементом (CRE).
Связавание ДНК регулируется ионами магния.
За связывание с ДНК отвечает домен bZIP_1 (PF00170).
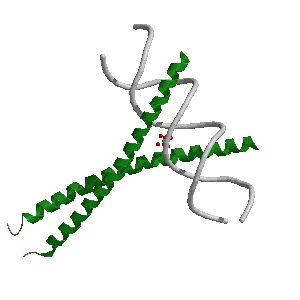
Особенность этого домена $#150; наличие двух спиралей, связанных между собой "лейциновыми
застежками". Это гидрофобные взаимодействия, плотно удерживающие две субъединицы белка.
Далее рассмотрим белки, содержащие домен bZIP_1.
Из БД Pfam получено выравнивание ближайших белков (seed). К нему добавлен
фрагмент (остатки 281-341) исследуемого белка.
|
|
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* |
|
|
|
|
|
|
|
|
2 |
0 |
|
|
|
|
|
|
|
|
|
* |
|
|
|
|
|
|
|
|
4 |
0 |
|
|
|
|
|
|
|
|
|
* |
|
|
|
|
|
|
|
|
6 |
0 |
|
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| C |
R |
E |
B |
1 |
_ |
M |
O |
U |
S |
|
: |
|
- |
- |
A |
R |
K |
R |
E |
V |
R |
L |
M |
K |
N |
R |
E |
A |
A |
R |
E |
C |
R |
R |
K |
K |
K |
E |
Y |
V |
K |
C |
L |
E |
N |
R |
V |
A |
V |
L |
E |
N |
Q |
N |
K |
T |
L |
I |
E |
E |
L |
K |
A |
L |
K |
D |
L |
Y |
C |
- |
- |
- |
- |
H |
K |
S |
D |
|
: |
|
5 |
9 |
| Y |
E |
N |
5 |
_ |
Y |
E |
A |
S |
T |
|
: |
|
A |
K |
A |
W |
K |
R |
A |
R |
L |
L |
E |
R |
N |
R |
I |
A |
A |
S |
K |
C |
R |
Q |
R |
K |
K |
M |
S |
Q |
L |
Q |
L |
Q |
R |
E |
F |
D |
Q |
I |
S |
K |
E |
N |
T |
M |
M |
K |
K |
K |
I |
E |
N |
Y |
E |
K |
L |
V |
Q |
K |
M |
K |
K |
I |
S |
R |
L |
|
: |
|
6 |
5 |
| A |
T |
F |
4 |
_ |
H |
U |
M |
A |
N |
|
: |
|
E |
K |
L |
D |
K |
K |
L |
K |
K |
M |
E |
Q |
N |
K |
T |
A |
A |
T |
R |
Y |
R |
Q |
K |
K |
R |
A |
E |
Q |
E |
A |
L |
T |
G |
E |
C |
K |
E |
L |
E |
K |
K |
N |
E |
A |
L |
K |
E |
R |
A |
D |
S |
L |
A |
K |
E |
I |
Q |
Y |
L |
K |
D |
L |
I |
E |
E |
|
: |
|
6 |
5 |
| T |
A |
F |
1 |
_ |
T |
O |
B |
A |
C |
|
: |
|
E |
R |
E |
L |
K |
R |
E |
K |
R |
K |
Q |
S |
N |
R |
E |
S |
A |
R |
R |
S |
R |
L |
R |
K |
Q |
A |
E |
A |
E |
E |
L |
A |
I |
R |
V |
Q |
S |
L |
T |
A |
E |
N |
M |
T |
L |
K |
S |
E |
I |
N |
K |
L |
M |
E |
N |
S |
E |
K |
L |
K |
L |
E |
N |
A |
A |
|
: |
|
6 |
5 |
| C |
P |
R |
F |
1 |
_ |
P |
E |
T |
C |
|
: |
|
D |
R |
D |
L |
K |
R |
E |
R |
R |
K |
Q |
S |
N |
R |
E |
S |
A |
R |
R |
S |
R |
L |
R |
K |
Q |
A |
E |
A |
E |
E |
L |
A |
I |
K |
V |
D |
S |
L |
T |
A |
E |
N |
M |
A |
L |
K |
A |
E |
I |
N |
R |
L |
T |
L |
T |
A |
E |
K |
L |
T |
N |
D |
N |
S |
R |
|
: |
|
6 |
5 |
| G |
B |
F |
3 |
_ |
A |
R |
A |
T |
H |
|
: |
|
E |
R |
E |
L |
K |
R |
E |
R |
R |
K |
Q |
S |
N |
R |
E |
S |
A |
R |
R |
S |
R |
L |
R |
K |
Q |
A |
E |
T |
E |
E |
L |
A |
R |
K |
V |
E |
A |
L |
T |
A |
E |
N |
M |
A |
L |
R |
S |
E |
L |
N |
Q |
L |
N |
E |
K |
S |
D |
K |
L |
R |
G |
A |
N |
A |
T |
|
: |
|
6 |
5 |
| G |
B |
F |
2 |
_ |
A |
R |
A |
T |
H |
|
: |
|
E |
K |
E |
V |
K |
R |
E |
K |
R |
K |
Q |
S |
N |
R |
E |
S |
A |
R |
R |
S |
R |
L |
R |
K |
Q |
A |
E |
T |
E |
Q |
L |
S |
V |
K |
V |
D |
A |
L |
V |
A |
E |
N |
M |
S |
L |
R |
S |
K |
L |
G |
Q |
L |
N |
N |
E |
S |
E |
K |
L |
R |
L |
E |
N |
E |
A |
|
: |
|
6 |
5 |
| E |
M |
B |
P |
1 |
_ |
W |
H |
E |
A |
|
: |
|
E |
R |
E |
L |
K |
R |
E |
R |
R |
K |
Q |
S |
N |
R |
E |
S |
A |
R |
R |
S |
R |
L |
R |
K |
Q |
Q |
E |
C |
E |
E |
L |
A |
Q |
K |
V |
S |
E |
L |
T |
A |
A |
N |
G |
T |
L |
R |
S |
E |
L |
D |
Q |
L |
K |
K |
D |
C |
K |
T |
M |
E |
T |
E |
N |
K |
K |
|
: |
|
6 |
5 |
| H |
B |
P |
1 |
A |
_ |
W |
H |
E |
A |
|
: |
|
E |
R |
E |
L |
K |
K |
Q |
K |
R |
K |
L |
S |
N |
R |
E |
S |
A |
R |
R |
S |
R |
L |
R |
K |
Q |
A |
E |
C |
E |
E |
L |
G |
Q |
R |
A |
E |
A |
L |
K |
S |
E |
N |
S |
S |
L |
R |
I |
E |
L |
D |
R |
I |
K |
K |
E |
Y |
E |
E |
L |
L |
S |
K |
N |
T |
S |
|
: |
|
6 |
5 |
| G |
B |
F |
1 |
_ |
A |
R |
A |
T |
H |
|
: |
|
E |
R |
E |
L |
K |
R |
Q |
K |
R |
K |
Q |
S |
N |
R |
E |
S |
A |
R |
R |
S |
R |
L |
R |
K |
Q |
A |
E |
C |
E |
Q |
L |
Q |
Q |
R |
V |
E |
S |
L |
S |
N |
E |
N |
Q |
S |
L |
R |
D |
E |
L |
Q |
R |
L |
S |
S |
E |
C |
D |
K |
L |
K |
S |
E |
N |
N |
S |
|
: |
|
6 |
5 |
| C |
P |
R |
F |
3 |
_ |
P |
E |
T |
C |
|
: |
|
E |
R |
E |
L |
K |
R |
Q |
R |
R |
K |
Q |
S |
N |
R |
E |
S |
A |
R |
R |
S |
R |
L |
R |
K |
Q |
A |
K |
S |
D |
E |
L |
Q |
E |
R |
L |
D |
N |
L |
S |
K |
E |
N |
R |
I |
L |
R |
K |
N |
L |
Q |
R |
I |
S |
E |
A |
C |
A |
E |
V |
T |
S |
E |
N |
H |
S |
|
: |
|
6 |
5 |
| G |
B |
F |
4 |
_ |
A |
R |
A |
T |
H |
|
: |
|
K |
A |
A |
A |
Q |
R |
Q |
K |
R |
M |
I |
K |
N |
R |
E |
S |
A |
A |
R |
S |
R |
E |
R |
K |
Q |
A |
Y |
Q |
V |
E |
L |
E |
T |
L |
A |
A |
K |
L |
E |
E |
E |
N |
E |
Q |
L |
L |
K |
E |
I |
E |
E |
S |
T |
K |
E |
R |
Y |
K |
K |
L |
M |
E |
V |
L |
I |
|
: |
|
6 |
5 |
| C |
R |
E |
B |
2 |
_ |
B |
O |
V |
I |
|
: |
|
E |
A |
A |
R |
K |
R |
E |
V |
R |
L |
M |
K |
N |
R |
E |
A |
A |
R |
E |
C |
R |
R |
K |
K |
K |
E |
Y |
V |
K |
C |
L |
E |
N |
R |
V |
A |
V |
L |
E |
N |
Q |
N |
K |
T |
L |
I |
E |
E |
L |
K |
A |
L |
K |
D |
L |
Y |
C |
- |
- |
- |
- |
H |
K |
S |
D |
|
: |
|
6 |
1 |
| A |
T |
F |
1 |
_ |
H |
U |
M |
A |
N |
|
: |
|
D |
P |
Q |
L |
K |
R |
E |
I |
R |
L |
M |
K |
N |
R |
E |
A |
A |
R |
E |
C |
R |
R |
K |
K |
K |
E |
Y |
V |
K |
C |
L |
E |
N |
R |
V |
A |
V |
L |
E |
N |
Q |
N |
K |
T |
L |
I |
E |
E |
L |
K |
T |
L |
K |
D |
L |
Y |
S |
- |
- |
- |
- |
N |
K |
S |
V |
|
: |
|
6 |
1 |
| C |
R |
E |
M |
_ |
H |
U |
M |
A |
N |
|
: |
|
E |
A |
T |
R |
K |
R |
E |
L |
R |
L |
M |
K |
N |
R |
E |
A |
A |
K |
E |
C |
R |
R |
R |
K |
K |
E |
Y |
V |
K |
C |
L |
E |
S |
R |
V |
A |
V |
L |
E |
V |
Q |
N |
K |
K |
L |
I |
E |
E |
L |
E |
T |
L |
K |
D |
I |
C |
S |
- |
- |
- |
- |
P |
K |
T |
D |
|
: |
|
6 |
1 |
| C |
R |
E |
B |
A |
_ |
D |
R |
O |
M |
|
: |
|
E |
K |
S |
L |
K |
K |
I |
R |
R |
K |
I |
K |
N |
K |
I |
S |
A |
Q |
E |
S |
R |
R |
K |
K |
K |
E |
Y |
M |
D |
Q |
L |
E |
R |
R |
V |
E |
I |
L |
V |
T |
E |
N |
H |
D |
Y |
K |
K |
R |
L |
E |
G |
L |
E |
E |
T |
N |
A |
N |
L |
L |
S |
Q |
L |
H |
K |
|
: |
|
6 |
5 |
| J |
U |
N |
B |
_ |
H |
U |
M |
A |
N |
|
: |
|
Q |
E |
R |
I |
K |
V |
E |
R |
K |
R |
L |
R |
N |
R |
L |
A |
A |
T |
K |
C |
R |
K |
R |
K |
L |
E |
R |
I |
A |
R |
L |
E |
D |
K |
V |
K |
T |
L |
K |
A |
E |
N |
A |
G |
L |
S |
S |
T |
A |
G |
L |
L |
R |
E |
Q |
V |
A |
Q |
L |
K |
Q |
K |
V |
M |
T |
|
: |
|
6 |
5 |
| J |
U |
N |
_ |
C |
H |
I |
C |
K |
/ |
|
: |
|
Q |
E |
R |
I |
K |
A |
E |
R |
K |
R |
M |
R |
N |
R |
I |
A |
A |
S |
K |
C |
R |
K |
R |
K |
L |
E |
R |
I |
A |
R |
L |
E |
E |
K |
V |
K |
T |
L |
K |
A |
Q |
N |
S |
E |
L |
A |
S |
T |
A |
N |
M |
L |
R |
E |
Q |
V |
A |
Q |
L |
K |
Q |
K |
V |
M |
N |
|
: |
|
6 |
5 |
| J |
R |
A |
_ |
D |
R |
O |
M |
E |
/ |
|
: |
|
Q |
E |
K |
I |
K |
L |
E |
R |
K |
R |
Q |
R |
N |
R |
V |
A |
A |
S |
K |
C |
R |
K |
R |
K |
L |
E |
R |
I |
S |
K |
L |
E |
D |
R |
V |
K |
V |
L |
K |
G |
E |
N |
V |
D |
L |
A |
S |
I |
V |
K |
N |
L |
K |
D |
H |
V |
A |
Q |
L |
K |
Q |
Q |
V |
M |
E |
|
: |
|
6 |
5 |
| G |
C |
N |
4 |
_ |
Y |
E |
A |
S |
T |
|
: |
|
E |
S |
S |
D |
P |
A |
A |
L |
K |
R |
A |
R |
N |
T |
E |
A |
A |
R |
R |
S |
R |
A |
R |
K |
L |
Q |
R |
M |
K |
Q |
L |
E |
D |
K |
V |
E |
E |
L |
L |
S |
K |
N |
- |
- |
- |
- |
- |
- |
- |
Y |
H |
L |
E |
N |
E |
V |
A |
R |
L |
K |
K |
L |
V |
G |
E |
|
: |
|
5 |
8 |
| C |
P |
C |
1 |
_ |
N |
E |
U |
C |
R |
|
: |
|
D |
P |
S |
D |
V |
V |
A |
M |
K |
R |
A |
R |
N |
T |
L |
A |
A |
R |
K |
S |
R |
E |
R |
K |
A |
Q |
R |
L |
E |
E |
L |
E |
A |
K |
I |
E |
E |
L |
I |
A |
E |
R |
- |
- |
- |
- |
- |
- |
- |
D |
R |
W |
K |
N |
L |
A |
L |
A |
H |
G |
A |
S |
T |
E |
- |
|
: |
|
5 |
7 |
| B |
Z |
L |
F |
1 |
_ |
E |
B |
V |
/ |
|
: |
|
E |
C |
D |
S |
E |
L |
E |
I |
K |
R |
Y |
K |
N |
R |
V |
A |
S |
R |
K |
C |
R |
A |
K |
F |
K |
Q |
L |
L |
Q |
H |
Y |
R |
E |
V |
A |
A |
A |
K |
S |
S |
E |
N |
D |
R |
L |
R |
- |
- |
- |
L |
L |
L |
K |
Q |
M |
C |
P |
S |
L |
D |
V |
D |
S |
I |
I |
|
: |
|
6 |
2 |
| Y |
A |
P |
4 |
_ |
Y |
E |
A |
S |
T |
|
: |
|
G |
K |
P |
L |
R |
N |
T |
K |
R |
A |
A |
Q |
N |
R |
S |
A |
Q |
K |
A |
F |
R |
Q |
R |
R |
E |
K |
Y |
I |
K |
N |
L |
E |
E |
K |
S |
K |
L |
F |
D |
G |
L |
M |
K |
- |
- |
- |
- |
E |
N |
S |
E |
L |
K |
K |
M |
I |
E |
S |
L |
K |
S |
K |
L |
K |
E |
|
: |
|
6 |
1 |
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Как видно из данного выравнивания, аспарагин (293 в CREB1_MOUSE)
косервативен. Это подтверждает, что найденный контакт важен для связывания с ДНК.
Красным окрашены остатки аланина, гидрофобно взаимодействующие с неполярными атомами ДНК.
Они тоже достаточно консервативны (во всех белках присутствует хотя бы один аланин на
этих позициях).
Аргинин 301 также консервативен.
- Построение схемы контактов белка с ДНК
С помощью программы nucplot, предназначенной для визуализации
контактов между ДНК и белком, построена схема контактов
белка и ДНК в структуре 1dh3.
Полученная схема отличается от того, что было найдено ранее. Но основной контакт –
c аспарагином 293 – содержится в схеме (под названием "nonbonded contact"). Также
присутствует контакт аргинина 293 с ДНК. Но гидрофобные контакты программа nucplot
не обнаружила. Также найдено много новых контактов. Возможно, программа ищет контакты с
более мягкими условиями.
