| Толщина гидрофобной части мембраны | 11.57 A |
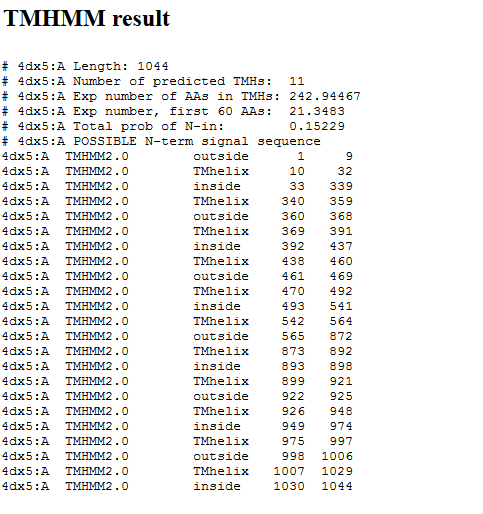
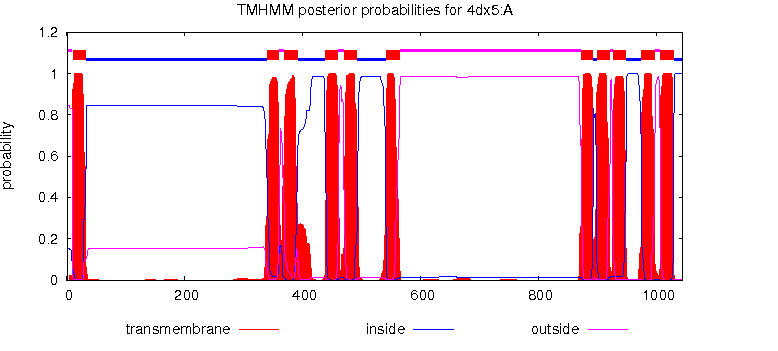
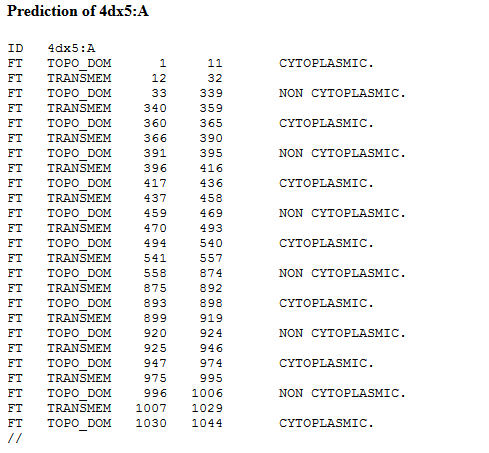
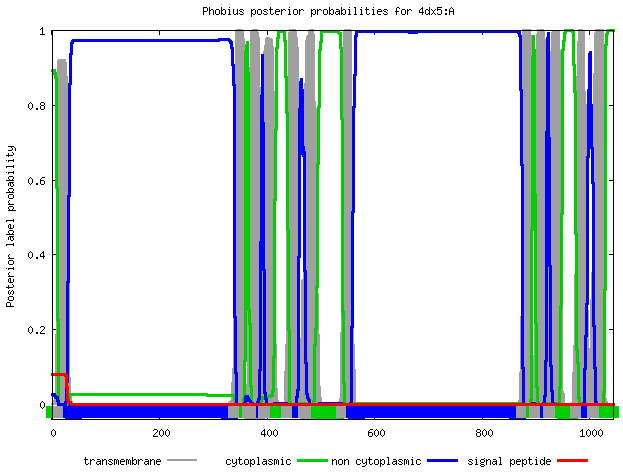
| Координаты трансмембранных спиралей | 1( 9- 27), 2( 340- 361), 3( 365- 386), 4( 394- 414), 5( 439- 458), 6( 470- 492), 7( 538- 557), 8( 873- 894), 9( 896- 919), 10( 927- 946), 11( 971- 991), 12(1003-1025) |
| Среднее количество остатков в одной трансмембранной спирали белка | 12 |
| данные для второго белка | 2jk4_A |
| Толщина гидрофобной части мембраны | 23.4 Å |
| Координаты трансмембранных спиралей | 1(29-36), 2(42-51), 3(58-65), 4(72-79), 5(84-90), 6(98-105), 7(115-122), 8(126-134), 9(141-148), 10(152-160), 11(170-176), 12(182-187), 13(193-199), 14(206-213), 15(222-228), 16(235-241), 17(246-252), 18(258-266), 19(277-285)
| | Среднее количество остатков в одном трансмембранном β-тяже белка | 8 |
|
| Задание 3 |
| Многокомпонентный / краситель / детергент / соль для органического растворителя (субстраты включают хлорамфеникол, тетрациклин, эритромицин,
налидиксовая кислота, фузидиновая кислота, фторхинолоны, липофильные β-лактамы, норфлоксацин, доксорубицин, новобиоцин,
рифампин, триметоприм, акрифлавин, кристалл-фиолетовый, этидий, дезинфицирующие средства, родамин-6G, ТРП, бензалконий, SDS, Triton X-100,
дезоксихолат / желчные соли / органические растворители (алканы), ингибирующие рост стероидные гормоны (эстрадиола и прогестерон) и фосфолипиды) (Elkins and Mullis, 2006).
Был предложен механизм бокового захвата субстратов из липидного бислоя в AcrB и его гомологов (Yu et al., 2003a, 2003b).
Известна асимметричная тримерическая структура установлена с использованием АгА, имеющей гексамерную структуру, и TolC имеет тримерную структуру (Seeger et al., 2006].
Также известна структура комплекса с YajC (Törnroth-Horsefield et al., 2007).
Ковалентно связанный тример AcrB доказывает наличие перистальтического взаимодействия, альтернативного доступа, механизма вращения (Takatsuka and Nikaido, 2009; Nikaido and Takatsuka, 2009; Pos, 2009)
Дальнейшие доказательства наличия вращательного механизма основывается на кинетическом анализе оттока цефалоспоринов, который может проявлять положительную кооперативность (Nagano and Nikaido, 2009).
Возможен также и экспорт сигнальных молекул для связи клеток-клеток (Yang et al., 2006).
Субстраты могут захватоваться в нижней области AcrB, а затем транспортироваться через связывающие карманы, ворота и, наконец, в воронку AcrA, которая соединяет AcrB с TolC (Husain & Nikaido и др., 2010).
AcrB был преобразован в протонный насос с легким управлением, используя дельта-родопсин (dR), связанный с AcrB через трансмембранный домен гликофорина A.
Это создало белок н, способный избирательно захватывать антибиотики из объемных растворов за счет энергии солнечного света (Kapoor и Wendell 2013).
Тримерная структура необходима для активности (Ye et al., 2014). Была продемонстрирована ассоциация с AcrZ (TC # 8.A.50), небольшой 1 TMS-белок (49 aas), который модифицирует субстратную специфичность AcrAB (Hobbs et al., 2012).
Аналогичным образом связывание YajC с AcrB стимулирует экспорт ампициллина (Törnroth-Horsefield et al., 2007).
AcrZ связывается с AcrB на вогнутой поверхности трансмембранного домена (Du et al., 2015).
Связывание субстрата ускоряет конформационные переходы и диссоциацию субстрата, демонстрируя кооперативность (Wang et al., 2015).
Общая структура AcrAB-TolC иллюстрирует модель моста адаптера, в которой воронкообразный гексамер AcrA образует взаимозаменяемое взаимодействие зубчатого колеса с областью наконечника альфа-ствола TolC.
Прямое взаимодействие между AcrB и TolC не допускается (Kim et al., 2015).
TMS2 в AcrB требуется для связывания липофильных карбоксилатов.
Канавка, образованная интерфейсом между TMS1 и TMS2, специфически связывает фузидиевую кислоту и другие липофильные карбоксилированные препараты (Oswald et al., 2016).
После связывания лиганда протон может связываться с кислотным остатком (ами) в трансмембранном домене, то есть Asp407 или Asp408, в предполагаемой сети электростатически взаимодействующих остатков, которые также включают Lys940 и Thr978, и это может инициировать серию конформационных изменения, которые приводят к вытеснению наркотиков (Su et al., 2006).
His978, вероятно, находится на пути H + (Takatsuka и Nikaido 2006).
AcrAB-TolC выделяется на старый полюс после деления клеток, заставляя две дочерние клетки проявлять разные лекарственные сопротивления (Bergmiller et al., 2017). |
|