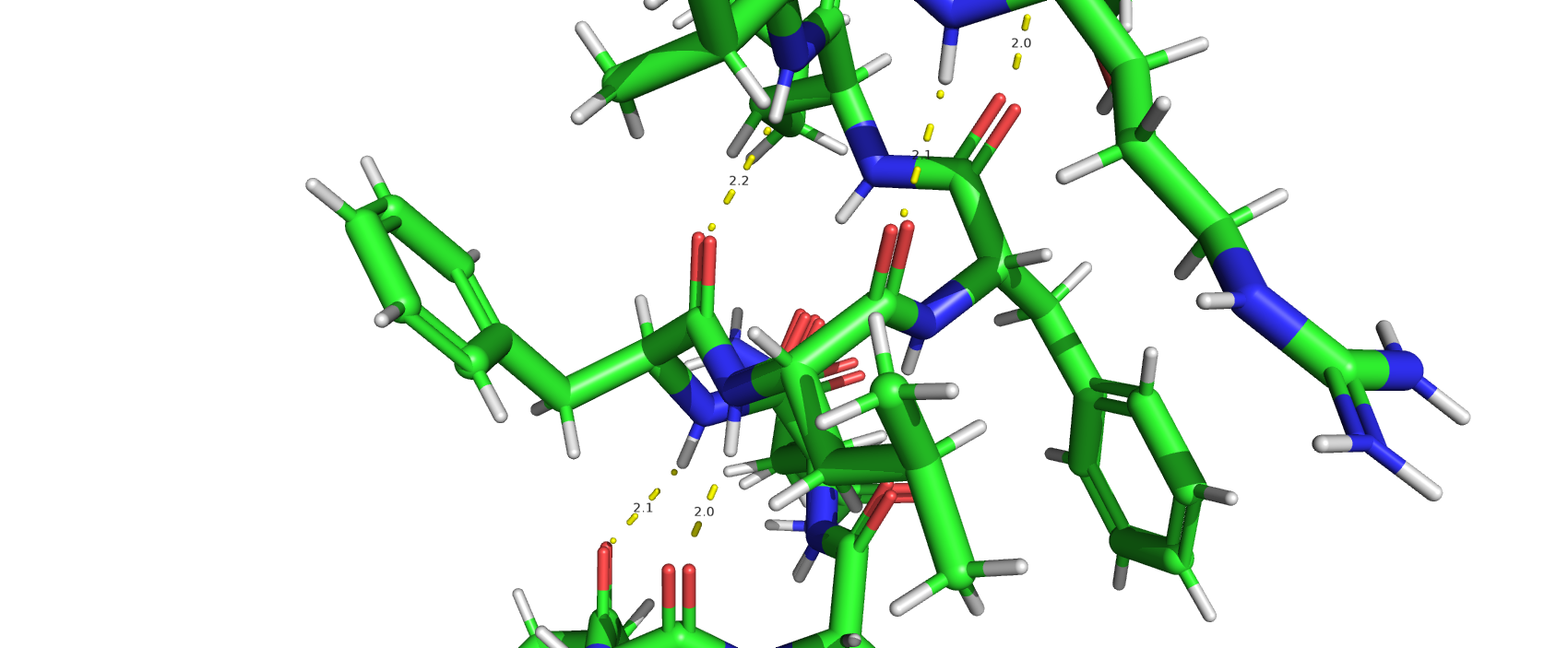
Водородные связи между атомами азота одной пептидной связи и карбонильным C' атомом кислорода другой пептидной связи остова белка (Рис. 1) являются осноным фактором стабилизации его вторичной структуры (альфа-спиралей, бета-листов и т.д.)

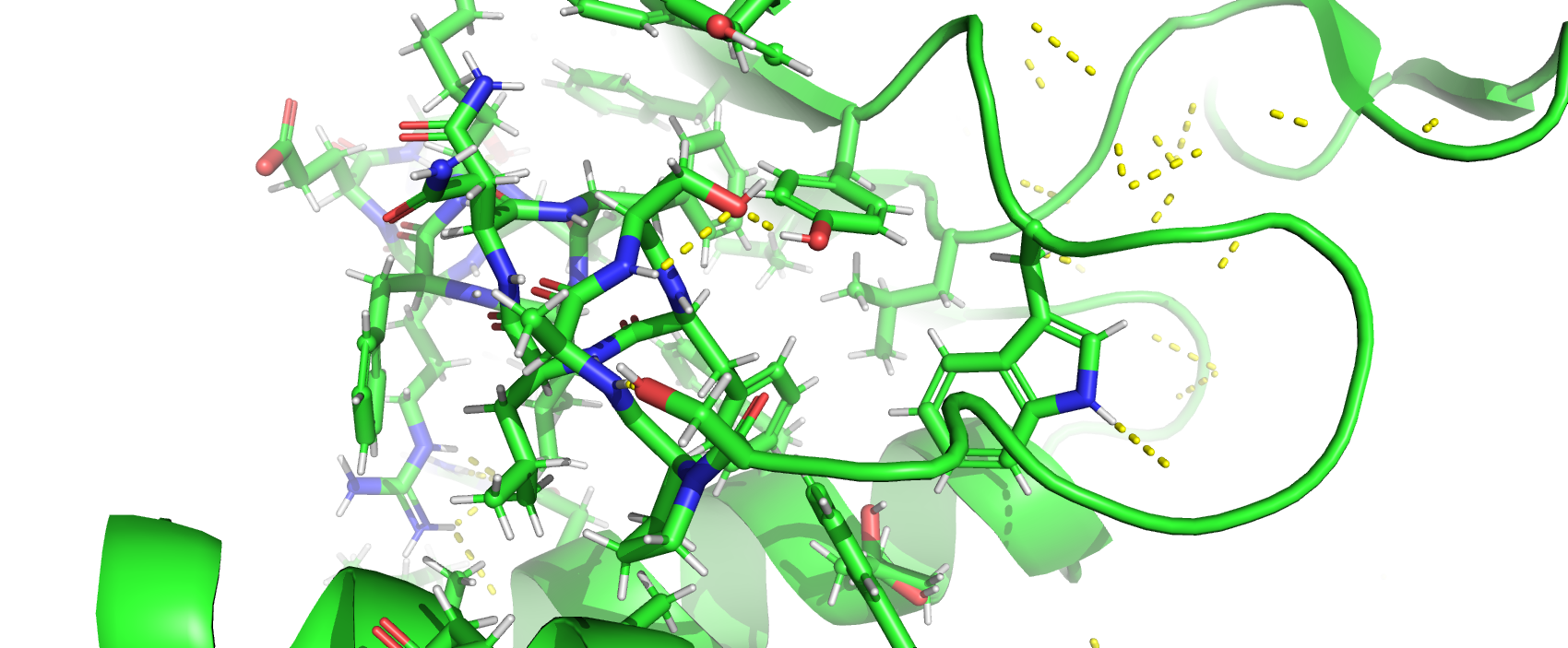
Водородные связи между атомами боковых радикалов аминокислот (Рис. 2) участвуют в формировании третичной и четвертичной структуры белка, стабилизации вторичной структуры белка, формировании активного центра ферментов и рецепторов.
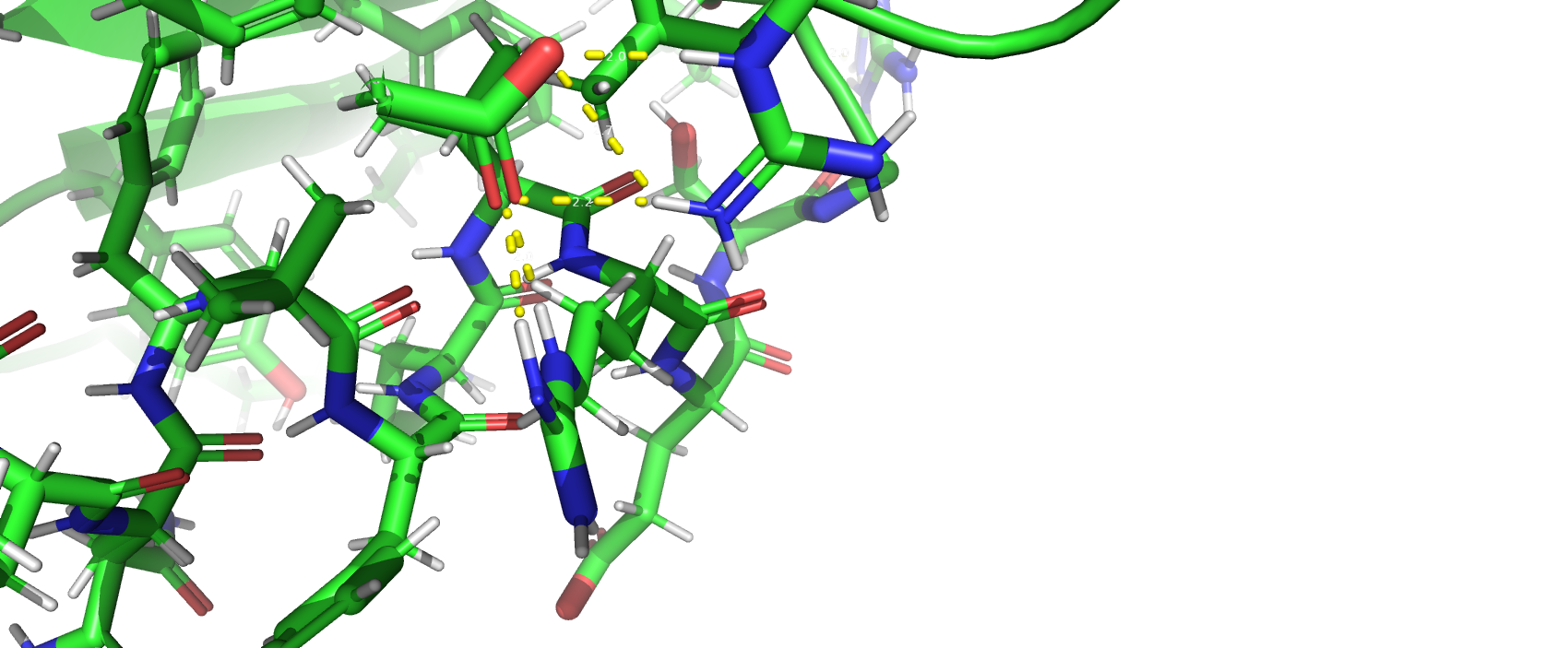
Солевые мостики - это электростатические взаимодействия между положительно и отрицательно заряженными боковыми радикалами аминокислот (Рис. 3). Положительно заряженные аминокислоты: аргинин, гистидин, лизин. Отрицательно заряженные аминокислоты: глутамат, аспартат. Эти контакты стабилизруют третичную структуру белка.
Дисульфидные связи это s-s связи между серой боковых радикалов цистеина. Они поддерживают третичную и четвертичную структуру. В структуре тирозиновой протеинфосфатазы нерецепторного типа 1 дисульфидные мостики не могут быть представлены (Рис. 4), так как данный белок находится в цитозоле, где восстановительная среда (большое количество восстановительных факторов, например, глутатион) делает их нестабильными.
Стэкинг взаимодействия между ароматическими p-сопряженными системами боковых цепей аминокислот стабилизируют вторичную и третичную структуру, могут участвовать в формировании активного центра фермента или рецептора. Стэкинг взаимодействий в стирозиновой протеинфосфатазн нерецепторного типа 1 отсутствуют (Рис. 5).