Визуализация молекул в JMol
В этом практикуме ведётся работа с файлами формата *.pdb. Мне был выдан файл с идентификатором 6BIO.
Апплет с изображением молекулы
В приведённом окне изображена молекула белка NlpC1 организма Trichomonas vaginalis. Нажмите на кнопку "Start script", чтобы запустить сценарий, и "Resume", чтобы продолжить. Сценарий запускается и автоматически — при загрузке апплета.
Сценарий, исполняемый апплетом, также можно скачать.
Параметры водородных связей между остовными атомами азота и кислорода
| # | Имена атомов | Длина связи N—O, Å | Угол N—O—C, ° |
|---|---|---|---|
| Альфа-спирали | |||
| 1 | N(188ASN)—O(184GLN) | 2,87 | 156,9 |
| 2 | N(201GLN)—O(197THR) | 2,86 | 163,7 |
| 3 | N(189ARG)—O(185TRP) | 3,16 | 156,9 |
| 4 | N(154ARG)—O(150ASN) | 3,22 | 148,7 |
| 5 | N(187TYR)—O(183MET) | 3,20 | 156,1 |
| Бета-тяжи | |||
| 1 | N(177TYR)—O(166LYS) | 3,10 | 161,1 |
| 2 | N(30ALA)—O(43TYR) | 2,87 | 143,2 |
| 3 | N(65ILE)—O(68GLU) | 2,82 | 162,5 |
| 4 | N(70CYS)—O(63VAL) | 2,99 | 158,0 |
| 5 | N(63VAL)—O(70CYS) | 2,81 | 169,1 |
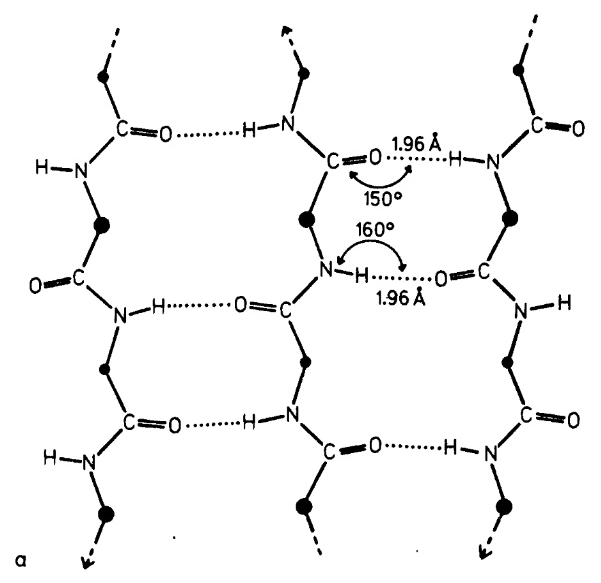
Посчитаем средние значения всех приведённых параметров и будем считать их «типичными» в рамках данной работы. Для длин связей и углов в альфа-спиралях получаем 3,06 Å и 156,5° соответственно, для бета-тяжей — 2,92 Å и 158,8°. «Идеальные» параметры оценим по источникам: в статье [1] приведены подробные данные по идеальным параметрам альфа- и 310-спиралей; так как для атомов в разных положениях параметры разные, мы тоже возьмём среднее. Получаем 3,03 Å и 155,7° для альфа-спиралей. Данные по бета-тяжам почерпнём в книге [2], стр. 357 (в исследуемом белке не выявлено ни одного параллельного в строгом смысле тяжа, такого, чтобы между параллельными цепями было хотя бы две связи, в связи с чем цифры учтём для антипараллельных). Расстояния там приведены только O—H, поэтому для пересчёта в N—O воспользуемся известным углом и теоремой косинусов. (Длину связи N—H используем по [3], рис. 4, равной 1 Å). Угол N—O—C оценим из углов N—H—O, H—O—C и известных расстояний (см. рис. 1).
По теоереме синусов NO/sin(160°) = NH/sin(∠NOH), откуда ∠NOH ≈ 6,7°. Используя сферическую (пространственную) теорему косинусов, можно доказать, что в данных условиях максимум и минимум ∠NOC достигаются, когда все 4 атома в одной плоскости. Мы же опустим эту часть и примем на веру, что максимум равен ∠HOC + ∠NOH = 156,7°, а минимум — ∠HOC - ∠NOH = 143,3°. Итак, идеальные параметры водородных связей в антипараллельных бета-тяжах — 143,3..156,7° и 2,92 Å.
| Параметр | Идеальное значение | Наблюдаемое значение | Отличие от идеального |
|---|---|---|---|
| Альфа-спирали | |||
| Длина связи N—O | 3,03 Å | 3,06 Å | 1,0 % |
| Угол N—O—C | 155,7° | 156,5° | 0,5 % |
| Бета-тяжи | |||
| Длина связи N—O | 2,92 Å | 2,92 Å | мало |
| Угол N—O—C | 143,3..156,7° | 158,8° | 1,4..10,3 % |
Можно отметить, что измеренные значения достаточно близки к идеальным.
Использованная литература
- Aravinda, S., Datta, S., Shamala, N., and Balaram, P. (2004). Hydrogen-Bond Lengths in Polypeptide Helices: No Evidence for Short Hydrogen Bonds. Angewandte Chemie International Edition, 43(48), 6728–6731. doi:10.1002/anie.200461127
- Jeffrey G.A. Hydrogen bonding in biological structures / G.A. Jeffrey, W. Saenger. - Berlin, Heidelberg: Springer, 1994. - X1.,569 p. - ISBN 3-540-57903-6
- Онлайн-документ: https://studfiles.net/preview/6172169/page:3/