Учебный сайт Саши Якушевой |
||||
Второй семестр |
||||
Главная |
Семестры |
Обо мне |
Ссылки |
|
|
Остовные водородные связи и элементы вторичной структуры Водородная связь образуется между водородом, связанным с электроотрицательным атомом, и другим электроотрицательным атомом. Вторичные структуры белка, α-спираль и β-лист, образуются благодаря водородным связям между атомами главной цепи (водородом NH-группы и кислородом СО-группы). Рассмотрим строение одной α-спирали белка семейства E II стадии споруляции (Stage II Sporulation E Family Protein from Thermanaerovibrio acidaminovorans). На рисунке 1 показаны все α-спирали молекулы белка. 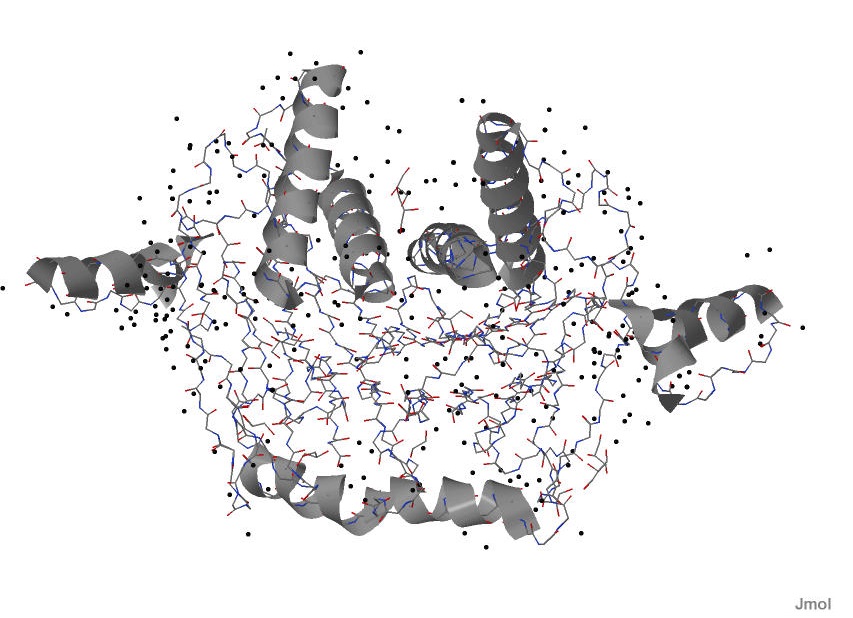
Рис. 1. Трёхмерная структура белка. В модели ribbons серым цветом выделены α-спирали. На рисунке 2 показана α-спираль с водородными связями в ней. 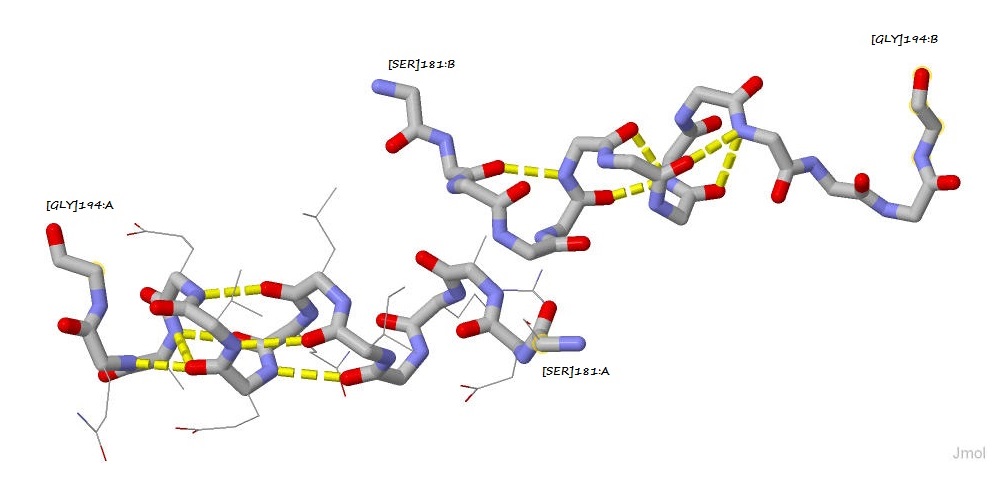
Рис. 2. Строение α-спирали белка. Раскраска атомов: серые — атомы углерода, голубые — атомы азота, красные — кислорода. Жёлтым пунктиром обозначены водородные связи. Рассмотрим строение β-листа. На рисунке 3 показаны все β-листы данного белка. Каждый β-лист состоит из нескольких тяжей, которые могут быть параллельны или антипараллельны. За счёт водородных связей, образующихся между водородом NH-группы одного тяжа и кислородом СО-группы соседего тяжа, такая структура стабилизируется. 
Рис. 3. Трёхмерная структура белка. В модели ribbons серым цветом выделены α-спирали. На рисунке 4 показан β-лист с водородными связями в нём. Тяжи пронумированы. Тяжи 1 и 2, а также тяжи 2 и 3 аптипареллельны друг другу, тяжи 3 и 4 - параллельны. 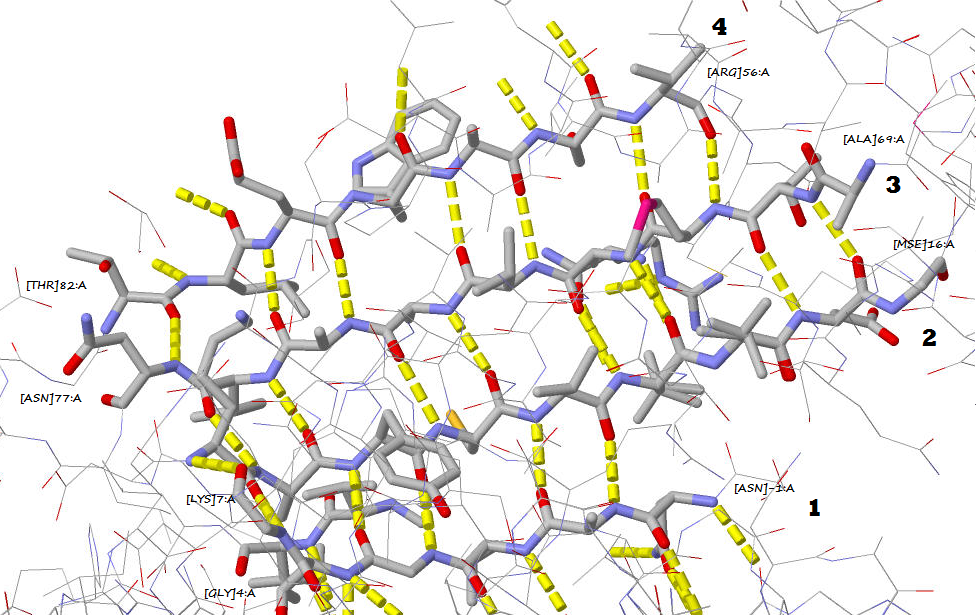
Рис. 4. Строение β-листа белка. Раскраска атомов: серые — атомы углерода, голубые — атомы азота, красные — кислорода. Жёлтым пунктиром обозначены водородные связи. © Саша Якушева, 2013
|