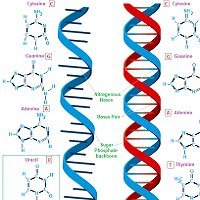
Изображение азотистых оснований и фрагмента ДНК с помощью MarvinSketch
Программа MarvinSketch предназначена для создания изображений химических
структур.
В ней с помощью готовых шаблонов (Template > Nucleosides) и других инструментов
были нарисованы структуры, изображенные на рис.1 и 2.
Файл с результатами:
посмотреть.
На рис.1 изображены нуклеотиды 2'-дезоксигуанозиндифосфат и 2'-дезокситимидинмонофосфат,
которые состоят из азотистых оснований, дезоксирибозы и двух или одного остатка фосфорной
кислоты соответственно.
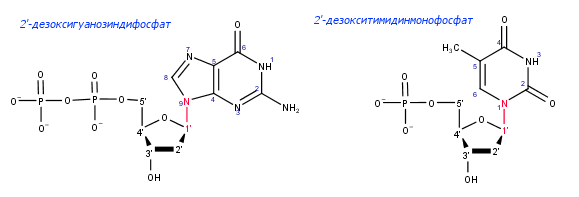 Рис.1. 2'-дезоксигуанозиндифосфат и
2'-дезокситимидинмонофосфат
Рис.1. 2'-дезоксигуанозиндифосфат и
2'-дезокситимидинмонофосфат
На рис.2 изображены нуклеозиды уридин и псевдоуридин, которые встречаются в РНК.
Они состоят из азотистого основания и рибозы.
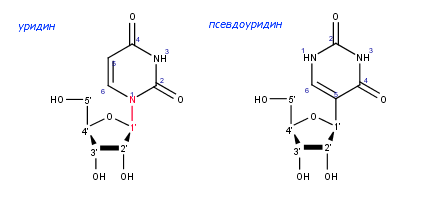 Рис.2. Уридин и псевдоуридин
Рис.2. Уридин и псевдоуридин
Атомы остатков азотистых
оснований и сахара пронумерованы, красным цветом выделены атомы, связанные
N-гликозидной связью. Обратите внимание, что у псевдоуридина образуется связь C(5)—C(1'),
поэтому она не выделена красным.
Также было воспроизведено изображение фрагмента двухцепочечной ДНК, приведенного
в презентации к занятию (рис.3). Остов выделен красным цветом, азотистые основания
подписаны. Стрелками показано направление цепи от 5' конца к 3' концу. Водородные
связи указаны пунктирными линиями.
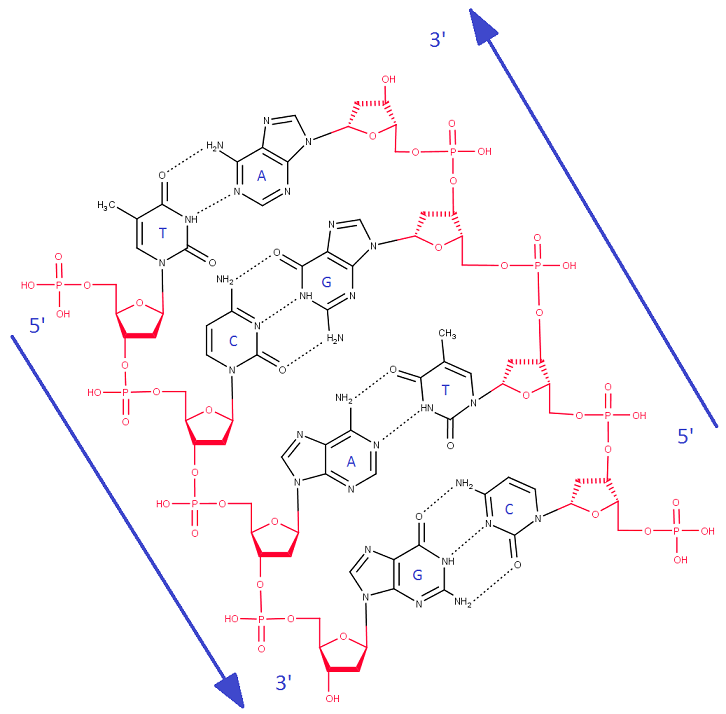 Рис.3. Изображение фрагмента ДНК
Рис.3. Изображение фрагмента ДНК
Изображение азотистых оснований и фрагмента ДНК с помощью MarvinSketch
Помимо образования водородных связей при известных канонических взаимодействиях
теоретически возможны и другие варианты — неканонические взаимодействия. В этом
разделе я попробую рассмотреть такие взаимодействия для тимина (выбран случайно, т.к.
страница с распределением оснований на kodomo не существует), не забывая об его
таутомерах. Явление таутомерии заключается в том, что вещество определенного состава
и молекулярного веса существует в виде равновесной смеси двух или нескольких изомеров,
легко переходящих друг в друга. Во многих случаях таутомерия обусловлена миграцией
катиона водорода (протона) от одного атома молекулы к другому.
Файл с результатами:
посмотреть.
Итак, с помощью программы MarvinSketch (Tautomer Generator) были найдены всевозможные таутомеры тимина.
На рис.4 изображены все 9 полученных таутомеров. Отметим, что в ДНК всегда присутствует форма с
кетонной группой С=О, а не с гидроксилом ОН.
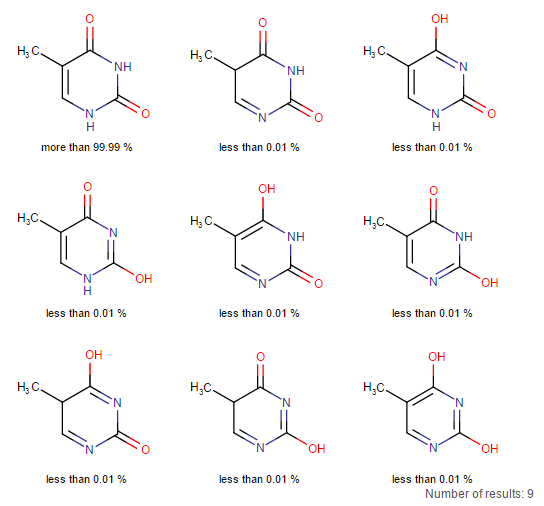 Рис.4. Структурные формулы таутомеров тимина
Рис.4. Структурные формулы таутомеров тимина
Однако учитывать распространенность той или иной формы я не буду. Единственное, я рассмотрю
образование неканонических пар только с участием трех форм тимина и только для
антипараллельных цепей, так как рассматривание всех возможных взаимодействий со
всеми таутомерами, как мне кажется, излишне. Уверена, что по паре примеров общий принцип будет вполне понятен.
На рис.5 представлены рассматриваемые нами нуклеотиды (обозначены для удобства):
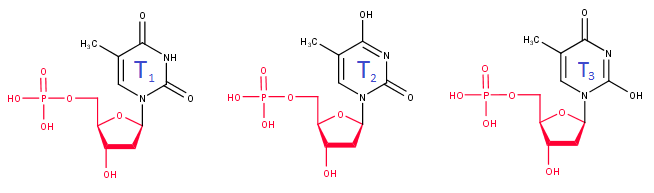 Рис.5. Рассматриваемые нуклеотиды
Т=Т
Рис.5. Рассматриваемые нуклеотиды
Т=Т. Сначала рассмотрим возможные взаимодействия между всеми этими таутомерами, т.е.
взаимодействия Т=Т (рис.6). Как мне кажется, все пары будут обладать примерно одинаковой устойчивостью:
первая (T
1=T
1), возможно, будет дестабилизироваться торчащими наружу аминогруппой и
кетонной группой, а во всех остальных случаях атомы кислорода и азота будут отталкиваться друг от друга.
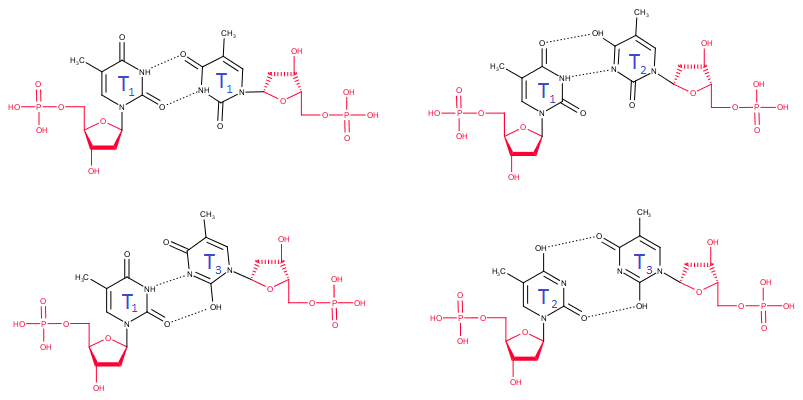 Рис.6. Возможные взаимодействия Т=Т
Т=A
Рис.6. Возможные взаимодействия Т=Т
Т=A. Теперь обсудим возможные взаимодействия Т=А (рис.7). Взаимодействие T
1=А
является каноничным (уотсон-криковская пара). Уотсон-криковские пары энергетически наиболее выгодны.
Это связано с тем, что в этих парах центры с повышенной и пониженной электронной плотностью
оснований расположены оптимально друг относительно друга. Комплементарные пары
оснований в нуклеиновых кислотах стабилизированы преимущественно электростатическими взаимодействиями.
Существует также хугстиновская пара А=Т, но мы условились рассматривать только антипараллельные цепи.
Вторая полученная пара T
3=A также выглядит довольно устойчивой.
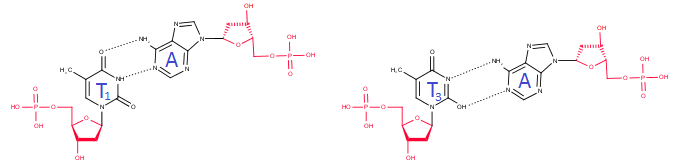 Рис.7. Возможные взаимодействия Т=А
Т=C
Рис.7. Возможные взаимодействия Т=А
Т=C. В случае взаимодействия Т=С (рис.8), как мне кажется, обе пары будут недостаточно
устойчивы по причинам, описанным в пункте для Т=Т.
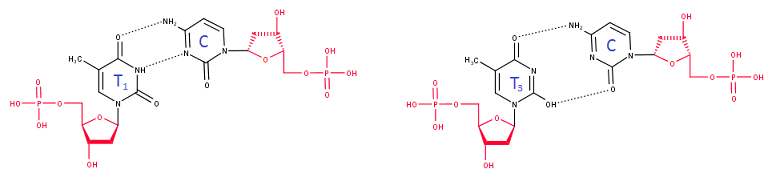 Рис.8. Возможные взаимодействия Т=С
Т-G
Рис.8. Возможные взаимодействия Т=С
Т-G. Напоследок рассмотрим взаимодействие Т и G (рис.9). В двух предложенных случаях образуются
двойные связи: T
1=G и T
3=G, причем обе, похоже, схожи по устойчивости. В случае
пары T
2 и G образуются три водородные связи, что делает это взаимодействие прочнее упомянутых ранее.
Возможно, наличие трех водородных связей и возможная устойчивость этой пары могут служить поводом для
дальнейших более тщательных исследований.
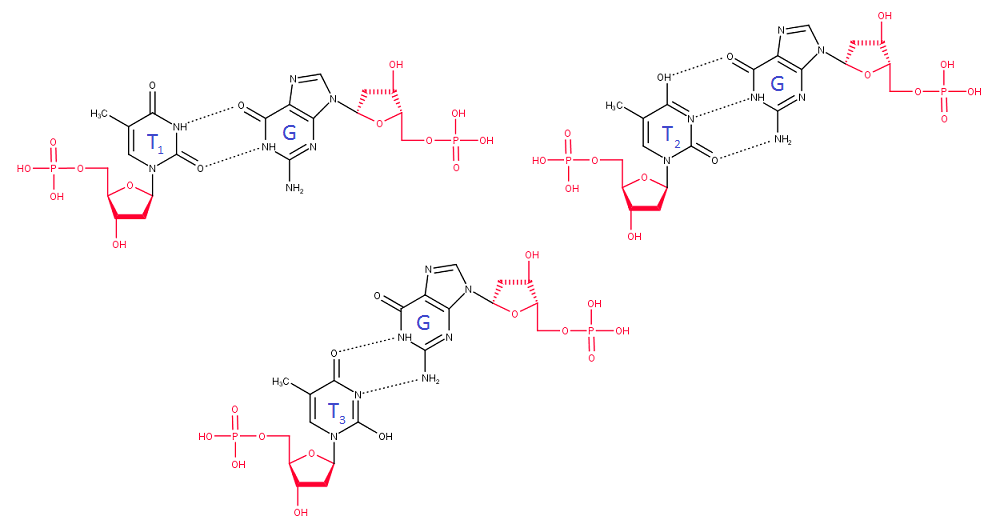 Рис.9. Возможные взаимодействия Т и G
Рис.9. Возможные взаимодействия Т и G