Электронная плотность
Задание 1: ЭП - хорошая и плохая расшифровки
PDB ID моего белка — 1PJX и 3I1C, причем разрешение первой структуры выше чем второй (разрешения составили 0.85 Å и 2.20 Å соответственно). Давайте посмотрим как они выглядят (рис. 1)
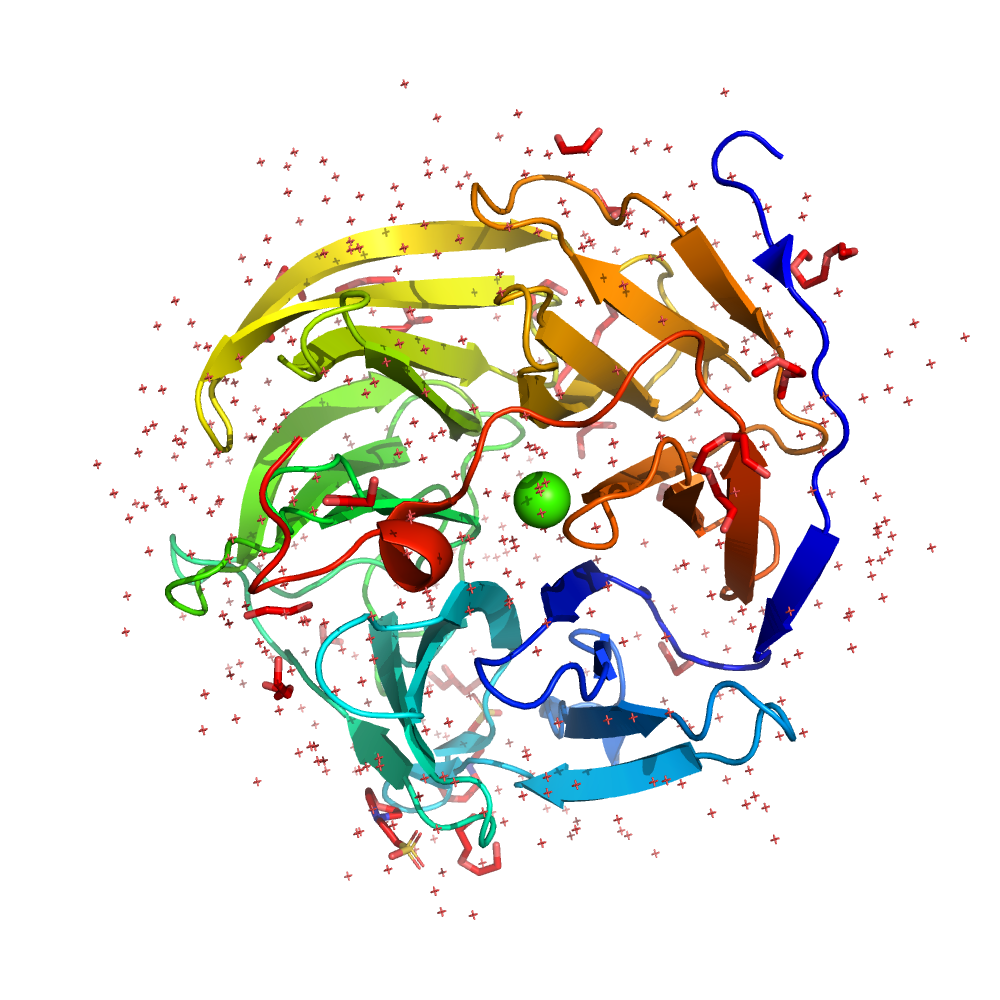
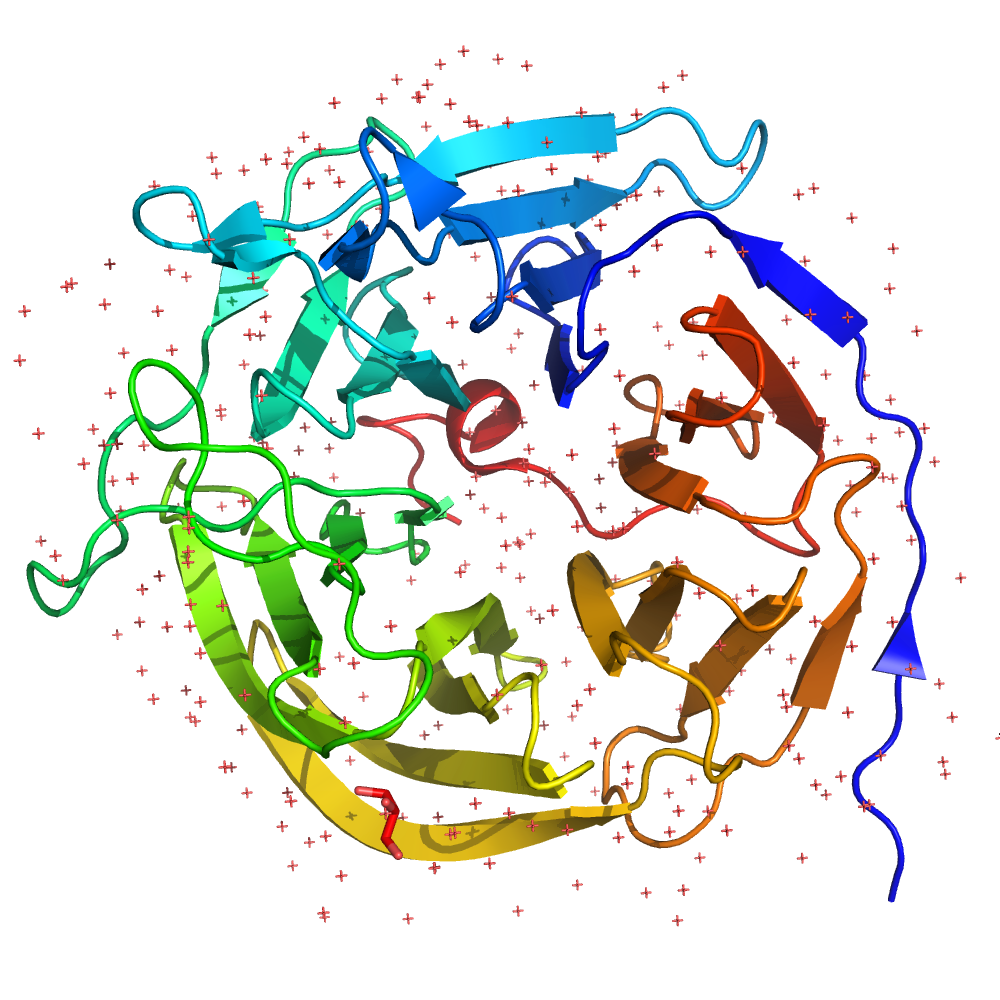
Белок представляет собой шестилопастной бета-пропеллер. Можно видеть, что структура 1PJX содержит помимо белка молекулы буфера для кристаллизации (глицерин, PEG, MES буфер), а также ионы кальция. При взгляде на структуры мне показалось, что концы белковых цепей по-разному свернуты, чтобы это проверить я решила выровнять структуры (рис. 2)
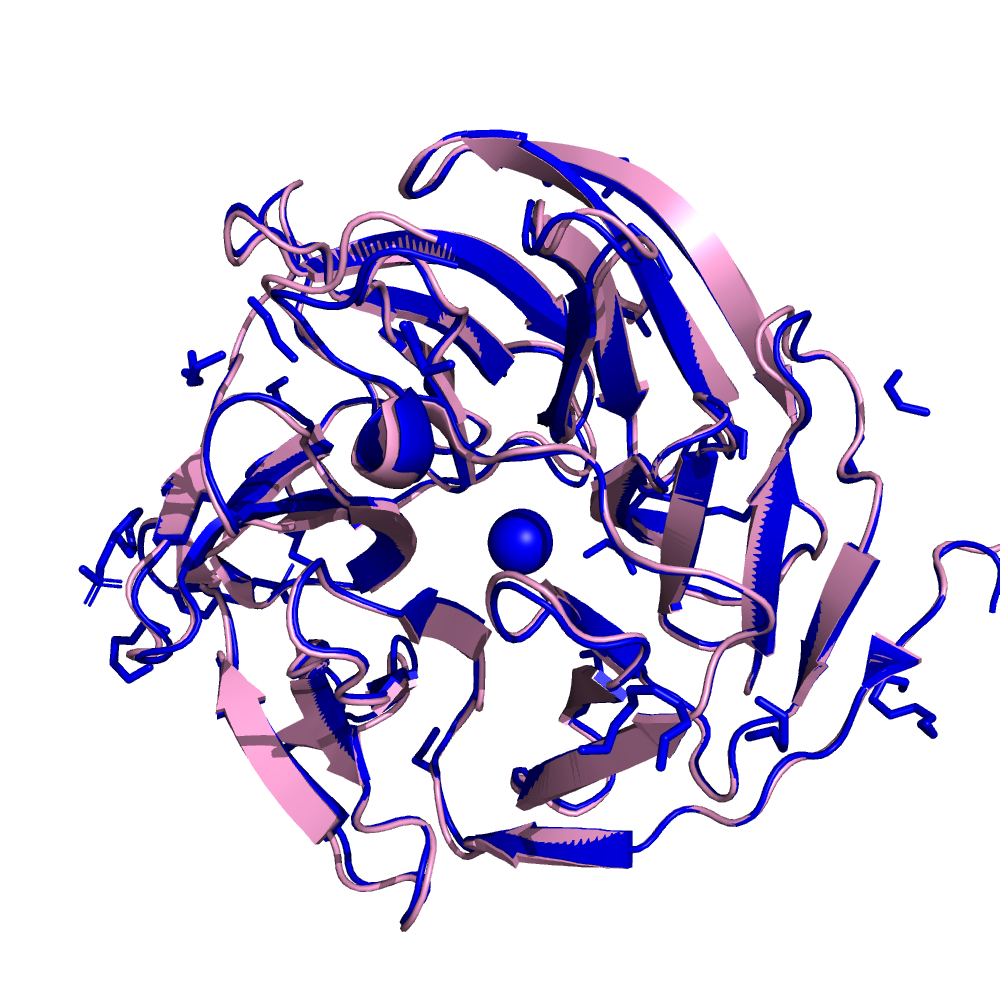
Исходя из выравнивания я заключила что внешне структуры очень схожи (RMSD составило 0.347), некоторые участки не совпадают в точности, концы действительно оказались по-равзному ориентированы, однако имеют право:) (то есть, я думаю, что самые концы не входят в состав вторичной структуры и таким образом их ориентация в большей степени зависит от кристаллизации, нежели от качества восстановления структуры)
Далее я открыла файлы электронных структур. Чтобы визуализировать фрагмент структуры были вызваны следующие команды PyMol:
select gly227, resi 227
isomesh gly_meh, {protein_id}_2fofc, 2, gly227, carve=2
Вот такие изобажения я получила для 227 остатка глицина (рис. 3)
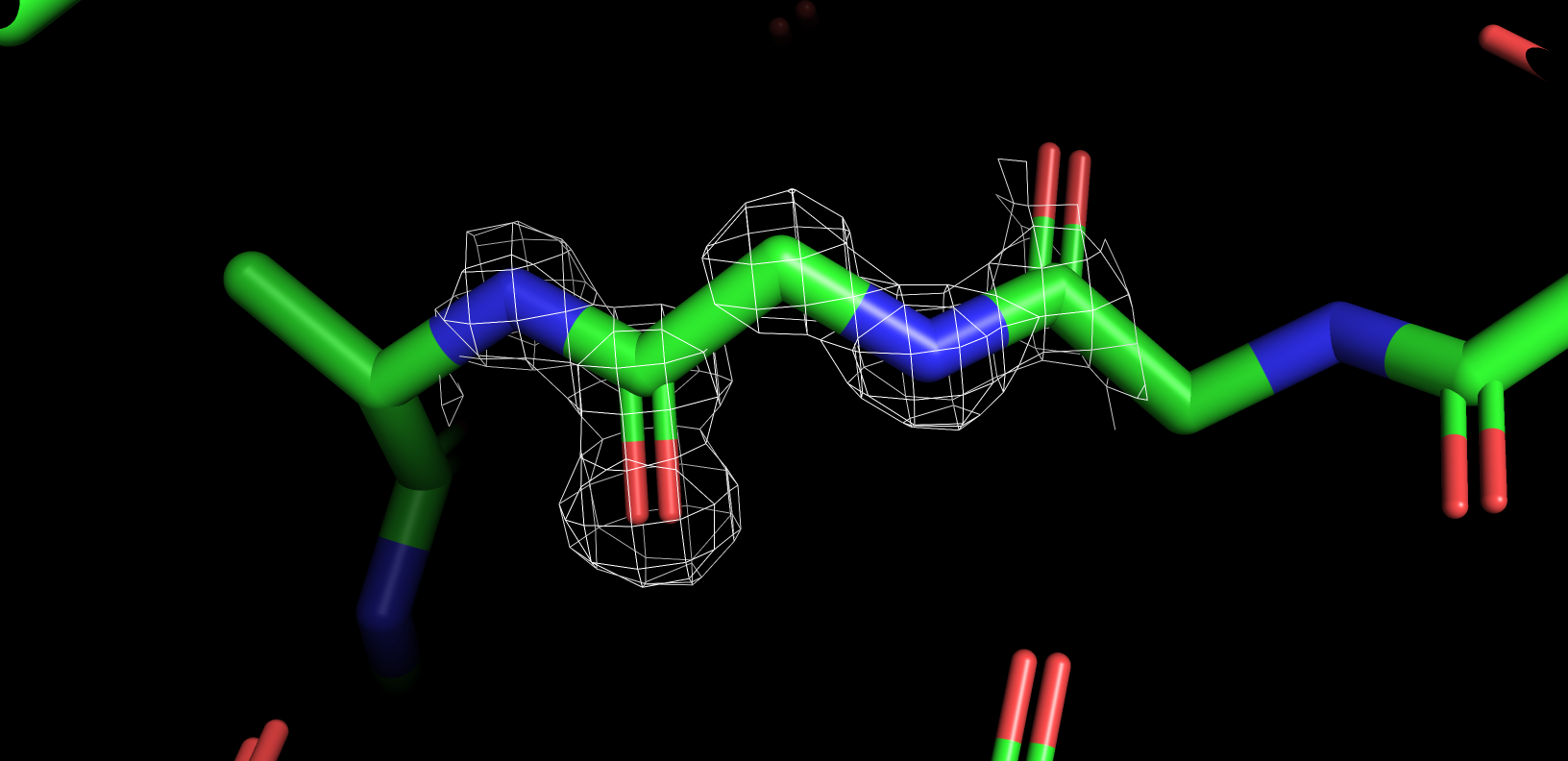
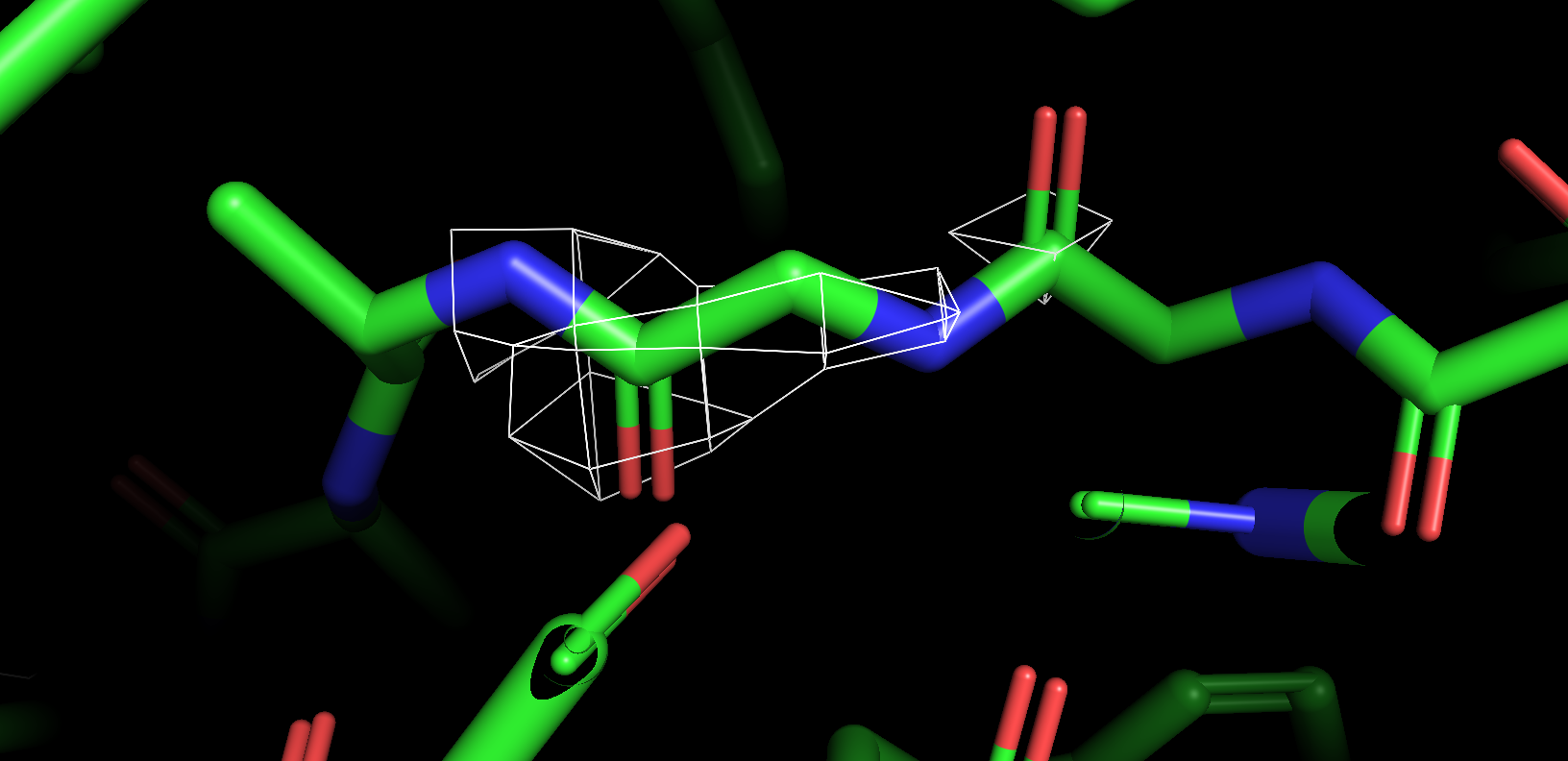
На изображениях видно, что для структуры 1PJX разрешение выше, это ясно, посколько электронная плотность отдельных этомов приобретает характерную форму шара.
Задание 2: ЭП и положение в структуре
Для этого задания мне досталась структура с PDB ID 2A3R. Далее я получила серию картинок с разными уровнями подрезки электронной плотности при помощи следующих команд:
fetch 2A3R
fetch 2A3R type=2fofc
show sticks, backbone
isomesh meh_{1-3}, 2A3R_2fofc, {1-3}, backbone, carve=2
Вот такие изображения белка я получила:
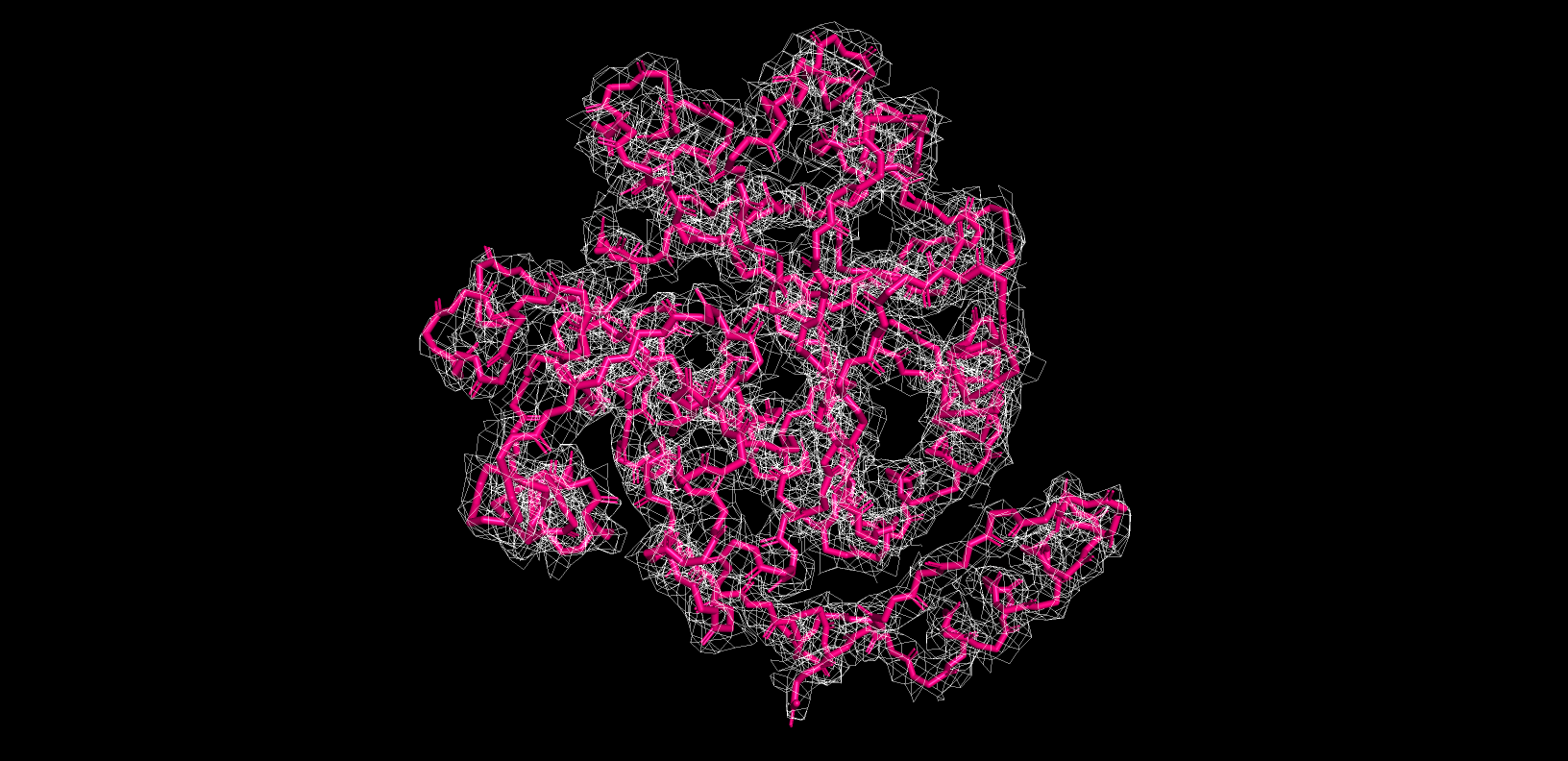
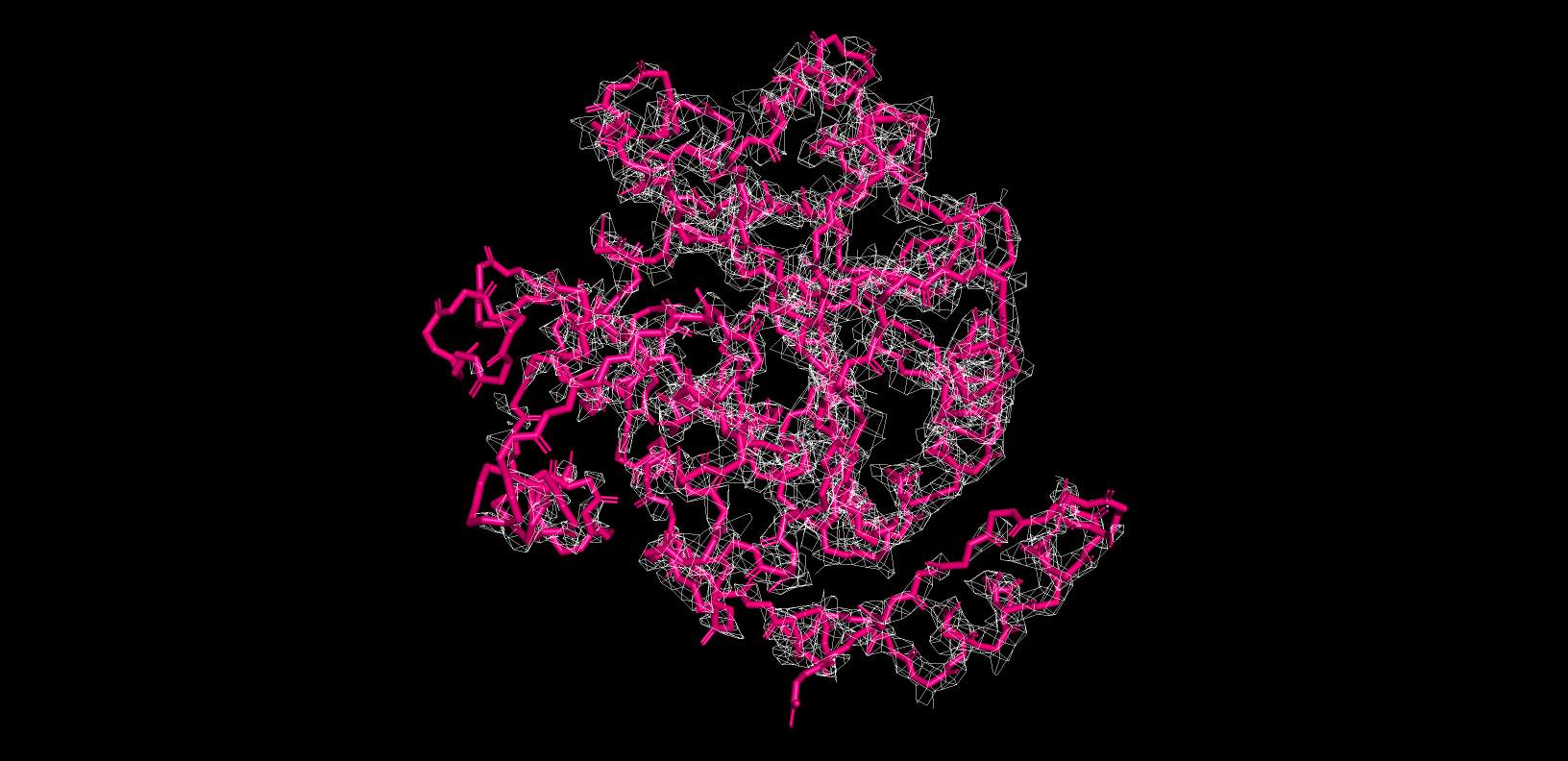

Действительно увеличивая уровень подрезки, можно налюдать снижение покрытия некоторых регионов mesh-ем. У меня это определенная боковая поверхность белка которая не контактирует второй цепью, а также самый кончик остова. Данные участки в меньшей степени взаимодействуют с остальным белком по сравнению с коровой частью. Кроме того поскольку в файле белок было две молекулы белка, где поверхность, расположенная ближе к второй белковой цепи имела большее покрытие, можно предположить, что за счет взаимодействий двух цепей белка коцформаций остова там меньше.
Задание 3: Альтернативные положения
Мне достался вариант B этого задания, то есть в белке с PDB ID: 6FWJ мне нужно найти альтлоки 136 аргинина. Pymol показывает сразу две конформации, если просто открыть файл с структурой:
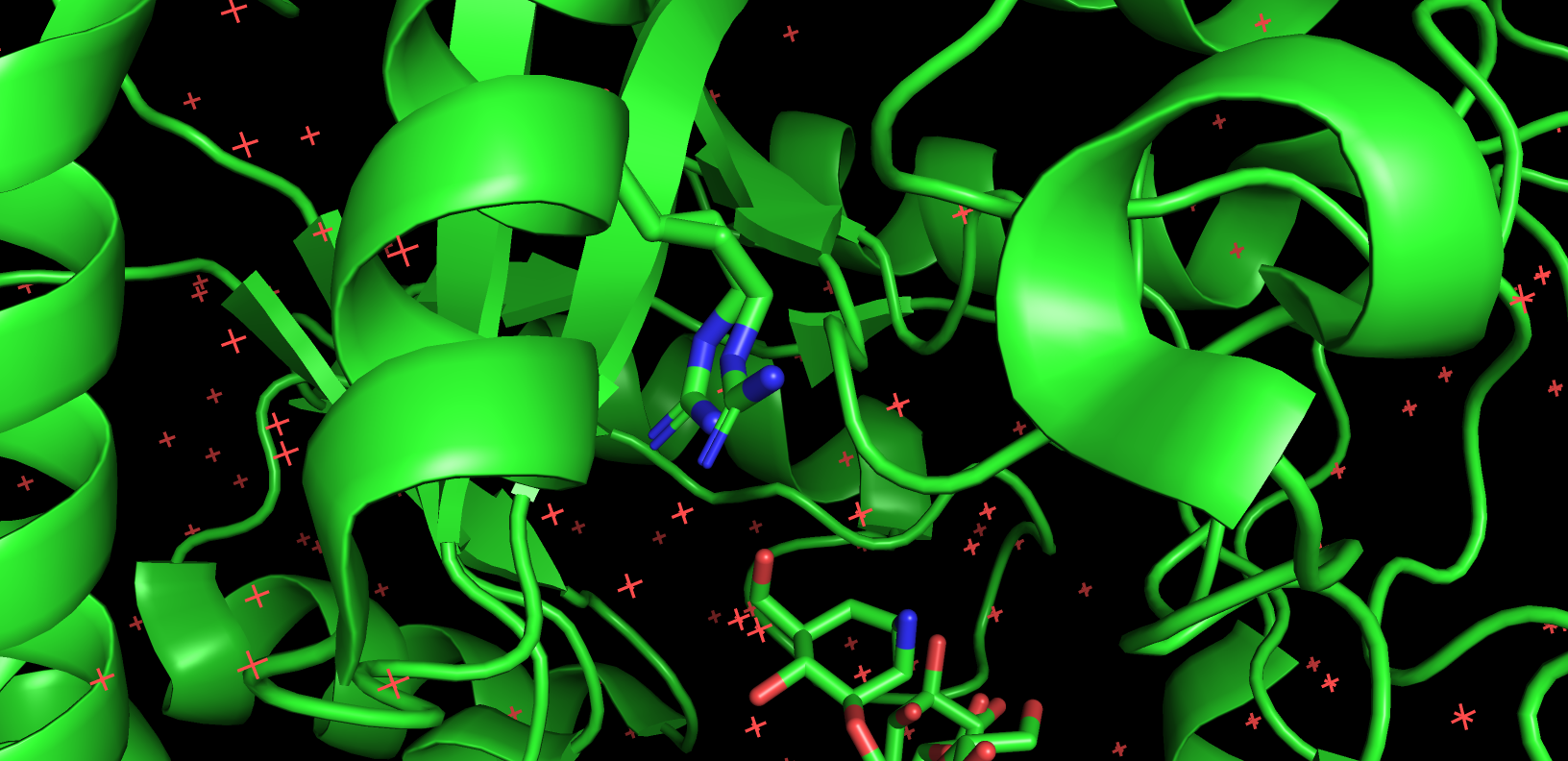
Рассмотрим теперь какие взаимодействия стабилизируют эти две конформации (рис. 6)
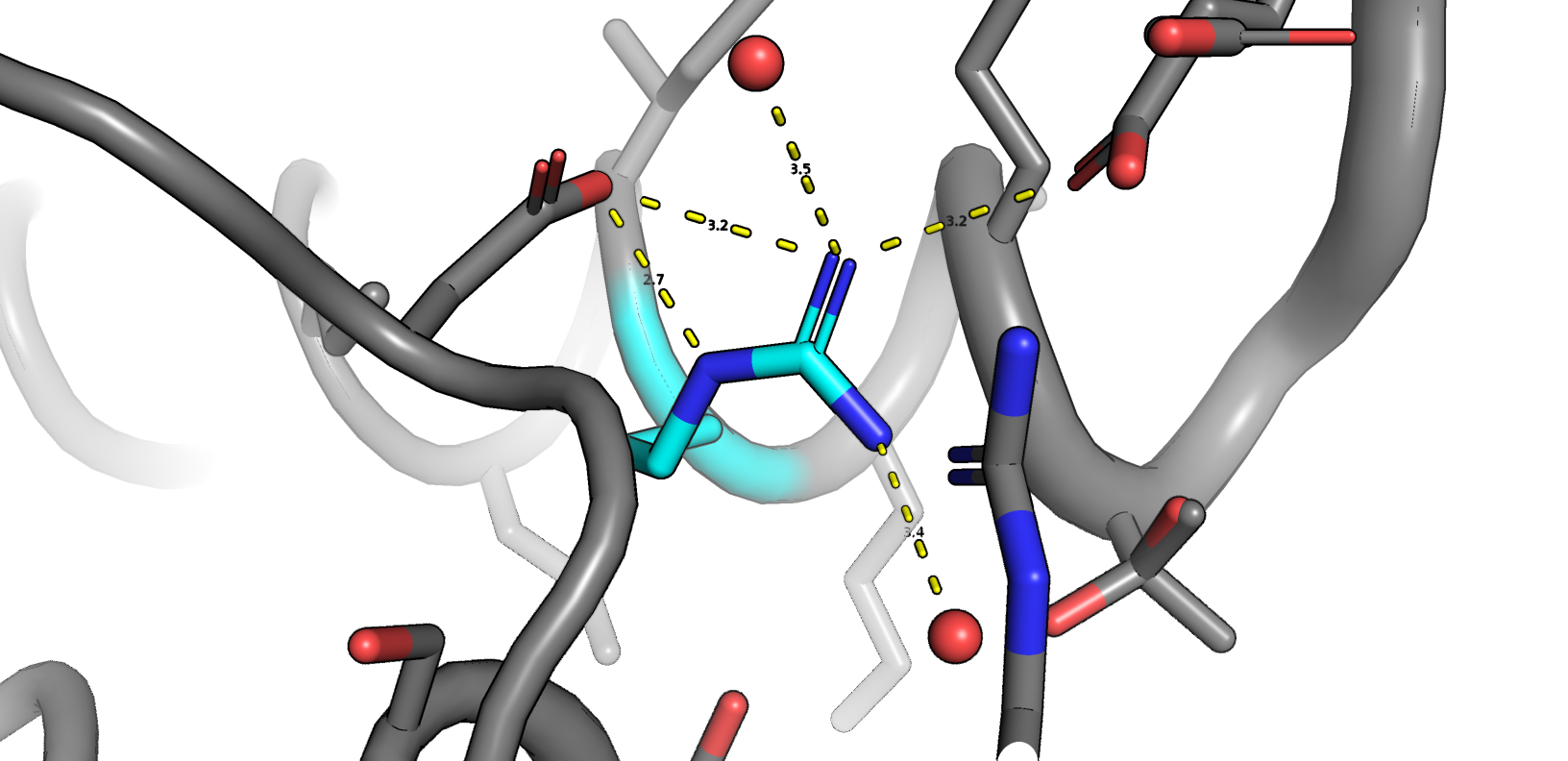
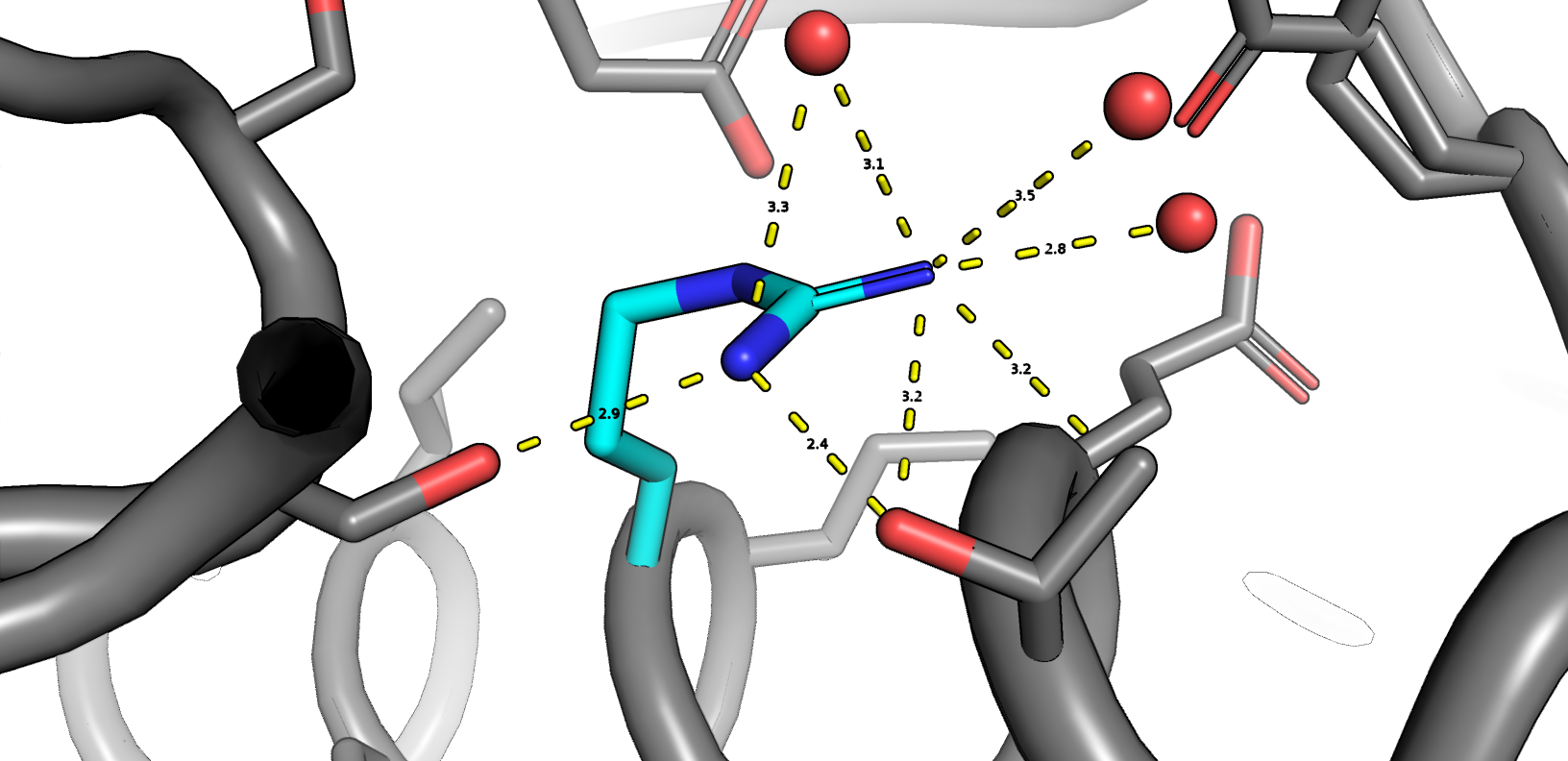
Можно видеть, что конформацию "A" стабилизируют два остатка аспартата, взаимодействуя с двумя различнвми азотами +
есть взаимодействие с 2 молекулами кристаллической воды. Конформацию "B" стабилизируют так же два остатка: серин и треонин
(у которого, у слову, тоже 2 альтлока, поэтому он может взаимодействовать с одним или двумя азотами аргинина); и 3 молекулы воды.
Какая из конформаций должная быть стабильней? Сложно сказать, наверное взаимоействия с водой не так важны для стабильности
в данном случае, как взаимодействия с остальными остатками (потому что не в кристалле вода — мобильная молекула), исходя из этого
я бы предположила, что более стабильная конформация "B". В ней потенциальные водородные связи короче.
Посмотрим теперь как это согласуется с электронной плотностью:
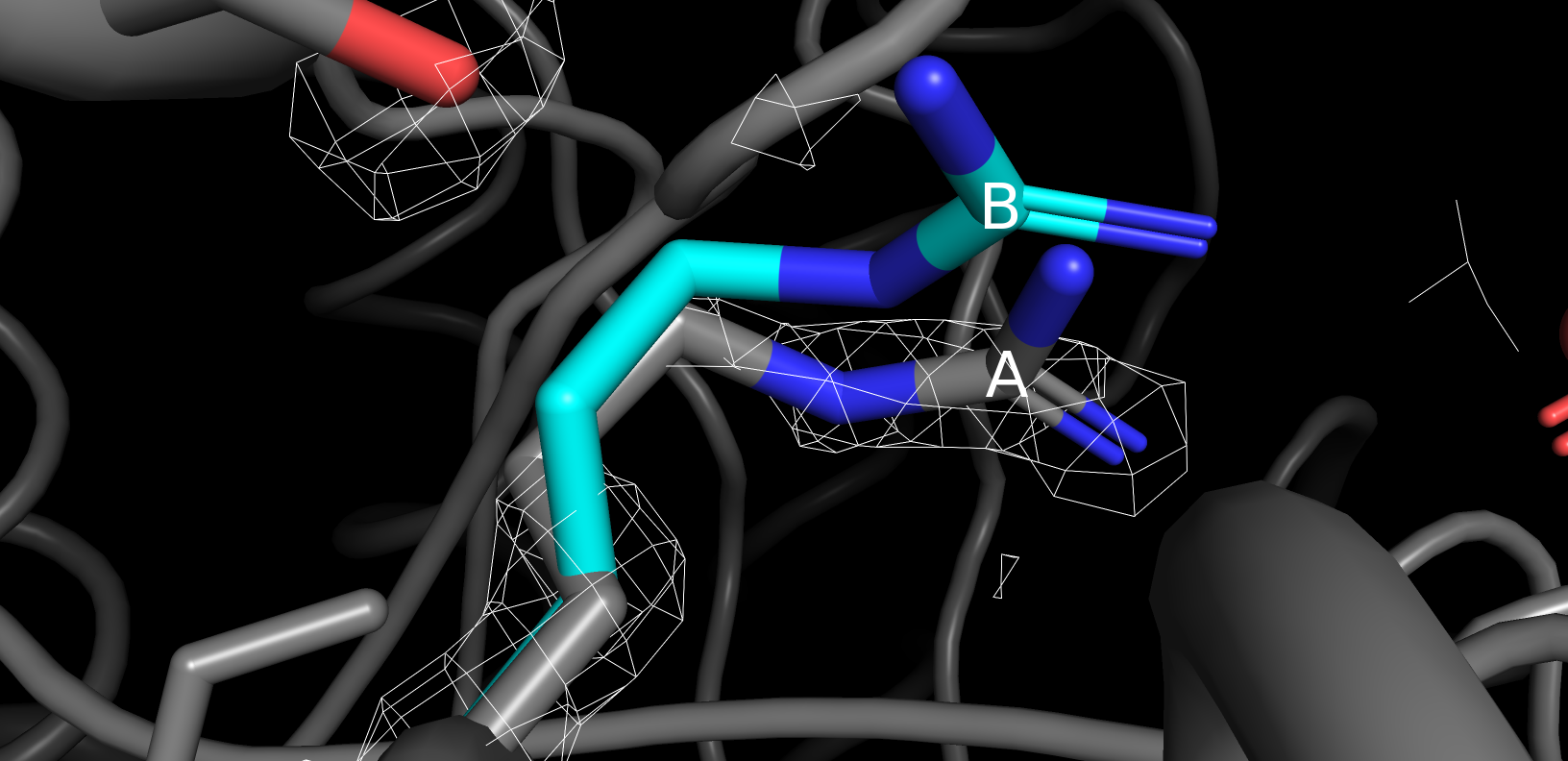
В результате, исходя из электронной плотности, стабильнее конформация "A". Возможно, это связано с тем, что треонин, стабилизирующий конформацию "B" сущестует в 2 конформациях, из-за чего на самом деле положение агинина менее стабильно (в конформации "B"). Кроме того, я еще подумала, что возможно имеет смысл какие атомы азота аргина участвуют в водородных связях.
Команды PyMol, которые я использовала в этом задание:
fetch 6FWJ
fetch 6FWJ type=2fofc
select my_residue_A, resi 136 and alt "A"
select my_residue_B, resi 136 and alt "B"
distance contacts, my_residue_A, all, 5, mode=2
distance contacts, my_residue_B, all, 5, mode=2
isomesh meh, 6FWJ_2fofc, 2, my_residue_B, carve=3
Задание 4: B-фактор
В данном задание надо было раскрасить белковый остов по величине B-фактора. Получившиеся изображения представлены на рис.8.
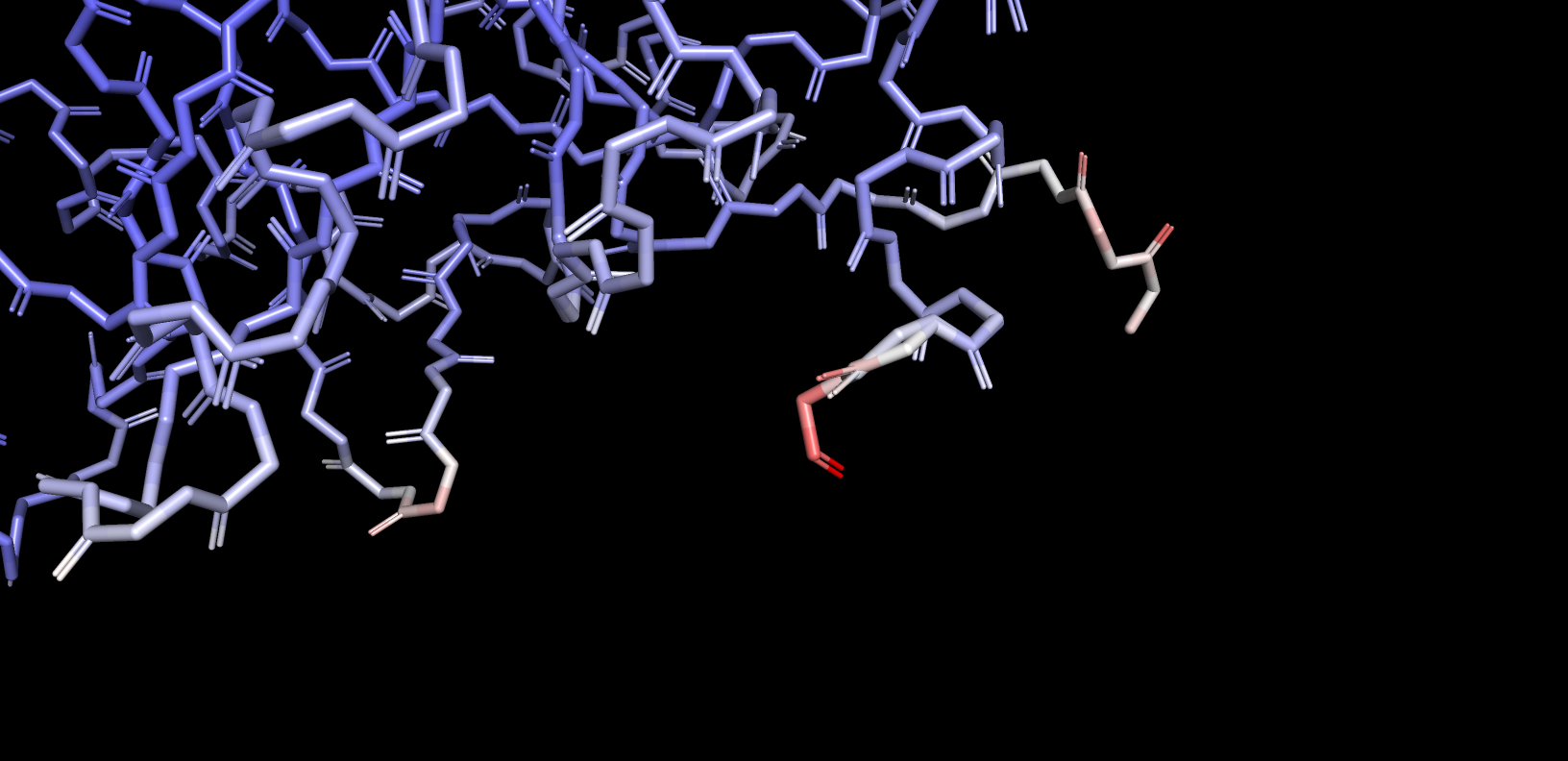
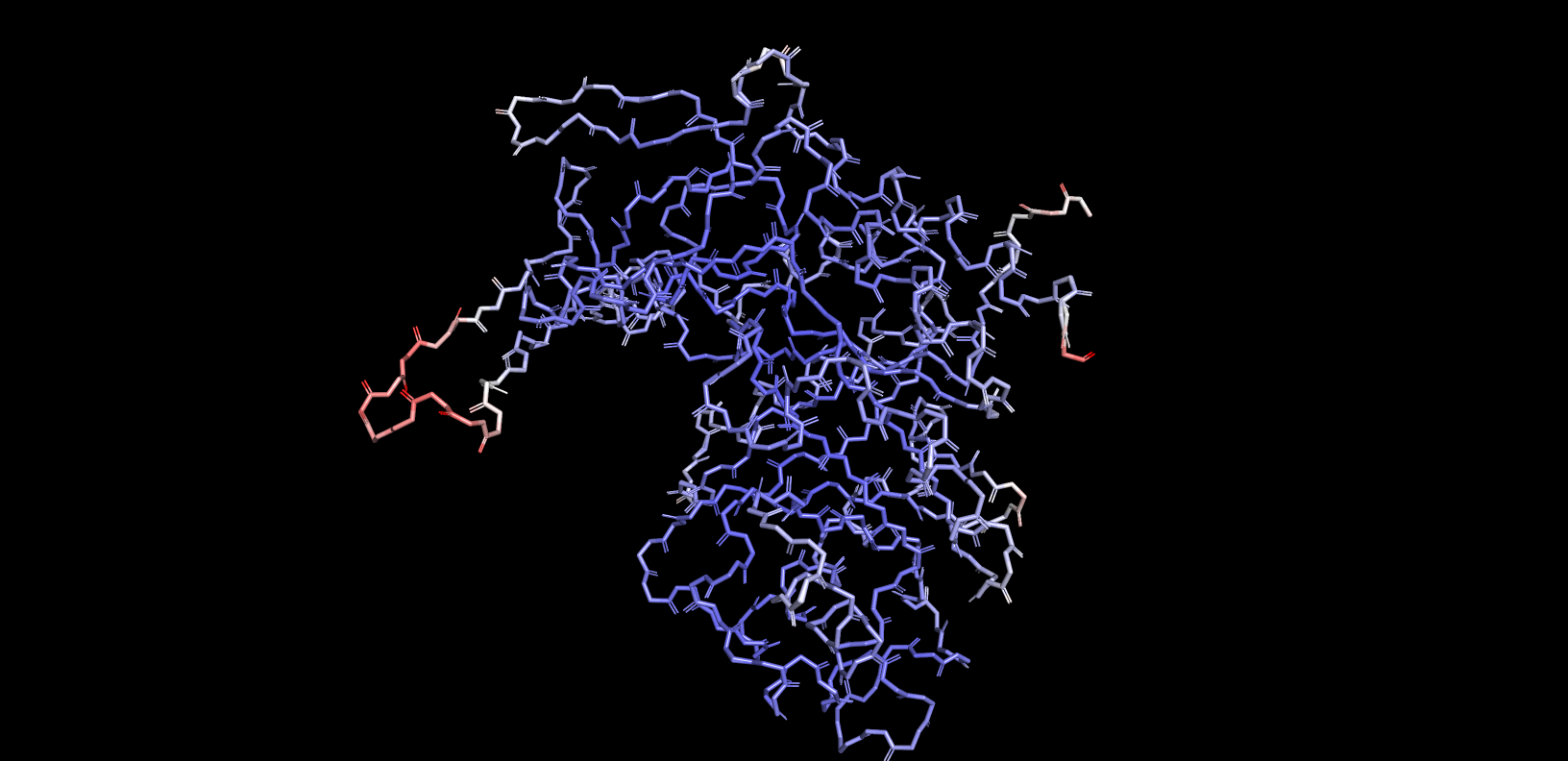
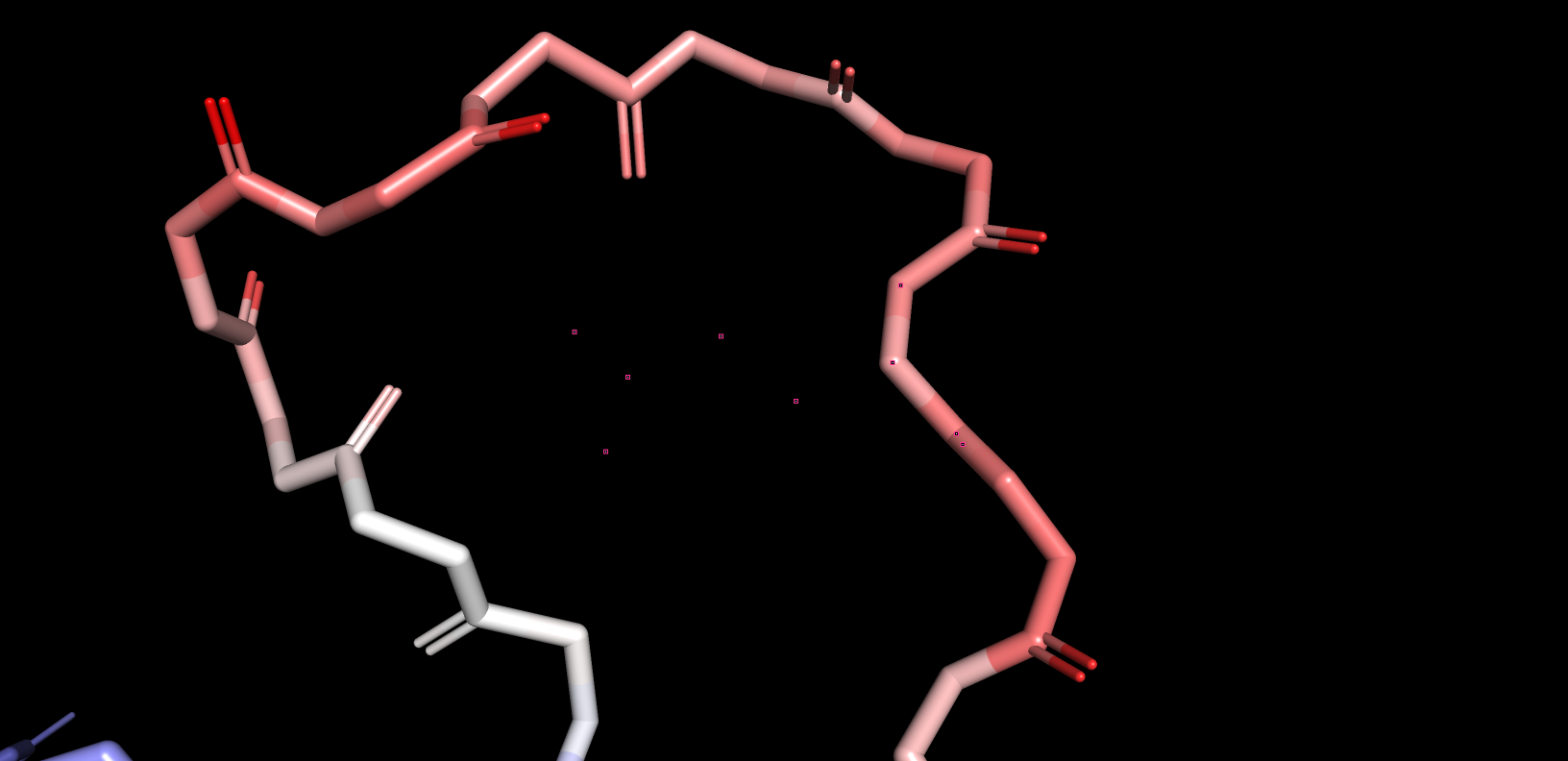
Участки с более высоким B-фактором окрашены в красный. Такие участки — петли и самый конец полипептидной цепи.
Можно предположить, что более высокому B-фактору соответствуют участки с более нестабильным положением. Такие участки
будут находится с большей вероятностью по краям глобулы, у них будет меньше контактов с осталной полипептидной цепью.
Рис. 8 в целом это отражает.
Далее на рис. 9 я отриовала аминокислотный остаток, у которого величина B-фактора увеличивалась к концу (то есть в
моем случае конец белел).
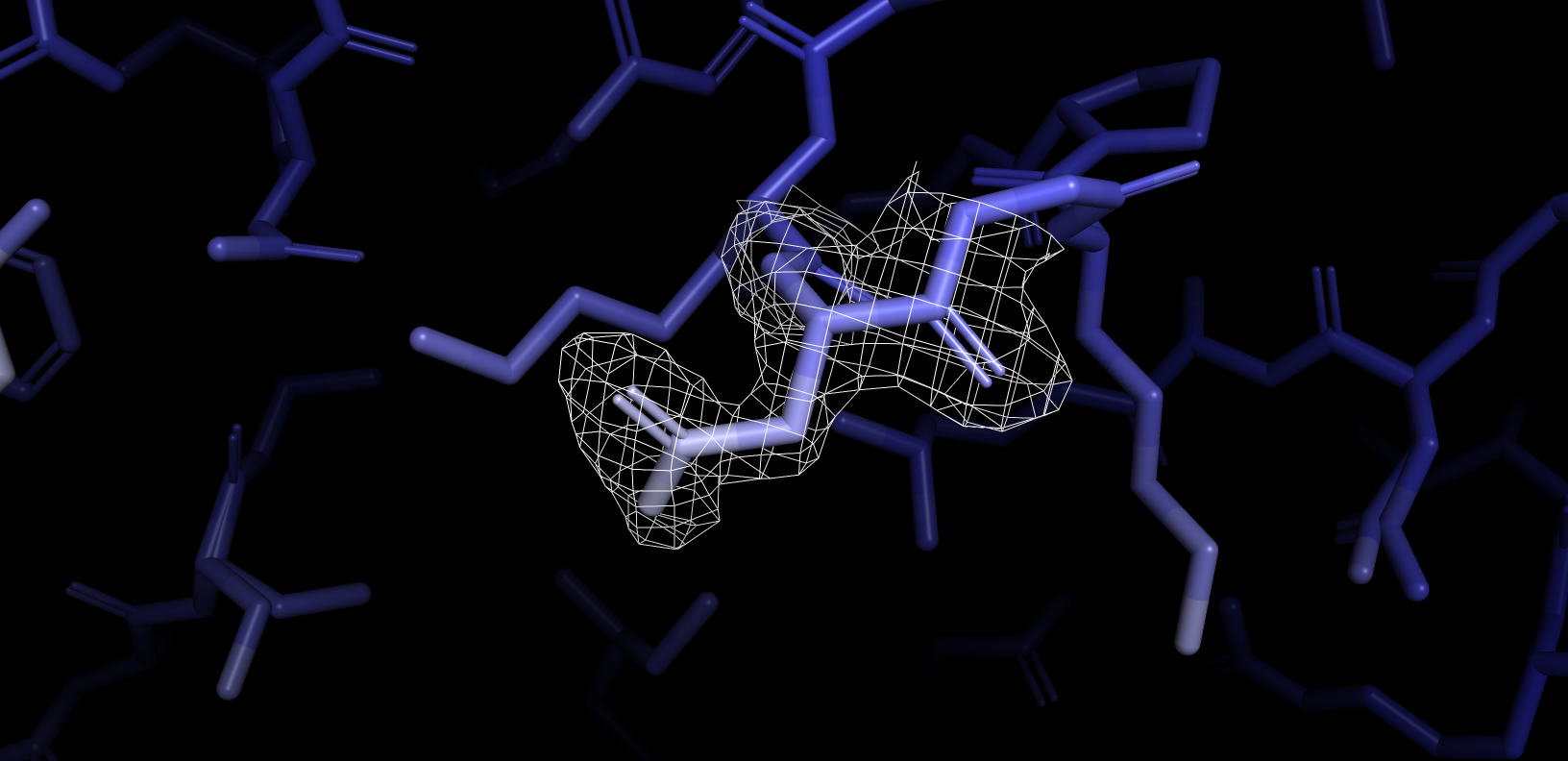
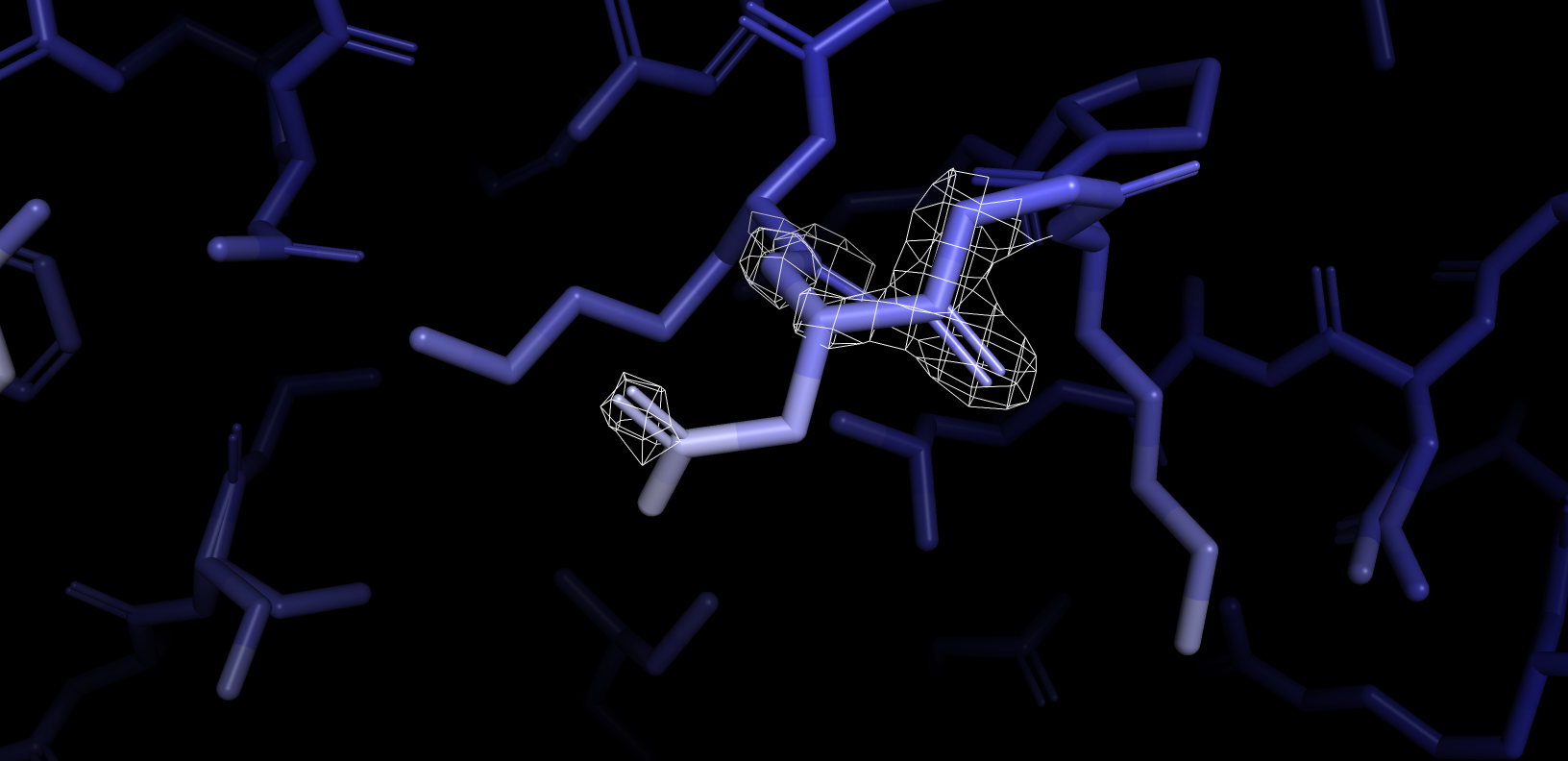
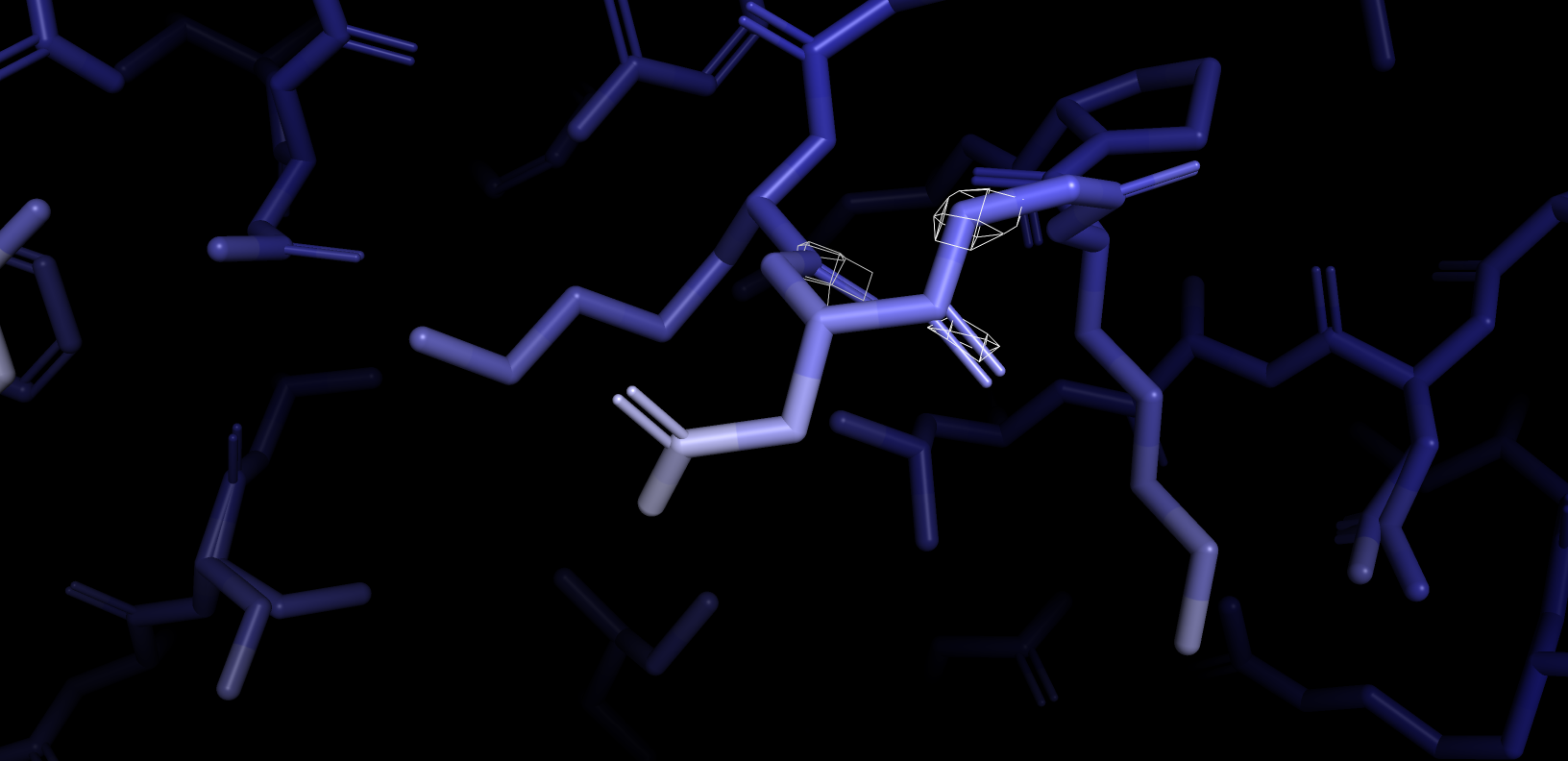
Можно видеть что при увеличение уровня подрезки электронная плотность перестает покрывать области с высоким B-фактором. Это означает, что низкие значения B-фактора отвечают высокой электронной плотности и наоборот.
Команды PyMol, которые я использовала в этом задание:
fetch 6FWJ
fetch 6FWJ type=2fofc
spectrum b, blue_white_red, backbone
spectrum b, blue_white_red
isomesh meh, 6FWJ_2fofc, {1-3]}, resi 187, carve=2
На страницу семестра
