Протонирование
Для данного практикума мне достался белок с PDB ID 1KVD ( KILLER TOXIN FROM HALOTOLERANT YEAST ), который был закристаллизован при pH = 3.5.
Протонирование при помощи PROPKA
Сначала я получила протонированную структуру при помощи сервиса PDB2PQR Установив желаемый pH равным 3.5 и остальные параметры по умолчанию. Вот такие предсказания pKa получились для аспартатов, глутаматов и гистидинов. Высокие pKa выделены жирным:
SUMMARY OF THIS PREDICTION
Group pKa model-pKa ligand atom-type
ASP 76 A 7.08 3.80
ASP 157 B 5.81 3.80
ASP 161 B 2.69 3.80
ASP 169 B 3.61 3.80
ASP 176 B 2.95 3.80
ASP 195 B 5.10 3.80
ASP 199 B 4.58 3.80
ASP 213 B 3.83 3.80
ASP 221 B 4.26 3.80
ASP 222 B 2.88 3.80
ASP 76 C 7.26 3.80
ASP 157 D 5.71 3.80
ASP 161 D 2.59 3.80
ASP 169 D 3.26 3.80
ASP 176 D 3.16 3.80
ASP 195 D 5.27 3.80
ASP 199 D 5.22 3.80
ASP 213 D 3.53 3.80
ASP 221 D 4.15 3.80
ASP 222 D 3.12 3.80
GLU 66 A 6.18 4.50
GLU 147 B 3.97 4.50
GLU 158 B 7.46 4.50
GLU 66 C 6.28 4.50
GLU 147 D 3.93 4.50
GLU 158 D 7.34 4.50
HIS 70 A 6.49 6.50
HIS 185 B 6.01 6.50
HIS 70 C 6.55 6.50
HIS 185 D 6.03 6.50
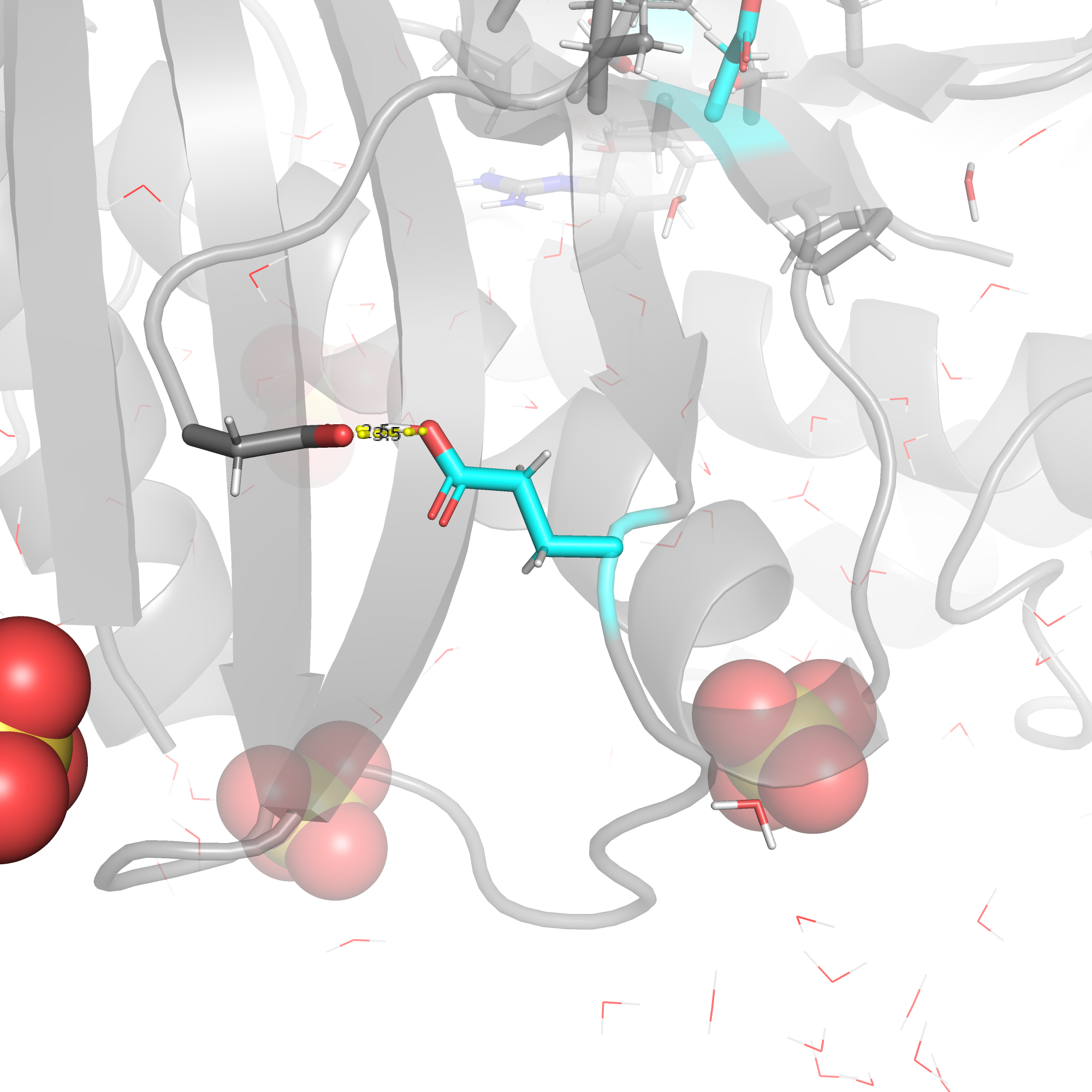
Рассмотрим как выглядят данные остатки. Начнем с 76 аспартата (рис. 1)
Рассматриваемый остаток выделен голубым.
Мы видим что данный аспартат протонирован по атому кислорода. У данного протона, как мне сначала показалось,
нет партнеров для образования водородной связи, однако почему тогда у этого остатка настолько высокий pKa? Подумав,
я визуализировала атомы остова и обнаружила, что технически расстояние позволяет образовывать водородные связи с ними(рис. 1 б)).
Образуются ли действительно водородные связи? Ближе всего (2.8 Å, что соответствует стандартной водородной связи)
находится атом азота, обычно выступающий в роли донора. Может ли он быть акцептором водородной связи, донируя
электронную пару? Вообще говоря нет, поскольку он навходится в sp2 гибридизации и все электроны задействованы
в образовании связей, свободных пар нет.
Что касается
атома кислорода, то расстояние до него чуть больше, чем стандартная водородная связь (2.8-3.0 Å ),
поэтому водородная связь будет слабая.
В общем, водород в принипе вписывается на слабую водородную связь с кислородом, геометрия такой связи адекватная.
Непротонированный атом кислорода образует LBHB связь с 213 аспартатом (длина между
гетероатомами — 2.5 Å).
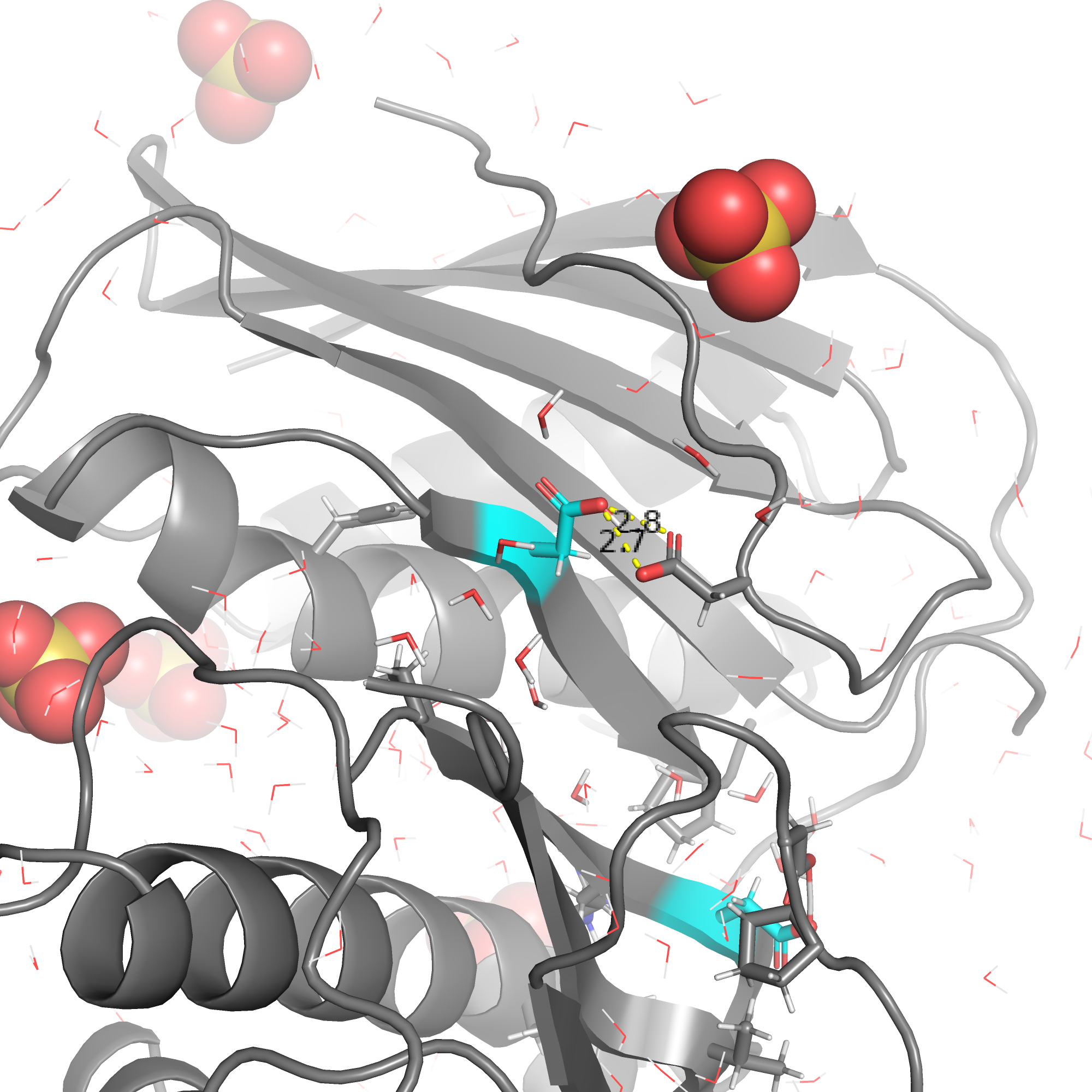
Далее рассмотрим 158 глутамат. Из рис. 2 видно, что он протонирован и протон имеет есколько возможностей для
образования водородной связи. В данной конформации наиболее выгодная свзь LBHB между кислородом рассматриваемого аспартата и
и кислородом 222 остатка аспартата. Положение протона предсказано неплохо,
то есть торчит на встречу к кислороду, а не куда-то еще.
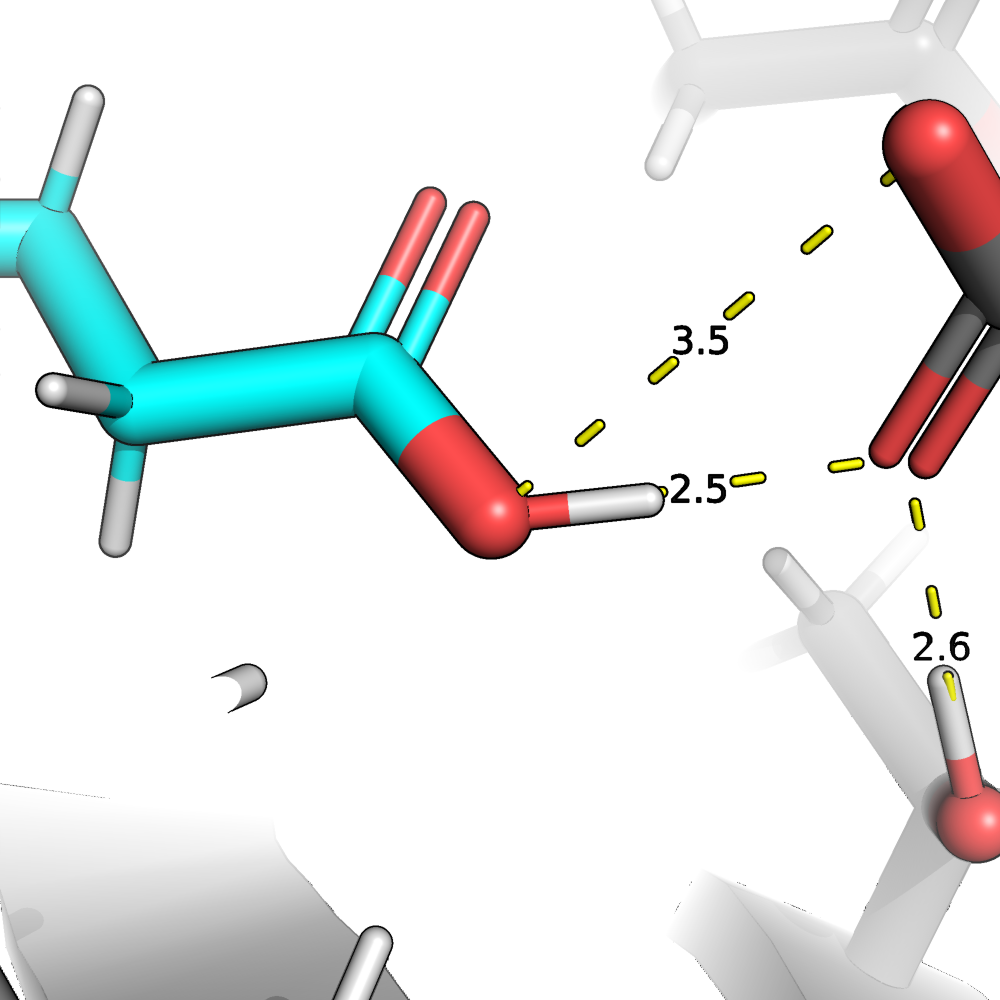
Конкретно в этих примерах протоны от PROPKA участвуют в водородных связях и имеют нужную геометрию. В случае аспартата связь слабая. То есть касаемо предсказания наличия протона и его расположения в целом нормально, хотя опять же связь с аспартатом не такая сильная.
Протонирование при помощи PROTOSS
Алгоритм добавления протонов PROTOSS игнорирует значния pKa остатков и протоны расставляет опираясь на окружение
, посмотрим какие результаты мы получим.
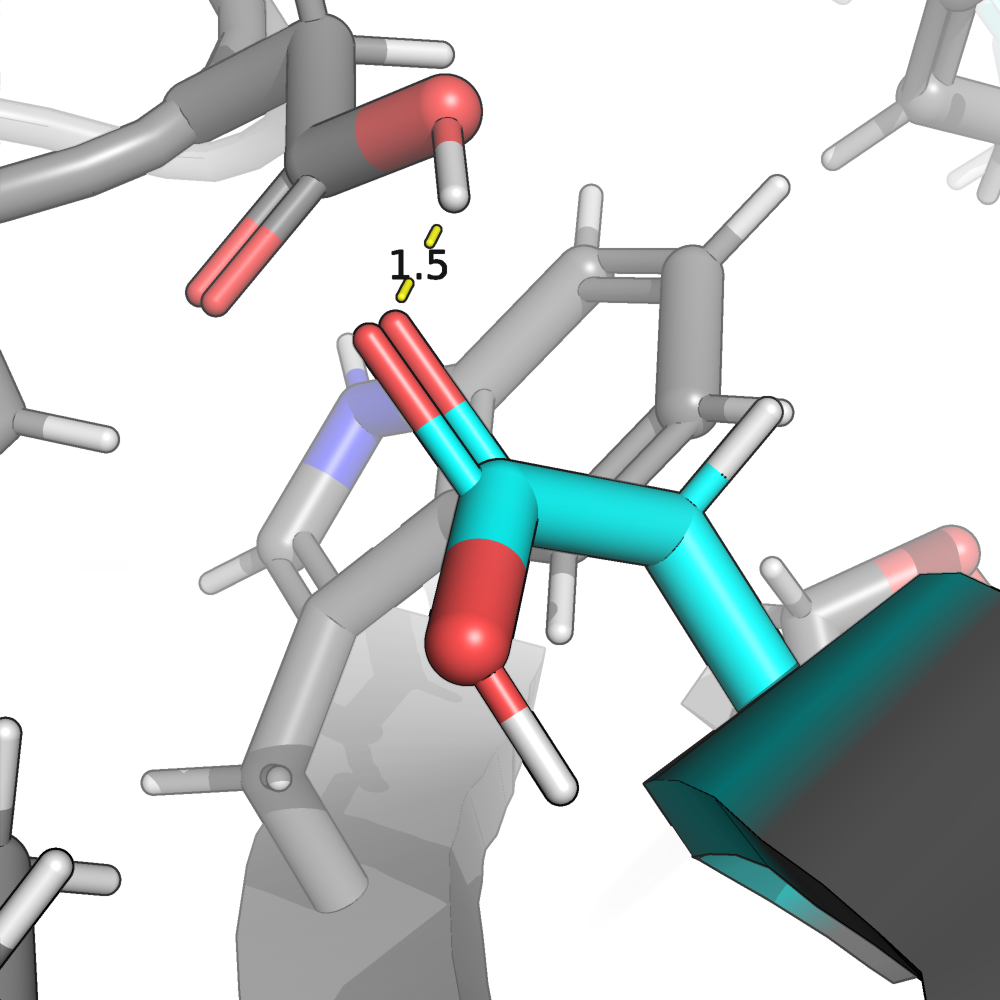
Итак начнем с 76 аспартата (см. рис. 3). Мы видим, что на этот раз протон ориентирован так, чтобы
формировать водородную связь с соседним аспартатом, а не остовом. Этот вариант более логичен, тк с остовом возможна только слабая связь. Получившаяся
геометрия водородной связи нормальная. Есть целых два равнозначных кислородных атома, которые могут быть акцепторами
водородной связи, может поэтому протон завис между этих двух возможностей? В любом случае угол водородной связи
в обоих случаях премлемый.
Поэтому 1/0 в пользу PROTOSS.
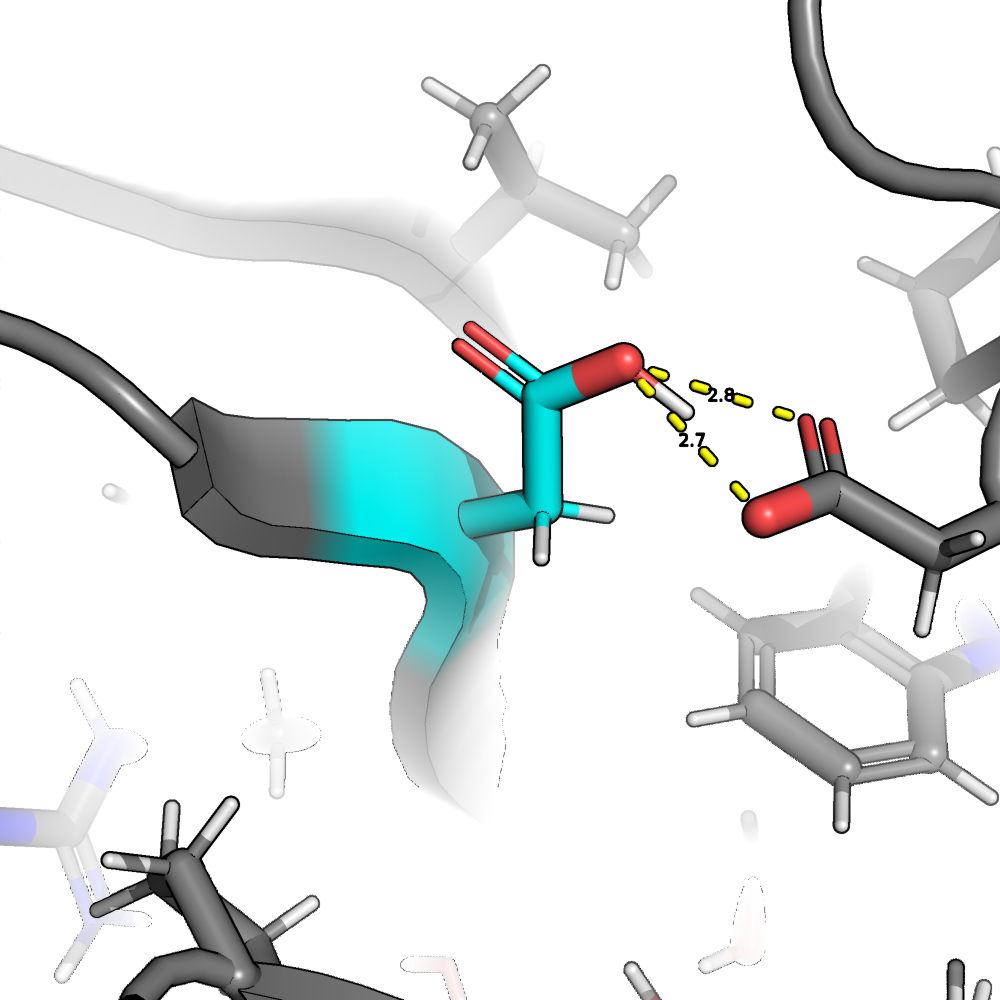
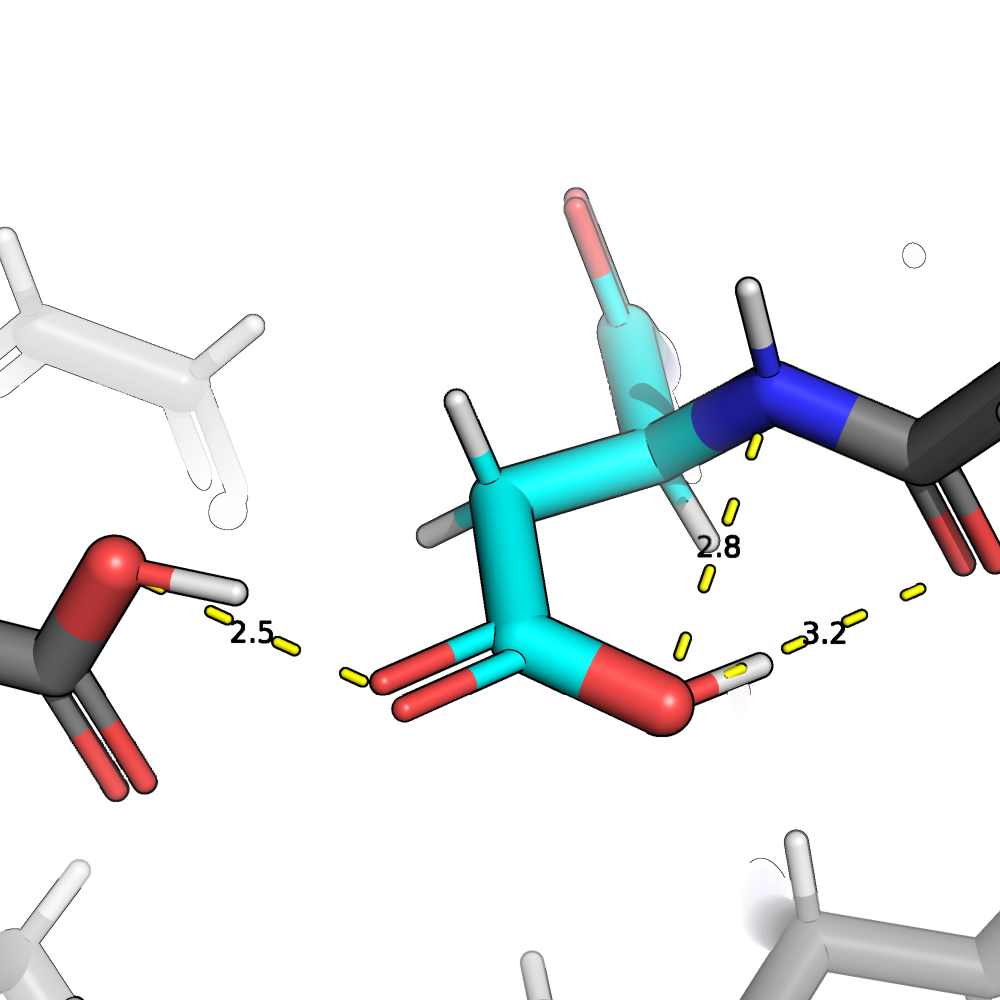
Далее рассмотрим остаток 158 глутамата (рис. 4). Здесь протонирование ничем не отлчается от PROPKA. 2/1 в пользу PROTOSS.
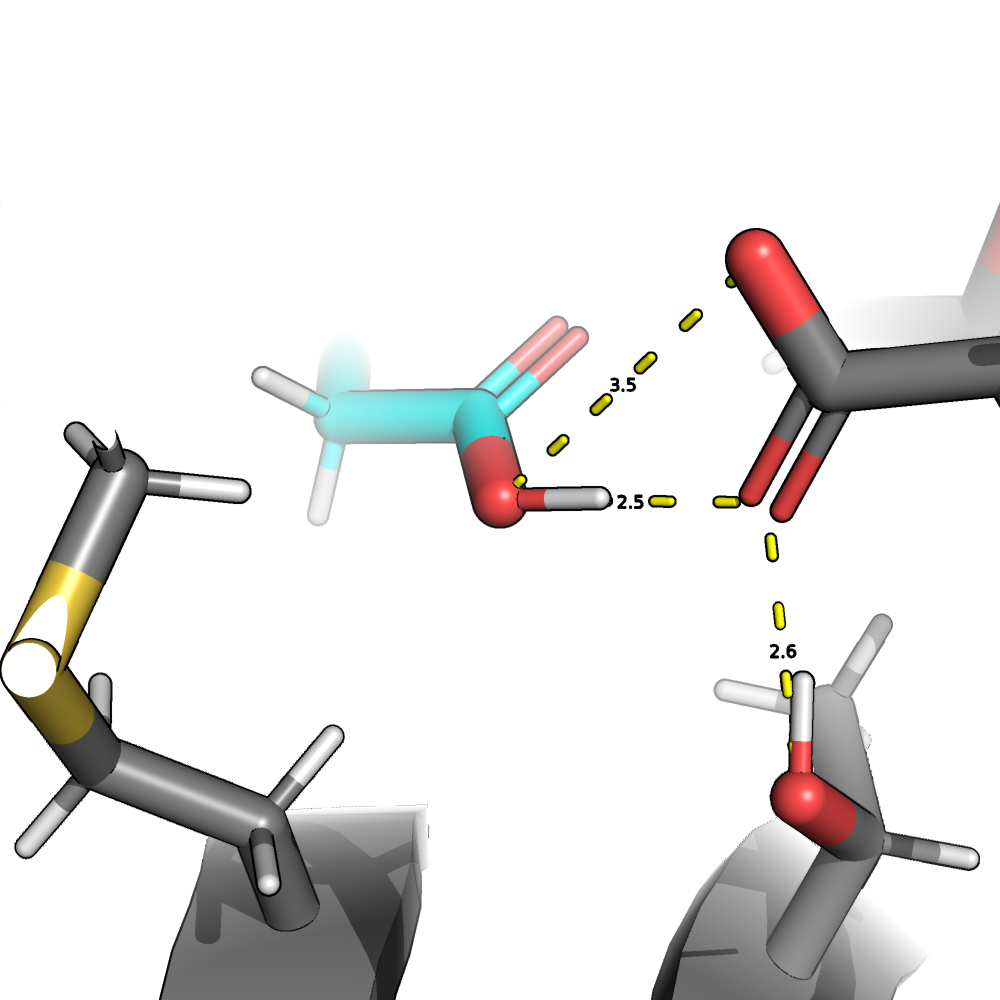
Выводы
С счетом 2/1 победа присуждается алгоритму PROTOSS. Протоны от PROTOSS наилучим образом вписываются в окружение.
Что будет, если среда станет щелочной? Протонирование пропадет, а вместе с ним водородные связи.
Пофантазируем, что будет, если протоны уйдут с рассматриваемых выше аминокислот.
Для этого взглянем на относительное положение остатков в структуре. На рис. 5 видно, что 158 глутамат
стабилизирует водородной связью конец белковой цепи (дополнительно его стабилирует еще один остаток, который не
показан на картинке). Остаток аспартата, как ни странно,
тоже стабиилизирует белковый "хвост", но на более раннем участке. Таким образом, можно предположить, что конец белковой цепи стал бы свободно болтаться.
Вообще, судя по предыдущему практикуму, поверхностные участки белковой цепи в целом более подвижны, что в целом не
удивительно, ведь они взаимодействуют (и как следствие стабилизируются) с остальными остатками только с одной стороны.
Поэтому я думаю, что стабилизировать конец цепи это довольно важно, иначе без этих связей он просто будет болтаться
и белок вероятно потеряет свои функции.