|
Home page Term 1 Term 2 Term 3 Term 4 About me Faculty website |
PyMOL Практикум 4Задание 1Для данного задания мне были даны структура РСА (PDB ID: 3E0H) с разрешением 1.81 ангстрем и структура ЯМР (PDB ID: 2KCU) с 20 моделями.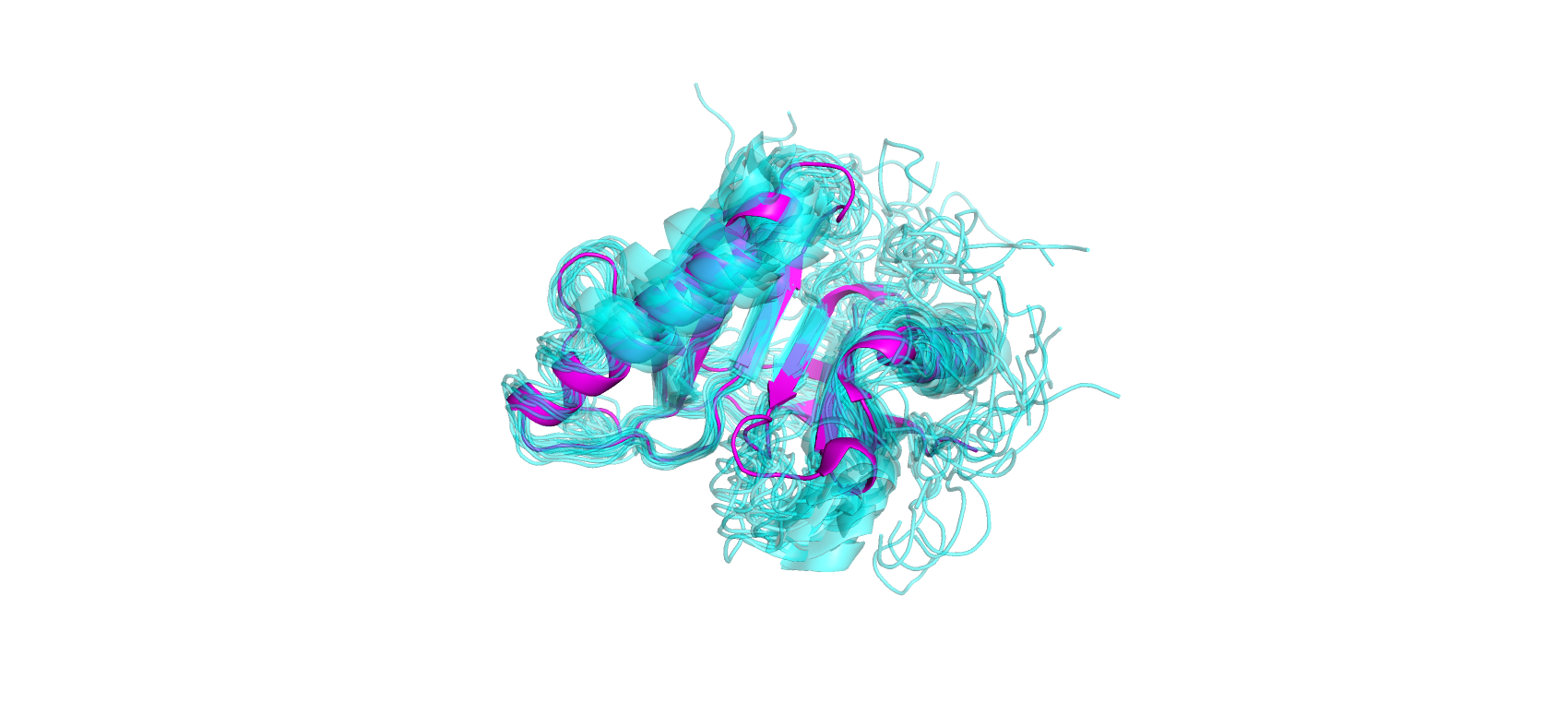 На макро-уровне сразу бросается в глаза, что конец цепи в моделях ЯМР (показаны синим) длиннее, чем в структуре РСА (фиолетовая). Это можно объяснить тем, что конец цепи при заморозке образца мог застыть в большом количестве конформаций, что привело к тому, что сигналы его атомов недостаточно усиливались кристаллической решеткой для того, чтобы быть увиденными. В ЯМР же такой проблемы нет, и мы видим эти концы целиком. Однако в структуре ЯМР, по какой-то причине, хуже сработала автоматическая аннотация, и альфа-спирали в аннотации получились короче, чем в РСА и чем они реально есть в структуре ЯМР. Между структурами РСА и ЯМР наименее похожи друг на друга концы цепей и петли, и наиболее похожи друг на друга бета-листы и альфа-спирали. На микро-уровне, в структуре ЯМР присутствуют атомы водорода, а в РСА структуре нет. Это связано с тем, что РСА позволяет засечь водороды только в случае субатомарного разрешения. В ЯМР атомы водорода всегда видны, так как это ЯМР-активные элементы. Задание 2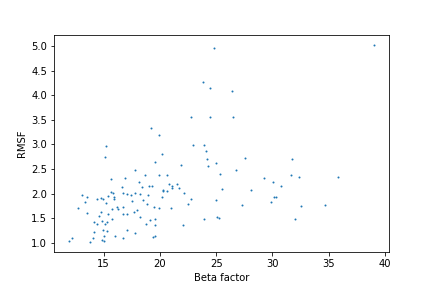 На данном графике видно, что имеется слабая линейная зависимость RMSF от В-фактора. Это значит, что ансамбль моделей в данной структуре ЯМР действительно можно очень грубо воспринимать как отражение подвижности белка. Задание 3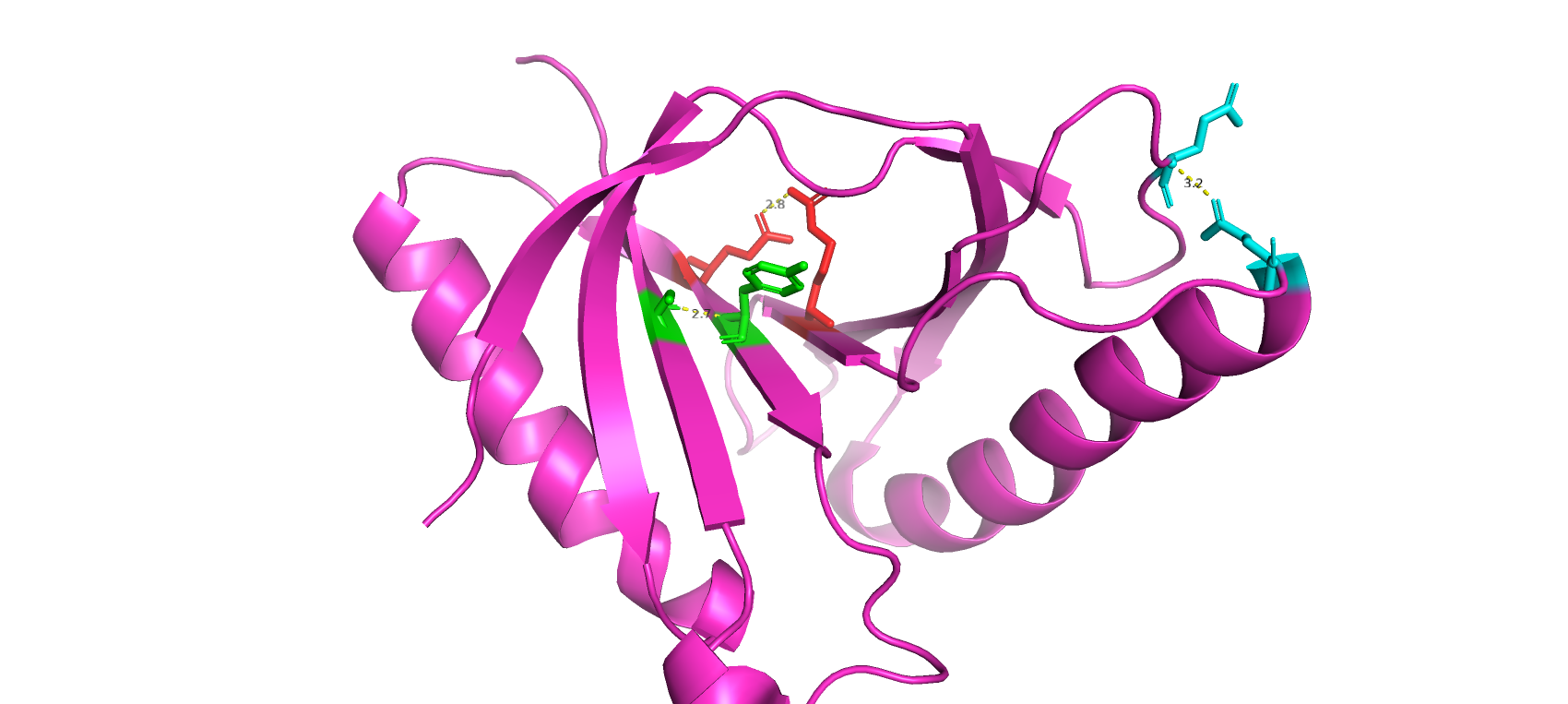 В качестве водородной связи между атомами остова в ядре белка я рассмотрел связь Tyr132-Ser152 (находится внутри бета-листа, отмечена зеленым), в качестве связи между боковыми цепями в ядре белка - связь Glu130-Arg60 (оба остатка входят в бета-лист, отмечены красным), а в качестве водородной связи в петлях - связь Glu82-Gln49 (оба остатка входят в петли, отмечены синим). Первые две пары остатков находятся внутри глобулы, а последняя пара - на поверхности. Нумерация связей в таблице соответствует порядку, в котором я перечислил их выше.
|
© Stanislav Tikhonov, 2020