Фрагмент пути для исследования: деградация триптофана до ацетилкофермента А
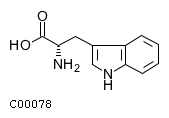
| L-Триптофан | Ацетилкофермент А |
| L-Tryptophan | Acetyl coenzyme A |
 |
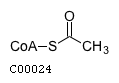 |
В KEGG БД метаболических путей (KEGG Pathways) искали метаболические пути включающие в себя оба заданных лиганда (триптофан и ацетилкофермент А). Была найдена только одна такая метаболическая карта "Метаболизм триптофана". Из этой карты вырезали кратчайший путь от триптофана к ацетилкоферменту А (такой путь на карте один). Файл запроса.
Красным цветом - заданные лиганды (триптофан, ацетилкофермент А); желтым цветом - все участвующие в пути ферменты.
- Описание выбранного пути
Общее число этапов на пути: 13
Возможный путь деградации триптофана до ацетил кофермента А ЭтапФерментативная реакцияФермент1 L-Tryptophan + Oxygen <=> L-Formylkynurenine 1.13.11.11 (1.13.11.52) 2 L-Formylkynurenine + H2O <=> Formate + L-Kynurenine 3.5.1.9 3 L-Kynurenine + Oxygen + NADPH + H+ <=> 3-Hydroxy-L-kynurenine + NADP+ + H2O 1.14.13.9 4 3-Hydroxy-L-kynurenine + H2O <=> 3-Hydroxyanthranilate + L-Alanine 3.7.1.3 5 3-Hydroxyanthranilate + Oxygen <=> 2-Amino-3-carboxymuconate semialdehyde 1.13.11.6 6 2-Amino-3-carboxymuconate semialdehyde <=> 2-Aminomuconate semialdehyde + CO2 4.1.1.45 7 2-Aminomuconate semialdehyde + NAD+ + H2O <=> 2-Aminomuconate + H+ + NADH 1.2.1.32 8 2-Oxoadipate + NH3 + NAD+ <=> 2-Aminomuconate + NADH + H+ + H2O 1.5.1.- 9 2-Oxoadipate + CoA + NAD+ <=> Glutaryl-CoA + CO2 + NADH + H+ 1.2.4.2 10 Glutaryl-CoA + Acceptor <=> Crotonoyl-CoA + Reduced acceptor + CO2 1.3.99.7 11 (S)-3-Hydroxybutanoyl-CoA <=> Crotonoyl-CoA + H2O 4.2.1.17 12 (S)-3-Hydroxybutanoyl-CoA + NAD+ <=> Acetoacetyl-CoA + NADH 1.1.1.35 13 2 Acetyl-CoA <=> CoA + Acetoacetyl-CoA 2.3.1.9 В данном метаболическом пути несколько примечательные фактов: во первых, все стрелочки расставлены куратором только в одном направлении (двухсторонних стрелочек нет). Во-вторых, первую реакцию данного пути катализирует два фермента. Фермент 1.13.11.11 (триптофан 2,3 диоксигеназа) проявляет специфичность к триптофану, но гораздо более активен в реакциях с L-триптофаном, в то время как 1.13.11.52 (индолемин 2,3 диоксигеназа) более активен к D-триптофану. Первые фермент проявляет большую субстрат специфичность.
Данные метаболический путь представляет собой цепочку реакций. - Возможность выбранной цепочки реакций у конкретных организмов
ОрганизмВозможно ли деградация триптофана до ацетилкофермента А по данным KEGG ? (Да/нет)Краткое обоснование
Homo sapiens Нет В KEGG отсутствуют гены ферментов катализирующиу 7 и 8 стадии, соответственно 1.2.1.32 и 1.5.1.- Escherichia coli K12 MG1655 Нет Из 13 необходимых ферментов, для 9 гены в KEGG отсутствуют Pseudomonas aeruginosa PAO1 Нет Из 13 необходимых ферментов, для 7 гены в KEGG отсутствуют Methanococcus janaschii Нет В KEGG нет ни одного гена для 13 необходимых ферментов Просмотрев наличие ферментов данного пути у разных организмов, не удалось обнаружить ни один организм, у которого бы по данным KEGG присутствовали гены всех 13 ферментов. Тем не менее, этот факт не отрицает возможности протекания деградации триптофана до ацетилкофермента А именно по этому метаболическому пути, а говорит лишь о том, что в KEGG нет данных о наличии в геномах просмотренных организмов генов таких ферментов.