
|
|
|
|
Занятие 6. Мембранные белки. Задание 1. Анализ множественного выравнивания трансмембранных белков В данном задании нам требовалось проверить сервис TMHMM - насколько правильно он предсказывает трансмембранные спирали в белке, а также проверить консервативность различных частей трансмембранных белков. Мне была выдана B-цепь белка-антипортера NhaP Na+/H+, основной функцией которого является поддержание pH и концентрации ионов натрия внутри клетки. Для начала необходимо было составить репрезентативную выборку гомологов этого белка. Я использовала инструмент BLAST на сайте EMBL EBI. Поиск проводился по базе UniProt Clusters на уровне идентичности 50%, было получено 200 гомологов, e-value худшей находки был 2.1E-21. Программой muscle было создано множественное выравнивание находок. Из выравнивания были удалены следующие последовательности: T1A069, UPI000695CEE8, T0DZG6, UPI00040374CA, UPI000686D53D, UPI000684ACF8 (слишком короткие, плохо выровнялись), G7XSI3, A0A017S9X5, T0CZV1, Q0EW88, A0A081FUT9, D0MEA4(просто плохо выровнялись). Файл с итоговым выравниванием. В программе Jalview к последовательности белка в выравнивании была прикреплена 3D структура и вручную отмечены мембранные участки в строке аннотации TM_REAL: Проект JalView Я дополнительно сверилась с координатами спиралей по базе OPM. Далее было получено предсказание трансмембранных спиралей программой TMHMM для гомолога A0A0M9UCS7_9CHLR. 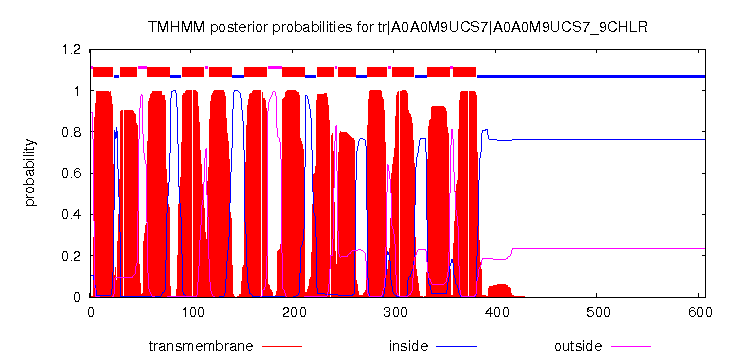
TMHMM выдала 13 спиралей, которые совпали с реальной структурой. Эти участки отмечены в JalView-проекте в строке TM_PREDICTED. Хотя некоторые предсказанные спирали отличались по длине от реальных, количество трансмембранных участков оказалось одинаковым, и границы были предсказаны более-менее верно. Предсказание может отличаться от реальной структуры потому что выполнялось для гомолога, а не для исходного белка. На рисунках 3 и 4 представлен мой трансмембранный белок с раскраской по гидрофобности аминокислот(Hydrophobicity: гидрофобные остатки выделены красным цветом) без порога идентичности и с порогом идентичности 5% соответственно. 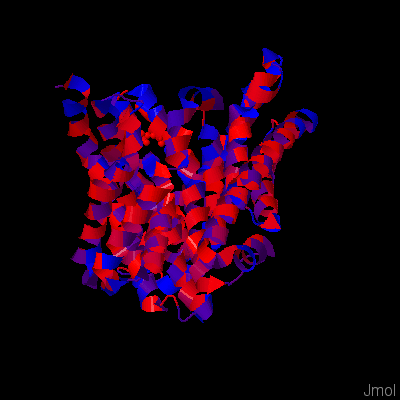
Рис.2 Структура мембранного белка с раскраской по гидрофобности аминокислот. P-сторона мембраны должна находиться снизу. Порога идентичности нет, гидрофобные остатки отмечены красным, гидрофильные - синим. 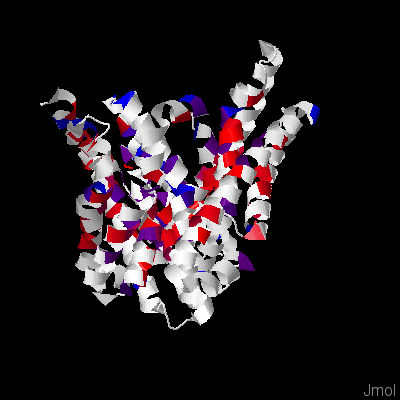
Рис.3 Структура мембранного белка с раскраской по гидрофобности аминокислот с порогом идентичности 5%. Гидрофобные остатки отмечены красным, гидрофильные - синим. В трансмембранных спиралях консервативны отдельные аминокислоты, большинство из которых гидрофобные. В принципе, можно сказать, что трансмембранные участки более консервативны, чем внемембранные. Однако порог идентичности очень низкий и, глядя на изображение белка, можно подумать, что консервативные аминокислоты распределены случайно по всему белку, а внемембранные его части просто сильно короче трансмембранных, поэтому вероятностно там консервативных аминокислот меньше. В трансмембранных участках попались и гидрофильные консервативные аминокислоты, которые, возможно, необходимы для работы фермента. |
|
© Шугаева Т.Е. 2016