
|
|
|
Построение и визуализация электронной плотности в PyMolДля выполнения этого и последующих практикумов я выбрала родопсин кальмара(рисунок 1). PDB-код выбранной cтруктуры - 2Z73 ( база PDB, база PDBe). Статья 'Crystal structure of squid rhodopsin', посвященная данной структуре, была опубликована в Nature в 2008 году (ссылка, для скачивания необходима оплата или Sci-Hub). 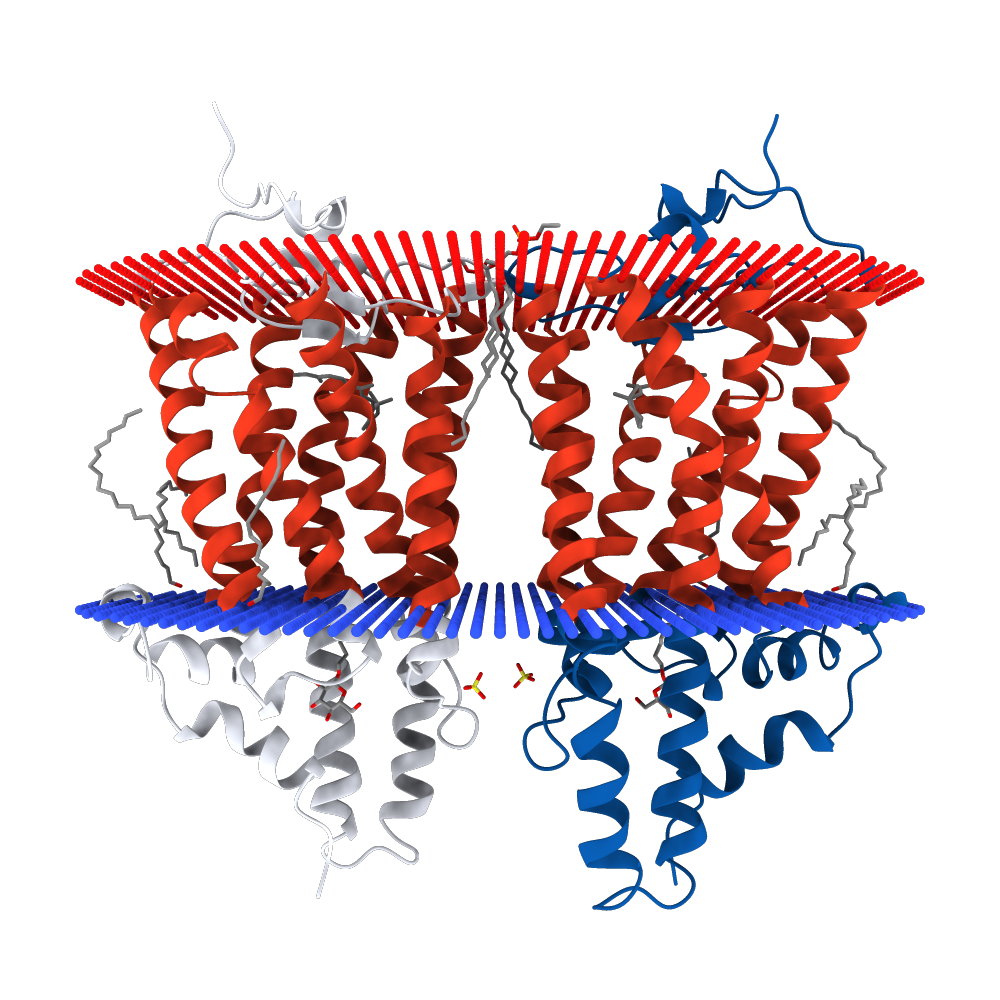
Рисунок 1. Crystal structure of squid rhodopsin. Разрешение структуры - 2,5Å 1. Изображение электронной плотности вокруг полипептидной цепи В программе PyMol (Free educational version) были открыты файлы 2z73.map.ccp4 и 2z73.pdb (в название файла с электронной плотностью пришлось добавить "map.", потому что иначе возникала накладка слоев, и электронная плотность не визуализировалась). Рисунки 2 и 3 были получены после применения скрипта, вращения и приближения камеры. Для лучшей визуализации представлена только цепь А, хотя в PDB файле записаны 2 симметричных молекулы белка (цепи А и B). 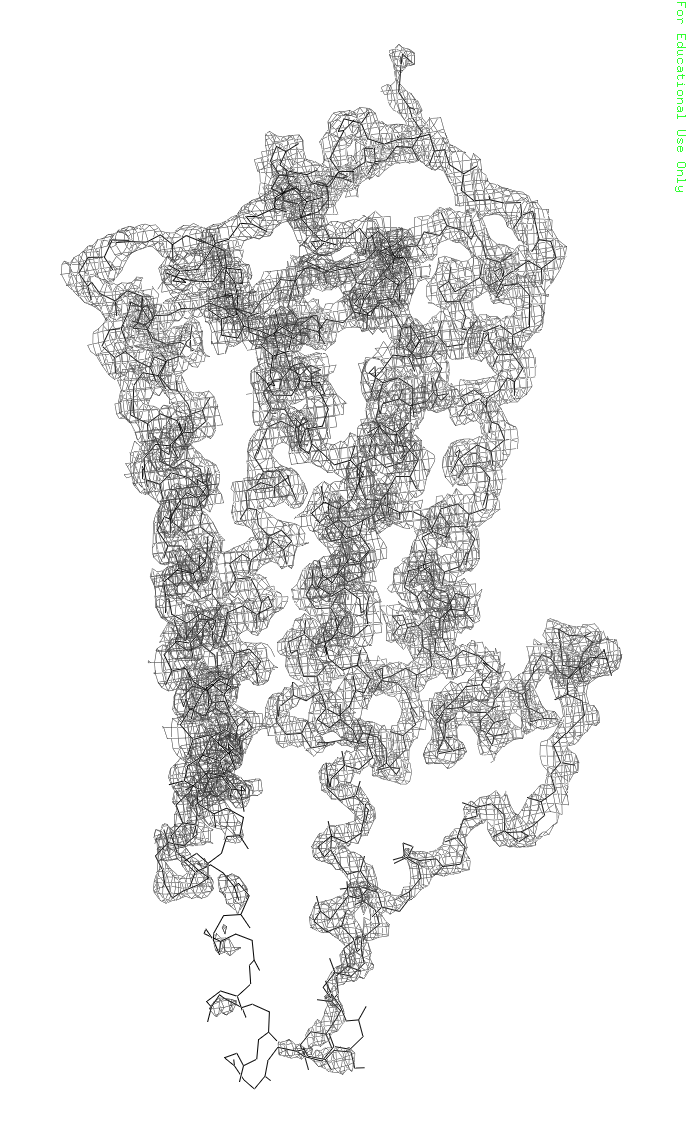 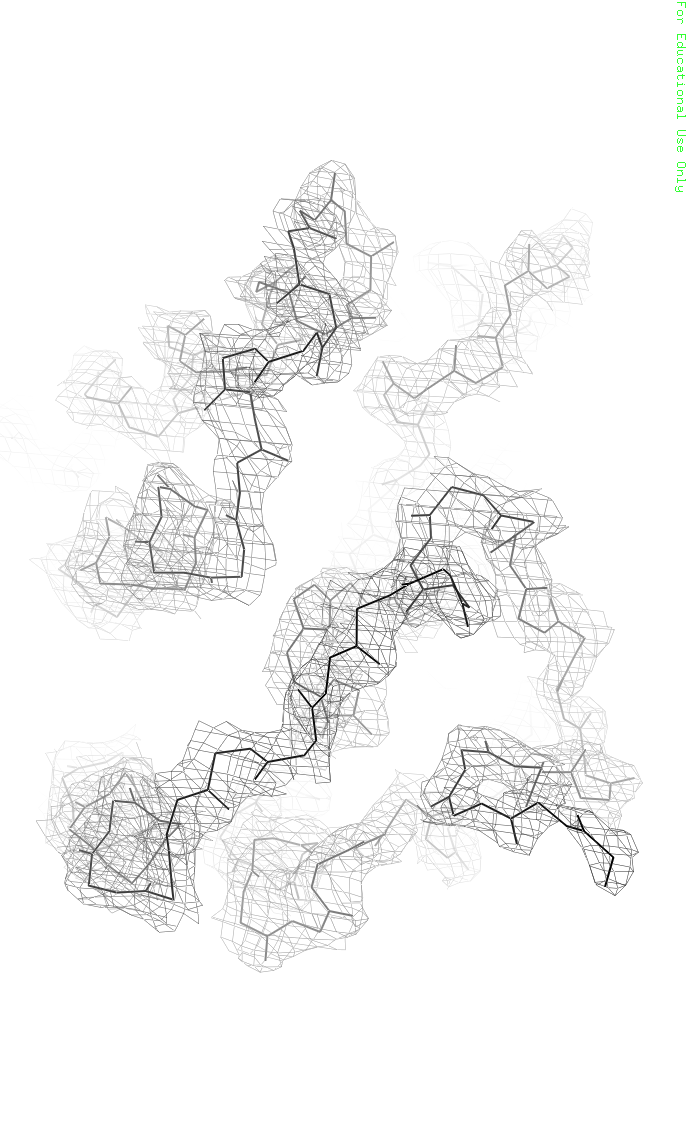
Рисунок 2(слева). Остов цепи А, level=2.0, carve=1.6, вид сбоку. Рисунок 3(справа).остов цепи А, level=2.0, carve=1.6, вид сверху, большее приблежение. 2. Изображение электронной плотности вокруг трех различных аминокислотных осатков 1) Триптофан 332, цепь А (скрипт) 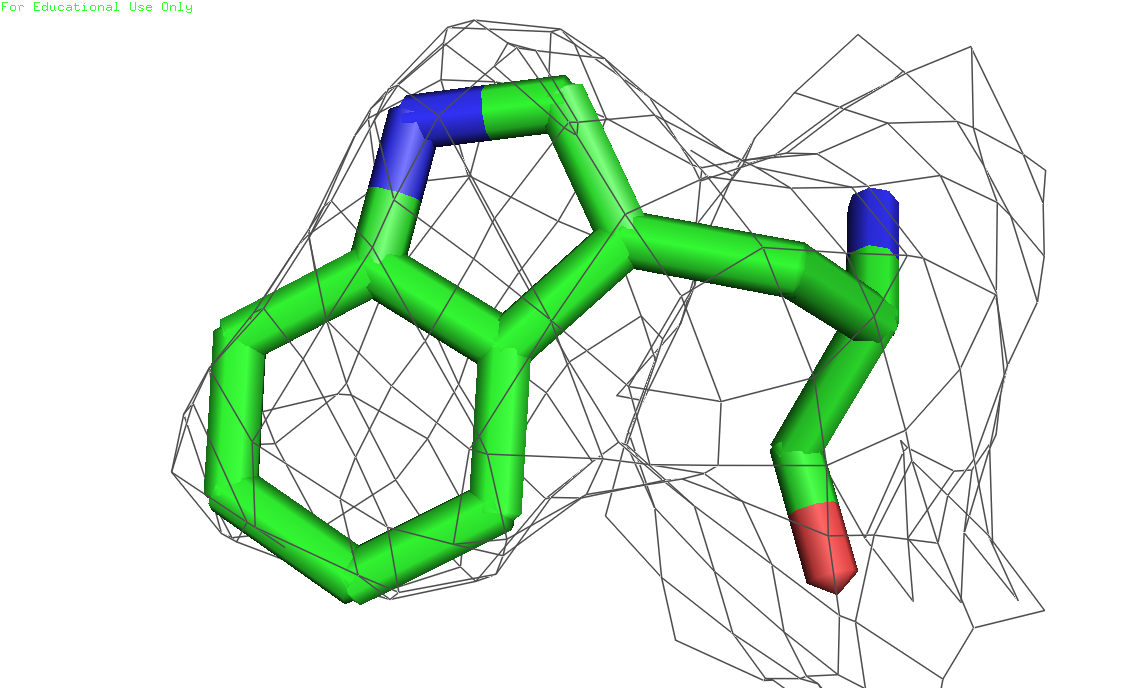 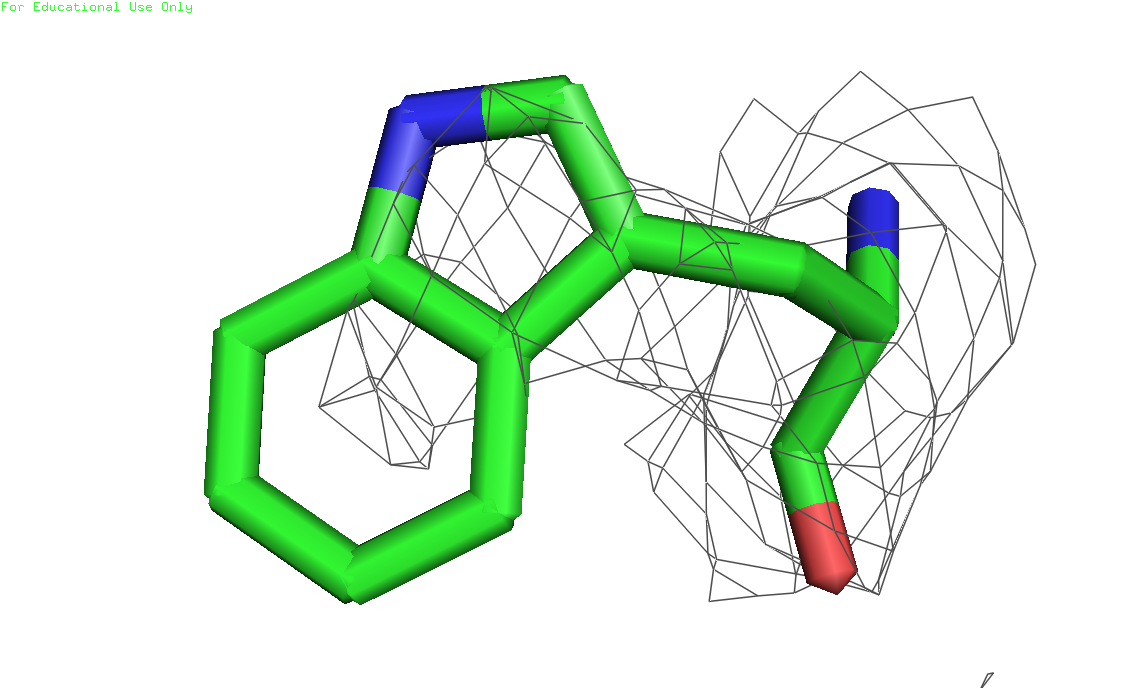 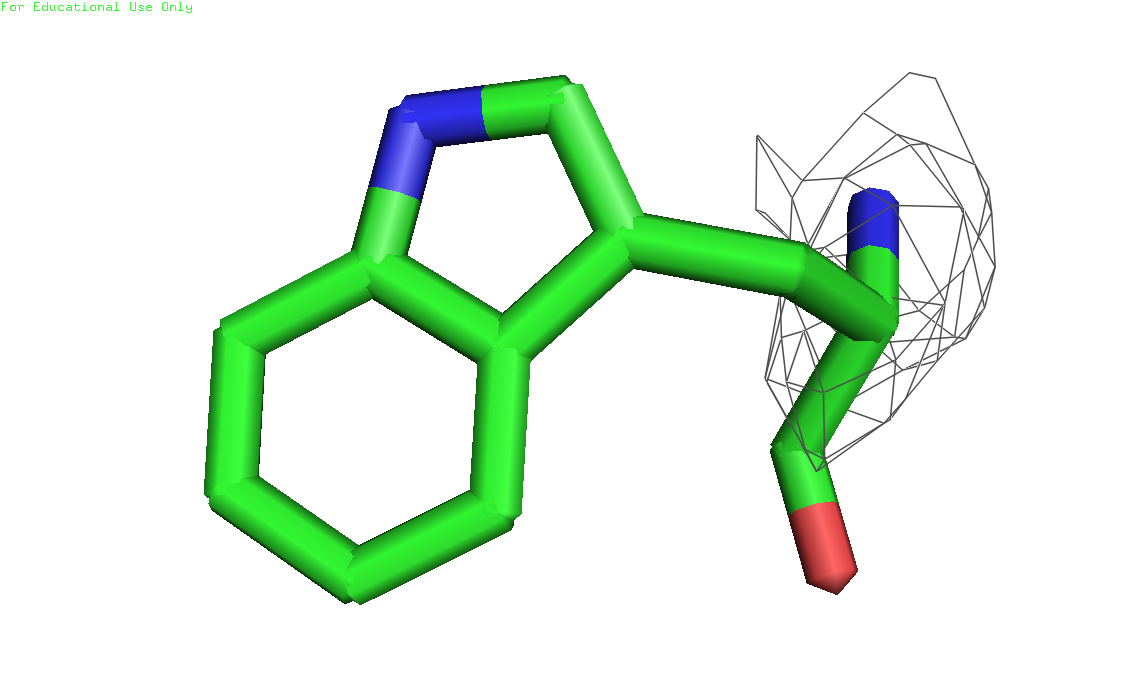
Рисунки 4, 5 и 6. Изображение триптофана 232, уровни подрезки слева направо соответственно: 1, 2 и 3. Электронная плотность показана на расстоянии 2 ангстрем от остатка (carve=2.0) 2) Глутамат 9, цепь А (скрипт) 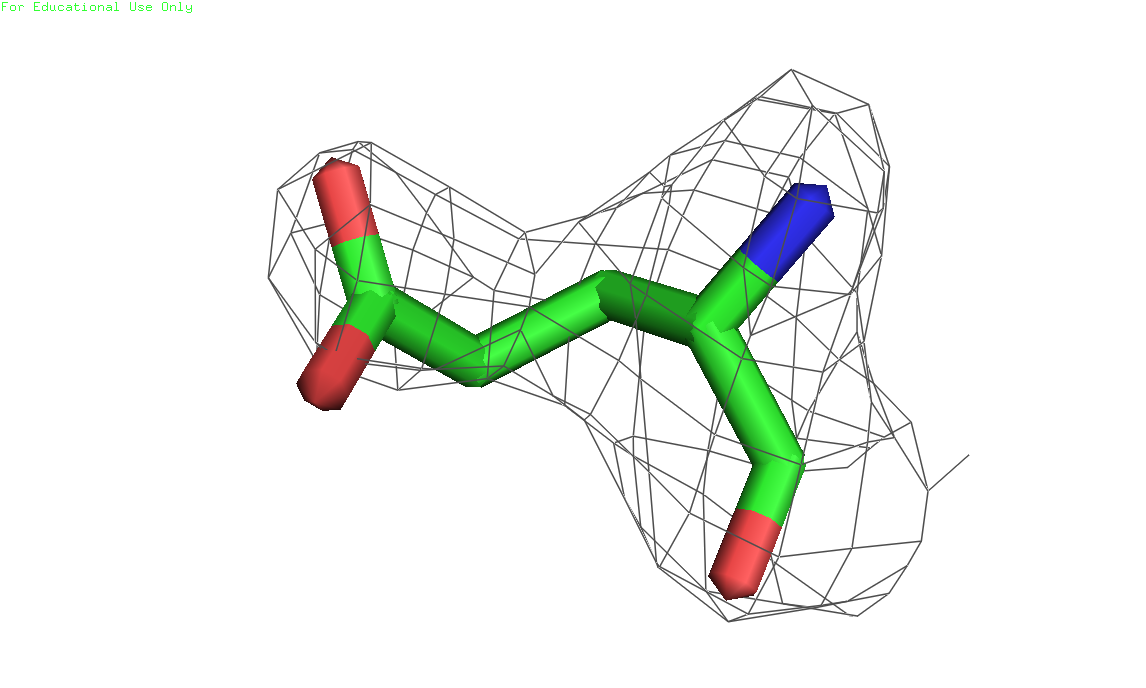 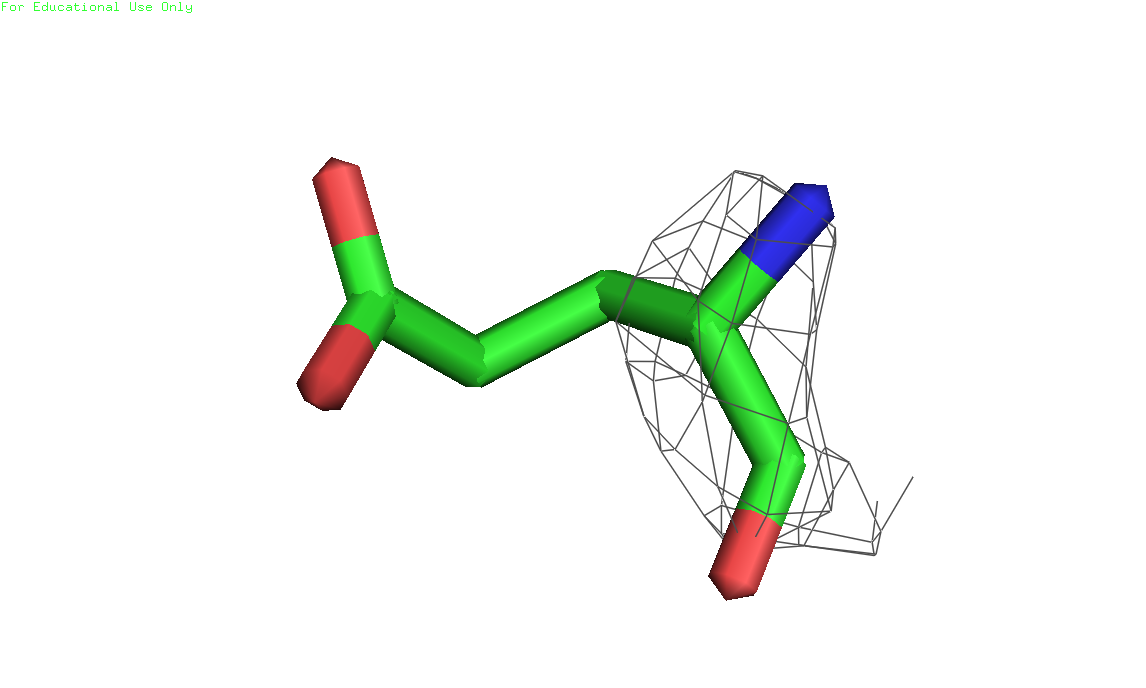 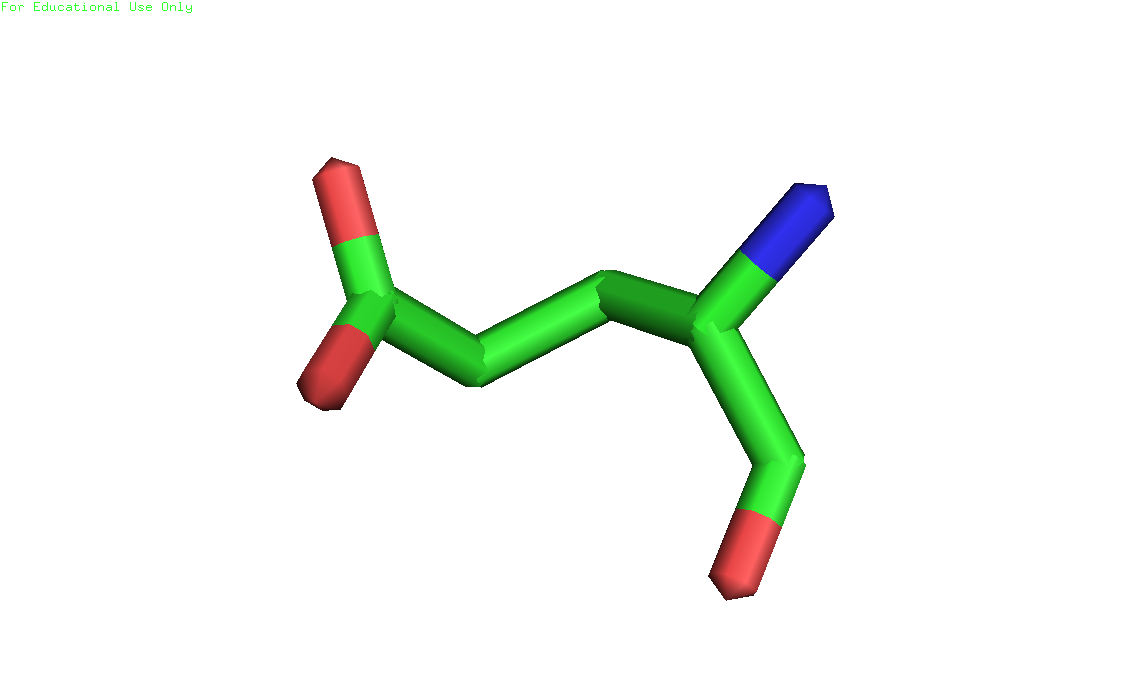
Рисунки 7, 8 и 9. Изображение глутамата 9, уровни подрезки слева направо соответственно: 1, 2 и 3. Электронная плотность показана на расстоянии 2 ангстрем от остатка (carve=2.0) 3) Аланин 236, цепь А (скрипт) 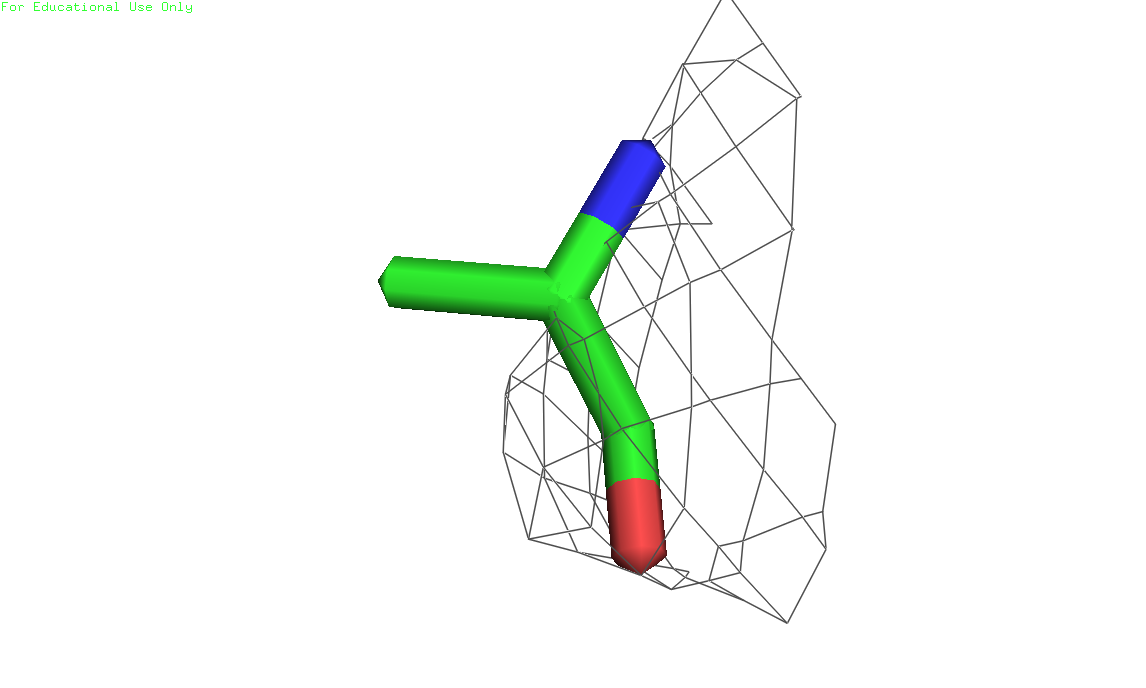 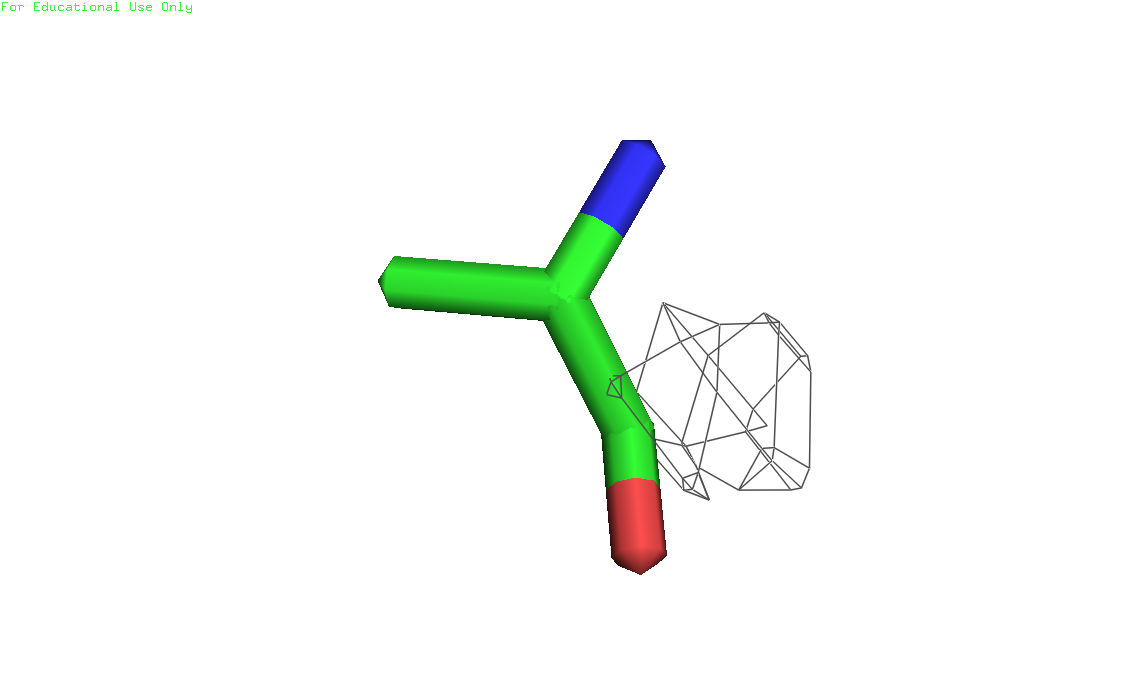 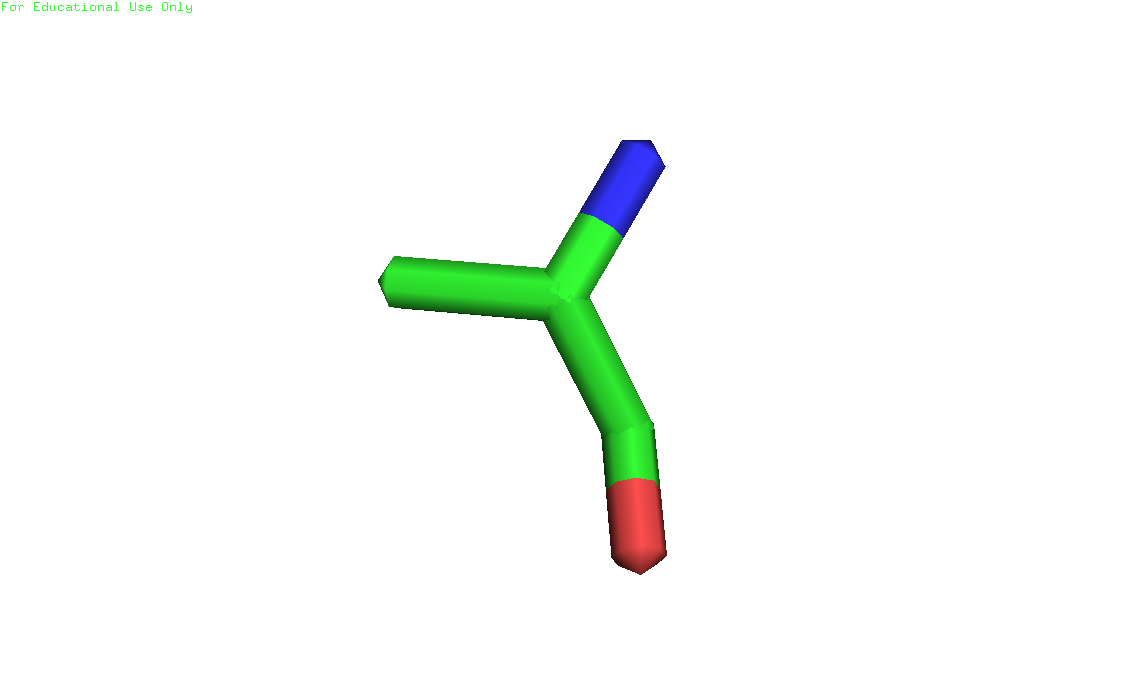
Рисунки 10, 11 и 12. Изображение аланина 236, уровни подрезки слева направо соответственно: 1, 2 и 3. Электронная плотность показана на расстоянии 2 ангстрем от остатка (carve=2.0) Расположение остатков в белке показано на рисунке 13. Все они находятся на относительной периферии белка. По рисункам 4-12 видно, что триптофан лучше всего вписывается в экспериментальную электронную плотность, уже при уровне подрезки 2.0 по электронной плотности можно угадать наличие довольно крупной боковой группы, а при уровне подрезки 3.0 видна часть остова. У двух других остатков вообще нет электронной плотности при уровне подрезки 3.0, но при дальнейшем уменьшении уровня глутамат неплохо вписывается. У аланина электронной плотности вокруг боковой группы не наблюдается даже при дальнейшем снижении уровня подрезки. Подобную разницу можно объяснить тем, что триптофан - это очень редкая и "дорогая" аминокислота. Скорее всего в данном белке структрура всей центральной части фиксирована и важна для выполнения функции (передачи возбуждения внутрь клетки), поэтому и триптофан определяется четко. А вот аланин располагается в периферической петле, вероятно, довольно подвижной, поэтому сигнал от него слабее. 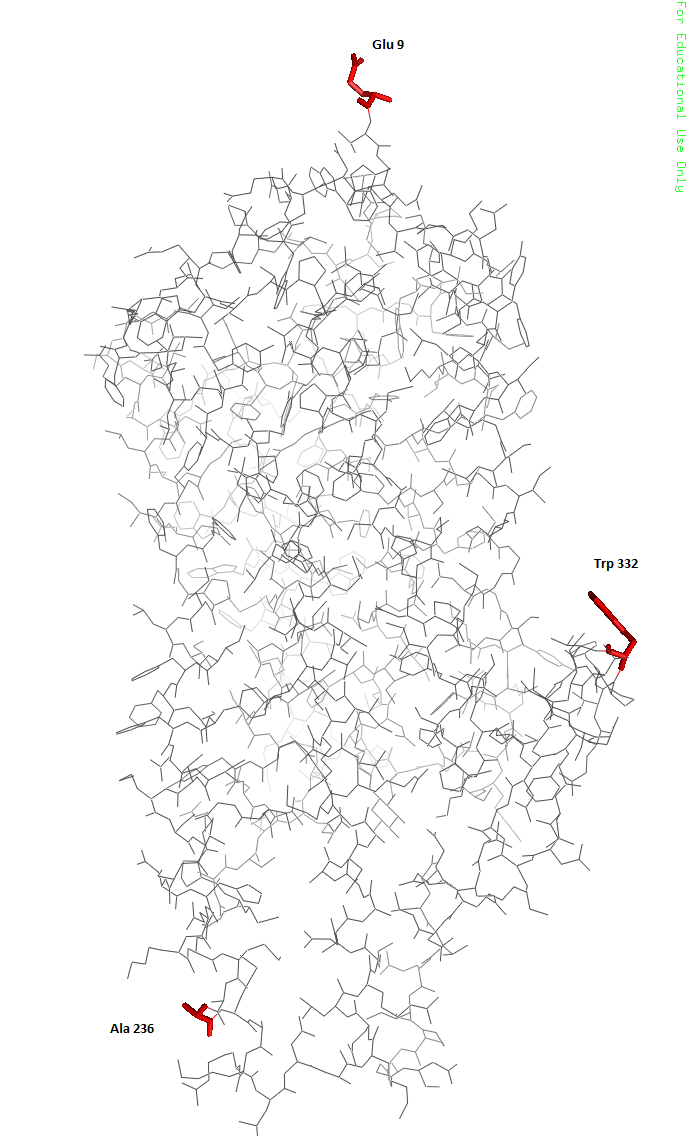
Рисунок 13. Расположение Trp 332, Glu 9 и Ala 236 в структуре родопсина кальмара. |
|
© Шугаева Т.Е. 2014