
|
|
|
Совмещение структурС помощью сервиса PDBeFold были найдены гомологи родопсина кальмара 2Z73. Поиск велся по цепи А, без изменения параметров. Выдача содержала 27 структур, из которых были выбраны три для дальнейшего построения выравнивания. Краткая информация о выбранных гомологах содержится в таблице 1. Первой строкой таблицы идет сам родопсин кальмара. По выбранным гомологам было получено структурное выравнивание: PDB-файл с совмещенными структурами (рисунок 1), выравнивание последовательностей. 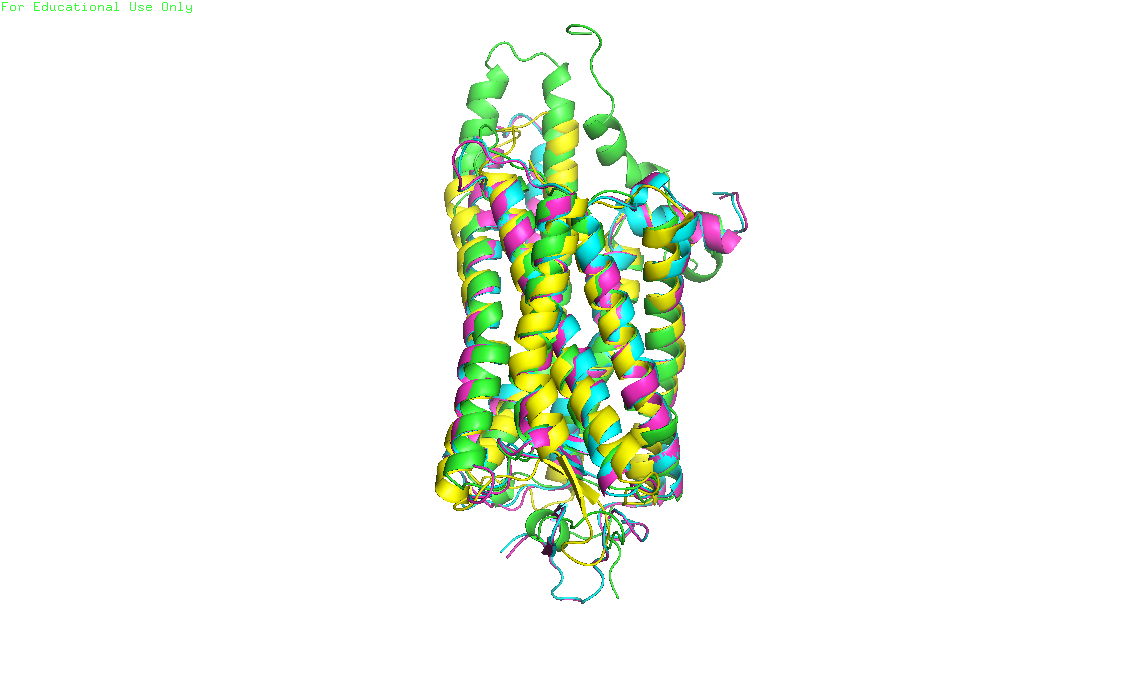
Рисунок 1. Выравнивание структуры родопсина кальмара с тремя гомологами Интересно сравнить выравнивание, полученное по структуре, с выравниванием, полученным программой Muscle. Эти файлы визуализированы на рсиунках 2 - 3. 
Рисунок 2. Выравнивание последовательностей, полученное по структуре 
Рисунок 3. Выравнивание последовательностей, полученное программой Muscle Выравнивания эти похожи, но можно найти большое количество отличий. Например, в выравнивании по структуре в самом начале (позиции 1 - 32) у трех первых последовательностей есть невыровненные "хвосты", что вполне согласуется с визуальным анализом. Это петлевой участок, свободно болтающийся в цитоплазме, который отстутствует у последнего белка 5dgh. Поэтому вариант, как эти начальные участки были обработаны программой Muscle (выровнены с гэпами), мне кажется менее правильным. Еще одно отличие представлено на рисунке 4. Рисунок 4. Слева: выравнивание по структуре. Справа: выравнивание Muscle. Отличие в выравниваниях: первая колонка на показанных фрагментах совпадает, но на позицях 182 - 188 в вырванивании по структуре обнаруживается выпетливание в белке 5dgh. Видно, что положение гэпов отличается. По выравниванию из структурных данных кажется, что эти невыровненные остатки в 5dgh (в pdb номера 142 - 148, позиции в выравнивании 182 - 188) должны сильно отичаться по своему положению от остатков в других структурах. Но визуально это не очень заметно (рисунок 5). 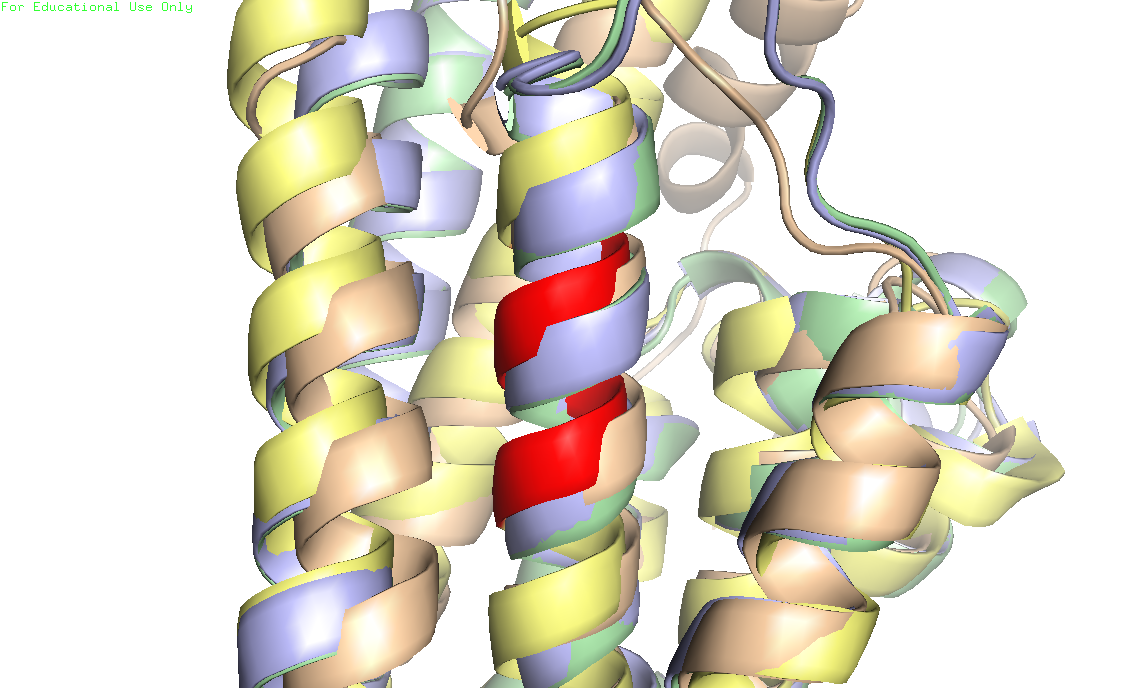
Рисунок 5. Странное место в выравниивании. Красным цветом отмечены интересующие нас остатки 142-148, положение которых должно сильно отличаться Я не вижу оснований утверждать, что данный фрагмент не выровнен с соответсвующими остатками из других структур. Витки альфа-спирали несколько сдвинуты, но все равно хорошо согласуются с таковыми в гомологах. Заключаю, что выравнивание программой Muscle в данном случае правильнее, чем выравнивание по структуре. Построение совмещения по заданному выравниваниюСтруктуру константного домена Т-клеточного рецептора из цепи бета я решила получить из структуры 2Z73, цепь E:113-241 (pdb-файл). Структуру домена альфа - из 1J8H, цепь D:118-203(pdb-файл). С помощью сервиса SheeP по данным PDB-файлам были построены карты бета-листов (рисунки 6-8). Рисунок 6. Карта бета листа из цепи альфа Рисунок 7. Карта первого бета листа из цепи бета Рисунок 8. Карта второго бета листа из цепи бета Листу из домена альфа соответствует бета-лист, изображенный на рисунке 7. Консервативный цистеин в альфа-цепи имеет номер 139, слева соседствет с валином, справа с лейцином. Консервативный цистеин в домене бета идет под номером 142 и имеет тех же соседей. По этом цисеинам и будем проводить совмещение стуктур. Перед совмещением я выбрала необходимые группы атомов: select set1, const_domain_A and resi 138-140; select set2, const_domain_B and resi 141-143. Далее я совместила структуры командой pair_fit set1, set2. Результат приведен на рисунке 9. 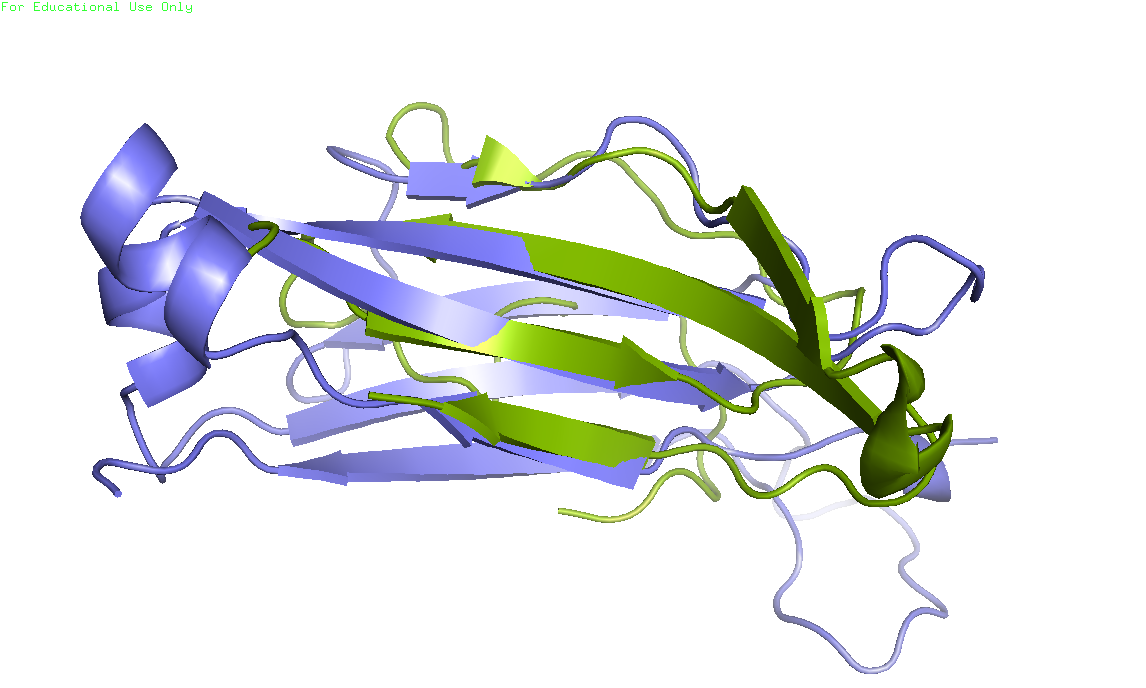
Рисунок 9. Совмещение участков константных доменов альфа и бета. Зеленым изображен домен альфа, синим - домен бета. По совмещению структур видно, что ход цепи совпадает, однако одной из петель домена бета в домене альфа соответсвует петля, прерываемая участком бета-листа и небольшим фрагментом альфа-спирали. И наоборот, в одном из мест, где в домене альфа петля, в домене бета стоит альфа-спираль. Учитывая данные различия, заключить, что топологии одинаковые, нельзя. |
|
© Шугаева Т.Е. 2014