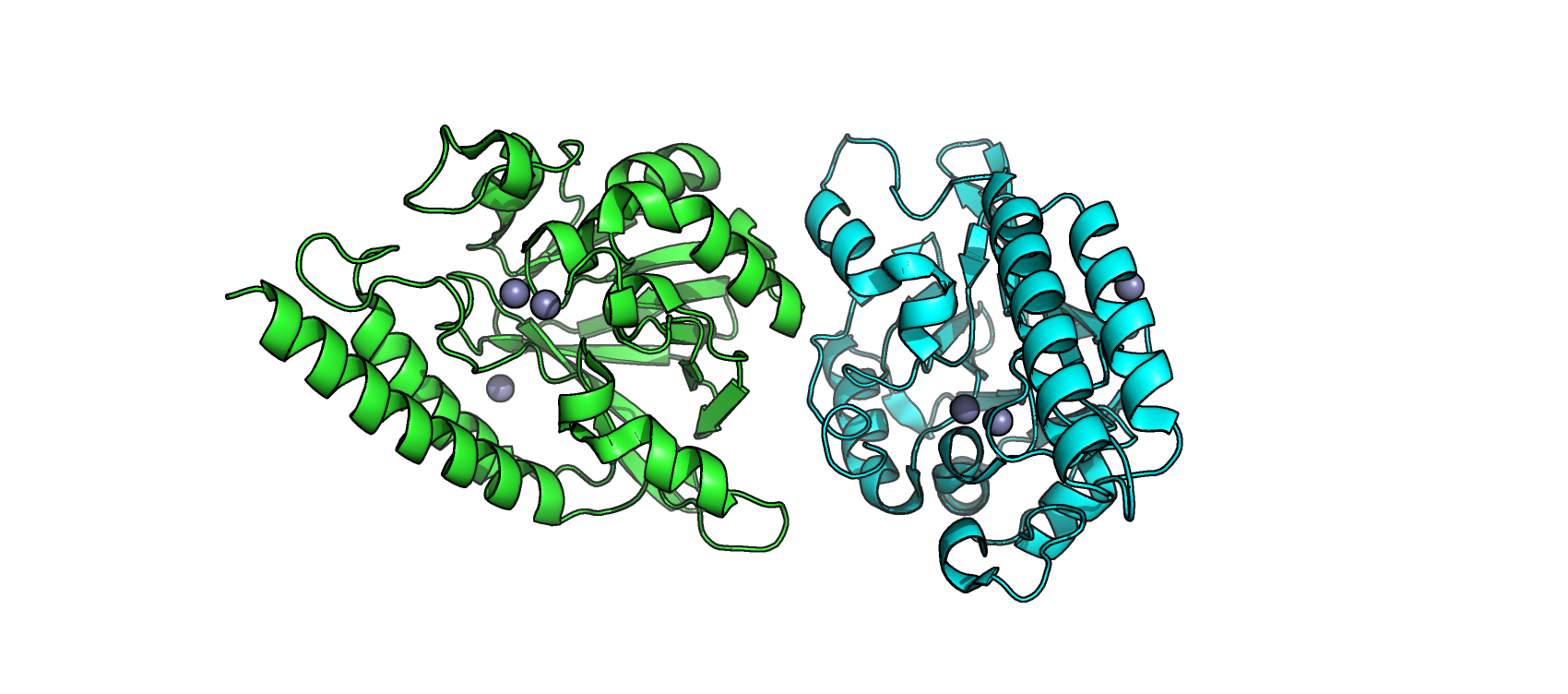Описание структуры и функций белка BJP-1 (металло-бета-лактамазы) из организма Bradyrhizobium japonicum
Практикумы 3 и 4
Структура
1. В данном практикуме идёт описание функций и структуры белка BJP-1 (PDB ID=2GMN), относящегося к классу гидролаз, а точнее — металло-бета-лактамазам (metallo-beta-lactamase).
2. В структуре данного белка присутствуют две полимерные цепи A и B, которые являются полностью идентичными. В этом можно убедиться, сравнив аминокислотные последовательности обеих цепей, которые представлены в разделе SEQRES PDB-файла с описанием структуры белка.
3. Обратившись к разделу файла в формате .pdb под названием REMARK350, можно обнаружить, что биологическая единица представлена мономером, следовательно, в неё может входить либо цепь А, либо цепь В.
Отдельные цепи
1. Обе полимерные цепи А и В односятся к одному и тому же организму — Bradyrhizobium diazoefficiens.
2. Uniprot_id обеих цепей — Q89GW5; название — Blr6230 protein; функция — связывание иона (тяжёлого) металла (metall ion binding).
3. Мутаций ни в одной из цепей нет (Mutation(s): No).
4. Для обнаружения модифицированных аминокислотных остатков необходимо обратиться к разделу MODRES PDB-файла.
Исходя из того, что такого раздела в файле, описывающем данный белок, нет, можно сделать вывод о том, что и нет модифицированных аминокислотных остатков,
однако есть один S-S мостик между 181 и 201 аминокислотам. Ссылка на файл с отчётом.
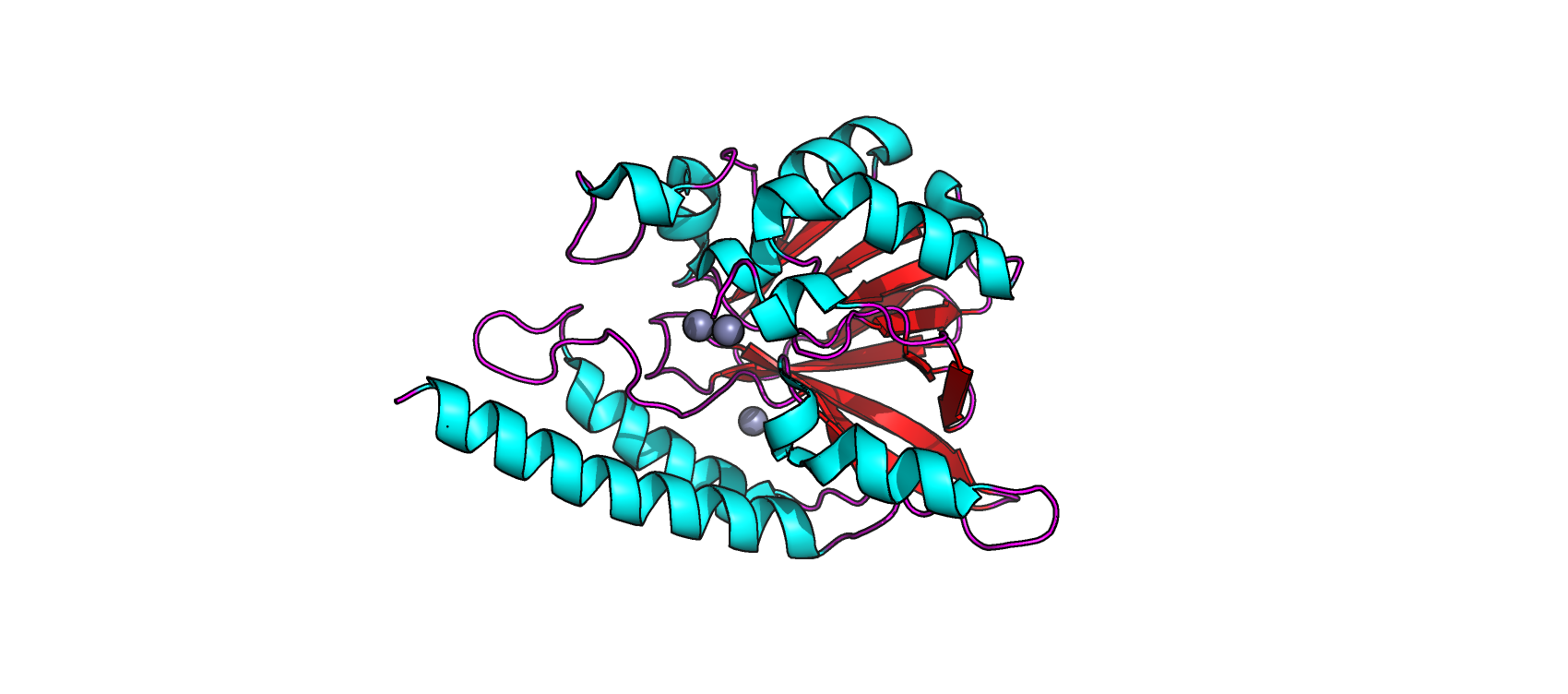
Малые молекулы
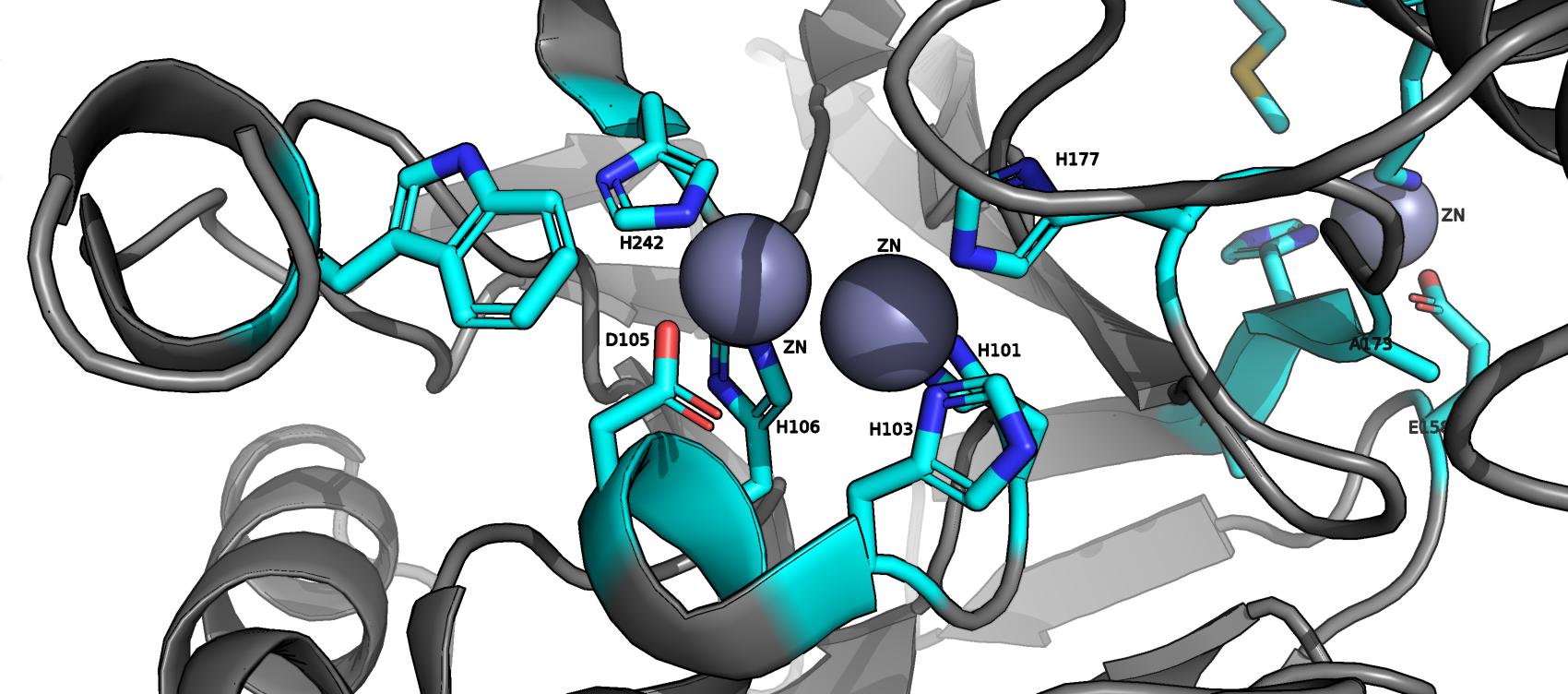
1. К малым молекулам, входищим в состав записи белка, относятся ионы цинк (Zinc, Zn2+, 6 гетероатомов на одну биологическую единицу) и молекулы воды (H2O).
2. Ссылка на отчёт.
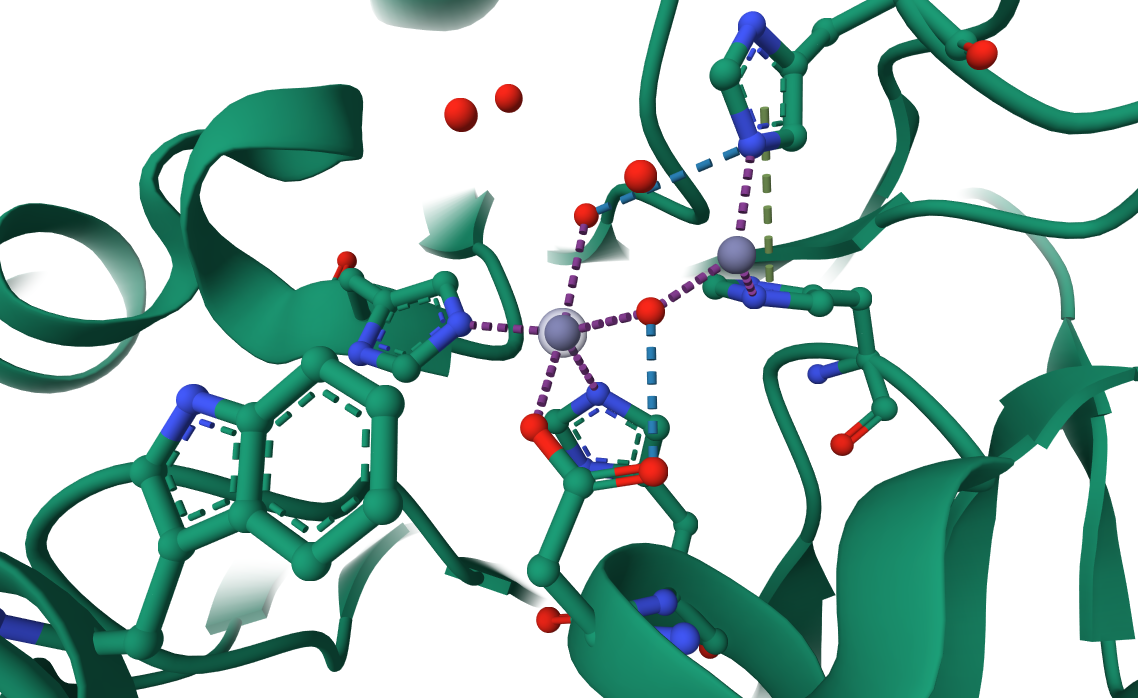
3. Представленные в структуре фермента ионы цинка, согласно статье, входят в состав активного центра и являются кофакторами.
Практикум 5
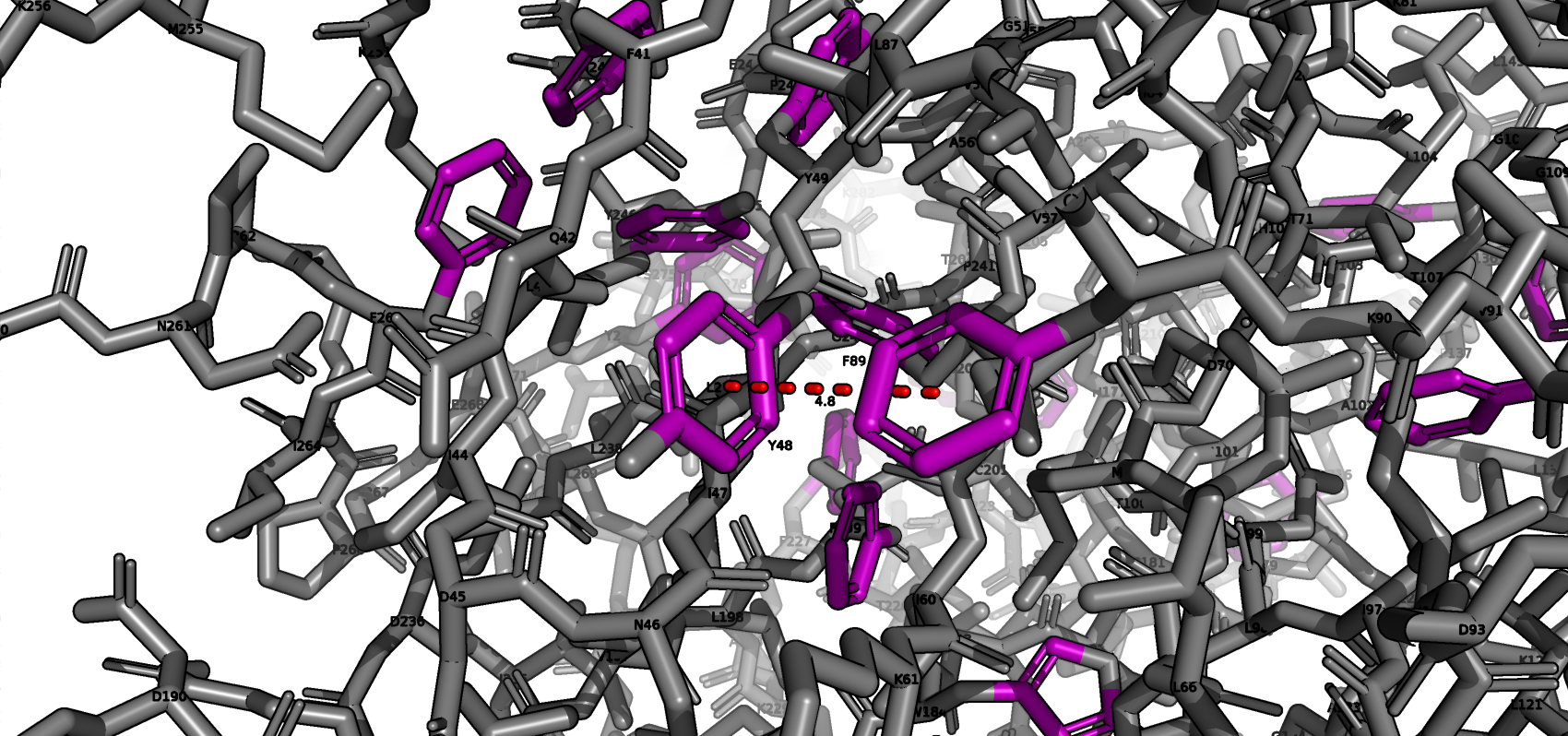
В данном практикуме по PyMOL представлены иллюстрации различных контактов и взаимодействий в структуре изучаемого белка BJP-1 (металло-бета-лактамаза).
Водородные связи
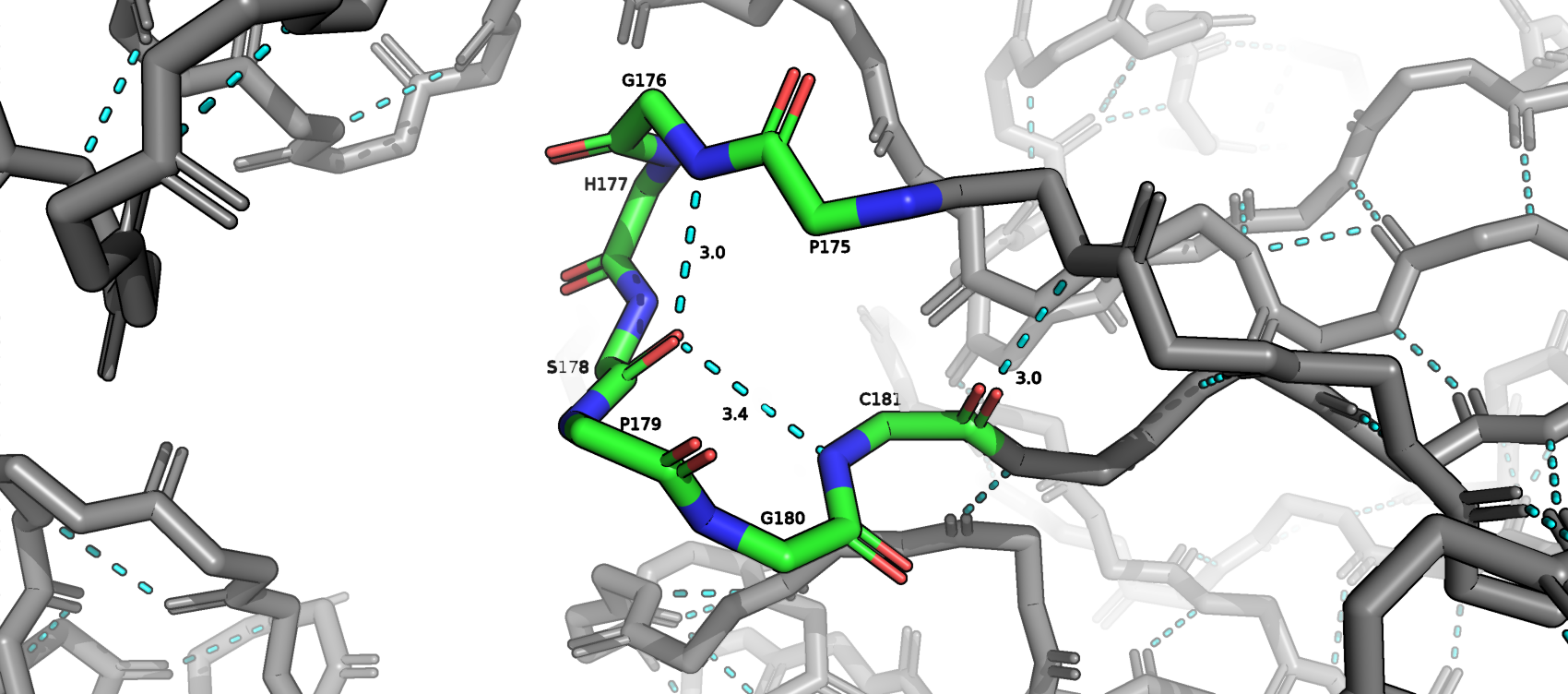
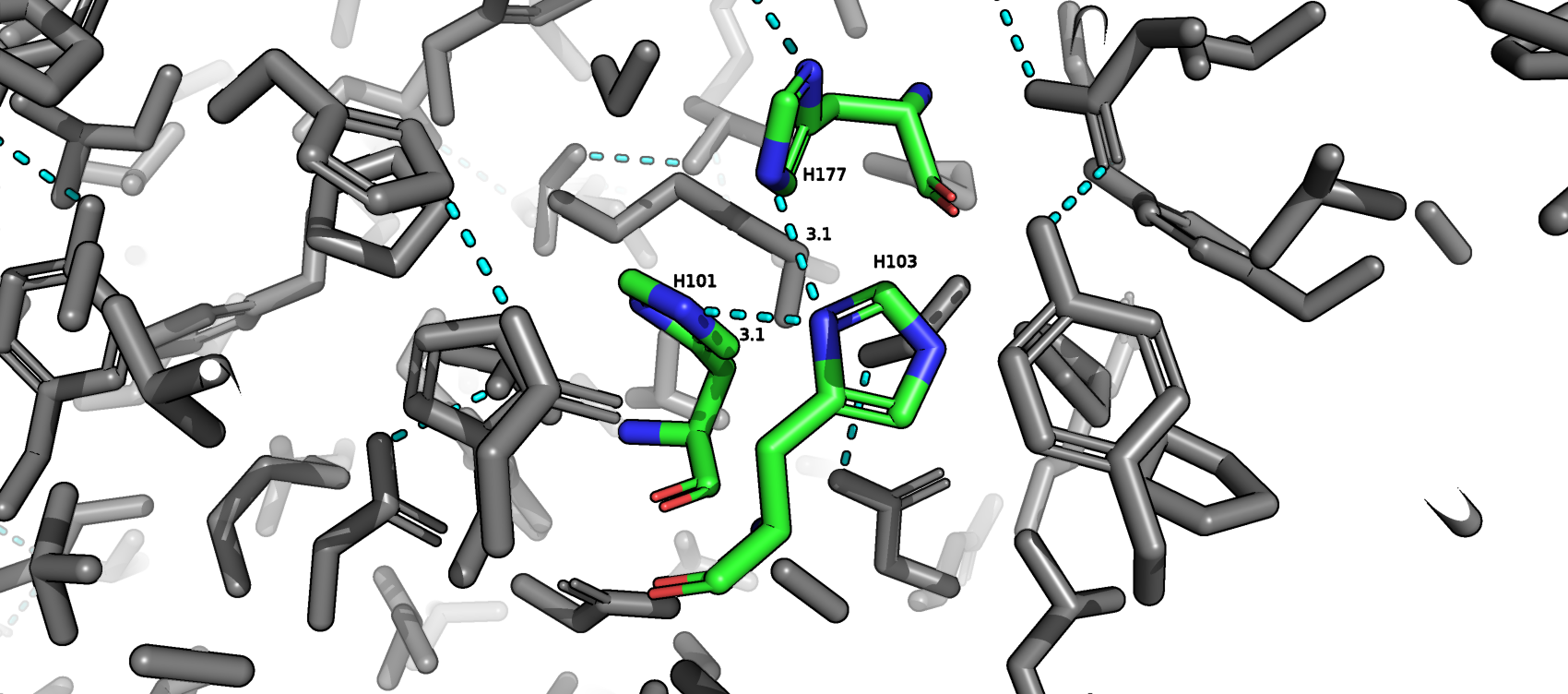
Солевой мостик
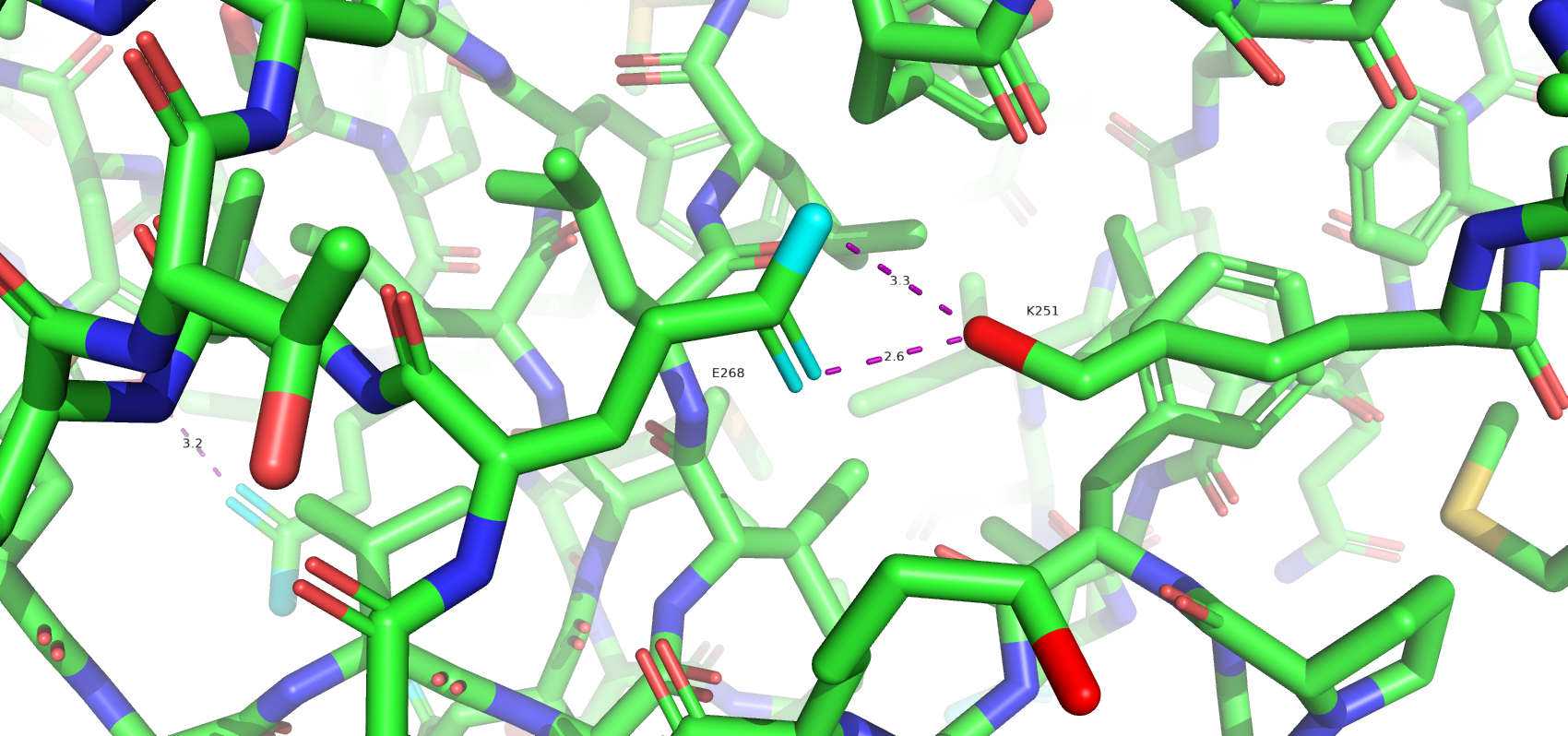
Дисульфидные связи
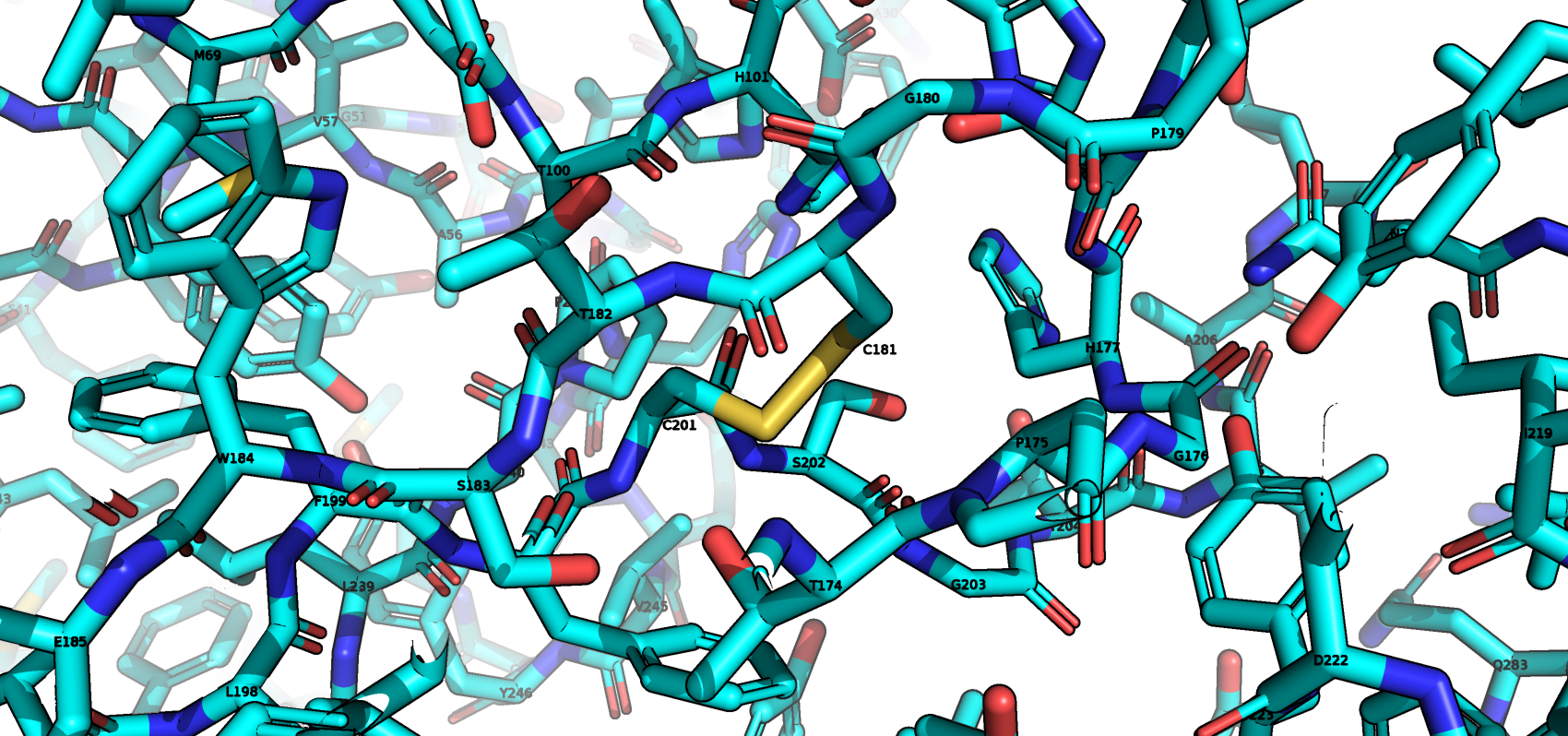
Стекинг-взаимодействия