1. Субстрат: D-Glucose 6-sulfate
2. Продукт: alpha-D-Glucose
3. Уравнение реакции:
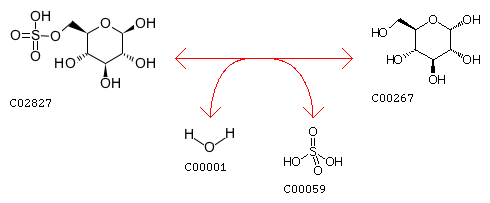
D-Glucose 6-sulfate + H2O <=> alpha-D-Glucose + Sulfate
4. Изображение реакции с помощью структурных формул:

5. Название фермента: glycosulfatase (гликосульфатаза).
6. Код фермента: EC 3.1.6.3.
Расшифровка:
EC 3 — Hydrolases (гидролазы);
EC 3.1. — Acting on ester bonds (действуют на сложноэфирные связи);
EC 3.1.6 — Sulfuric ester hydrolases (действуют в реакциях с сульфогруппами) ;
EC 3.1.6.3 — glycosulfatase (действуют на сульфогруппу в сахарах).
7. Метаболический путь: Glycolysis (гликолиз) . Карту с реакциями этого метаболического пути можно увидеть здесь.
8. Используя карту, можно проследить, из чего мог образоваться данный
субстрат (D-Glucose 6-sulfate) и во что может превратиться заданный продукт
(alpha-D-Glucose).
Субстрат может появиться двумя путями : из альфа- или бета-D-глюкозы (alpha-D-glucose или beta-D-glucose)
9. Продукт может образоваться: из beta-D-glucose (бета-D-глюкоза) , alpha-D-Glucose 1-phosphate (альфа-D-глюкоза 1-фосфат) и alpha-D-Glucose 1-phosphate (альфа-D-глюкоза 6-фосфат) .
Картинка с выбранным фрагментом:
Два выбранных фермента отмечены красным.
| Ферменты | 2.5.1.48 | 2.5.1.47 |
| Название | cystathionine gamma-synthase (цистатионин-синтаза) | cysteine synthase (цистеин-синтаза) | Класс | Transferases (трансферазы) | Transferases (трансферазы) |
| Систематическое название | O4-succinyl-L-homoserine:L-cysteine S-(3-amino-3-carboxypropyl)transferase | O3-acetyl-L-serine:hydrogen-sulfide 2-amino-2-carboxyethyltransferase |
| Расшифровка кода |
EC 2 — трансферазы EC 2.5 — перенос алкильных или арильных групп EC 2.5.1 — перенос алкильных или арильных групп EC 2.5.1.48 — cystathionine g-synthase |
EC 2 — трансферазы EC 2.5 — перенос алкильных или арильных групп EC 2.5.1 — перенос алкильных или арильных групп EC 2.5.1.47 — cysteine synthase |
| Комментарии | ||
| Катализируемая реакция | O-succinyl-L-homoserine + L-cysteine = cystathionine + succinate | O3-acetyl-L-serine + hydrogen sulfide = L-cysteine + acetate |
| Субстрат |
L-Cysteine
O-Succinyl-L-homoserine |
O3-Acetyl-L-serine
Hydrogen sulfide |
| Продукт |
Cystathionine
Succinate |
Acetate L-Cysteine |
| Количество субъединиц | 4 | 2, реже 3 или 4 |
| Оптимум pH | 7.4-8.2 | 6.7-10.5 |
| Кофактор | Pyridoxal phosphate | Pyridoxal phosphate |
Идентификатор использованных карт: 00400.
Из карты видно, что у кишечной палочки (E.coli K-12) имеются ферменты для проведения ВСЕХ реакций биосинтеза.
А теперь посмотрим на метаболический путь внутриклеточного паразита Rickettsia prowazekii.
Здесь нет двух ферментов начальной стадии биосинтеза, а значит, осуществление биосинтеза фенилаланина из хоризмата в организме внутриклеточного паразита Rickettsia prowazekii НЕВОЗМОЖНО.