Практикум 12.
1. Знакомство с базой данных OPM
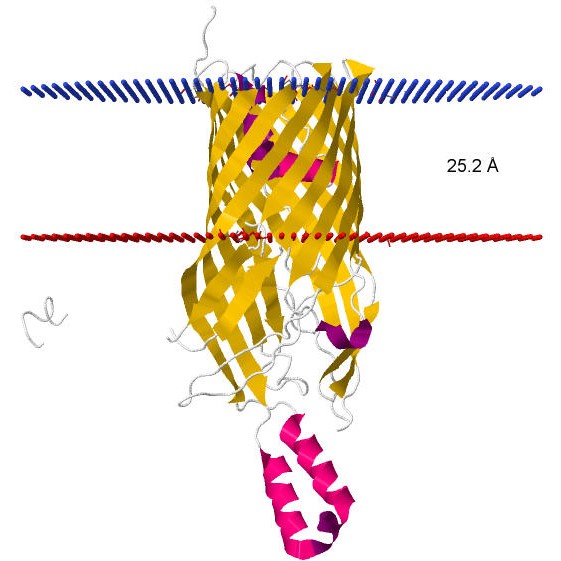
В качестве трансмембранного белка был выбран FadL (FADL_ECOLI, 3pgu) - транспортер длинных жирных кислот внешней мембраны E.coli. Трансмембранная часть этого белка представлена 14-ми β-тяжами из 8-ми аминокислотных остатков, формирующими так называемый β-бочонок.
| Тип | Трансмембранный |
|---|---|
| Класс | Трансмембранный β-бочонок |
| Суперсемейство | FadL белок наружной мембраны |
| Семейство | Транспортеры жирных кислот FadL |
| Организм | Escherichia coli |
| Толщина гидрофобной части | 25.2 Å | Координаты трансмембранных участков | 1( 43- 52), 2( 78- 87), 3( 94- 101), 4( 126- 135), 5( 142- 149), 6( 207- 216), 7( 223- 229), 8( 274- 281), 9( 289- 296),10( 325- 333),11( 341- 348),12( 367- 376),13( 383- 390),14( 411- 421) |
| Среднее количество остатков в одном β-тяже белка | 8 |
| Локализация | Внешняя мембрана Грам-отрицательных бактерий |
2. DeepTMHMM: Предсказание трансмембранных элементов по последовательности белка
Белок(α):CBSB_SACS
Fasta-файл: seq
Выдача: файл
Обсуждение:
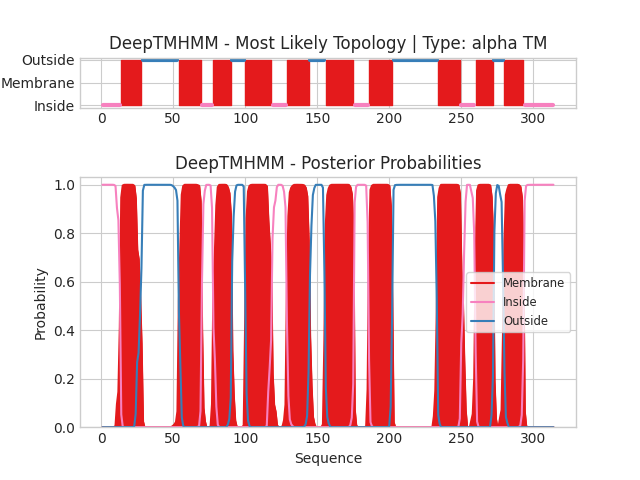
Сервис DeepTMHMM позволяет предсказывать трансмембранные участки по первичной структуре белка. В графической выдаче по горизонтали отложены координаты остатков белка, на вертикальной оси показаны предсказание положение определенных участков (верхний рисунок) и вероятность принадлежности конкретного остатка к той или иной топологии (нижний рисунок). Каждый цвет означает определенную локализацию участка: Membrane - трансмембранный, Inside - внутриклеточный, Outside - внеклеточный.
Для выданного белка было предсказано 10 трансмембранных участков (α-спиралей). N- и C-конецы белка согласно предсказанию являются внутриклеточными.
Белок(β): FADL_ECOLI
Fasta-файл: seq
Выдача: файл
Обсуждение:
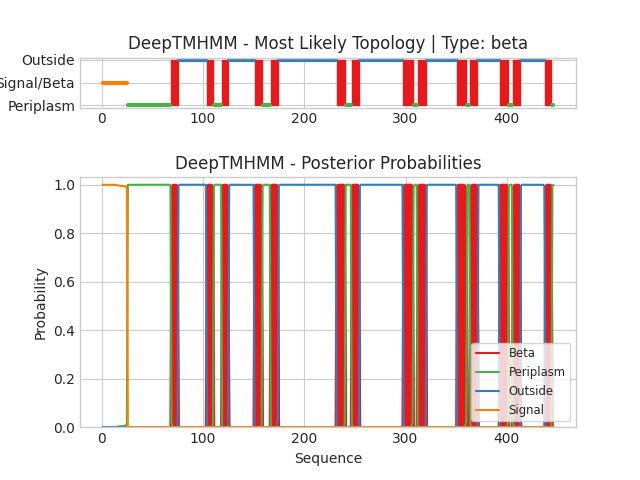
Смысл полученных изображений и значение осей аналогичны выдаче для α-спирального белка. Каждый цвет означает определенную локализацию участка: Beta - бета-слой (мембранный), Periplasm - периплазматический (аналог внутриклеточной части), Outside - внеклеточный, Signal - сигнальный пептид для периплазматической локализации.
Для выданного белка было предсказано 14 трансмембранных участков (β-слоев). N-конец белка является сигнальным пептидом, за ним согласно предсказанию следует периплазматический участок, а С-конец - внеклеточным. Стоит сказать, что предсказания, на первый взгляд, не совпадают с OPM, однако в данной выдаче учитывается сигнальный пептид. Поэтому координаты всех предсказанных β-слоев как бы "смещаются" на его длину.
3. PPM: Предсказание положения выданного белка в мембране
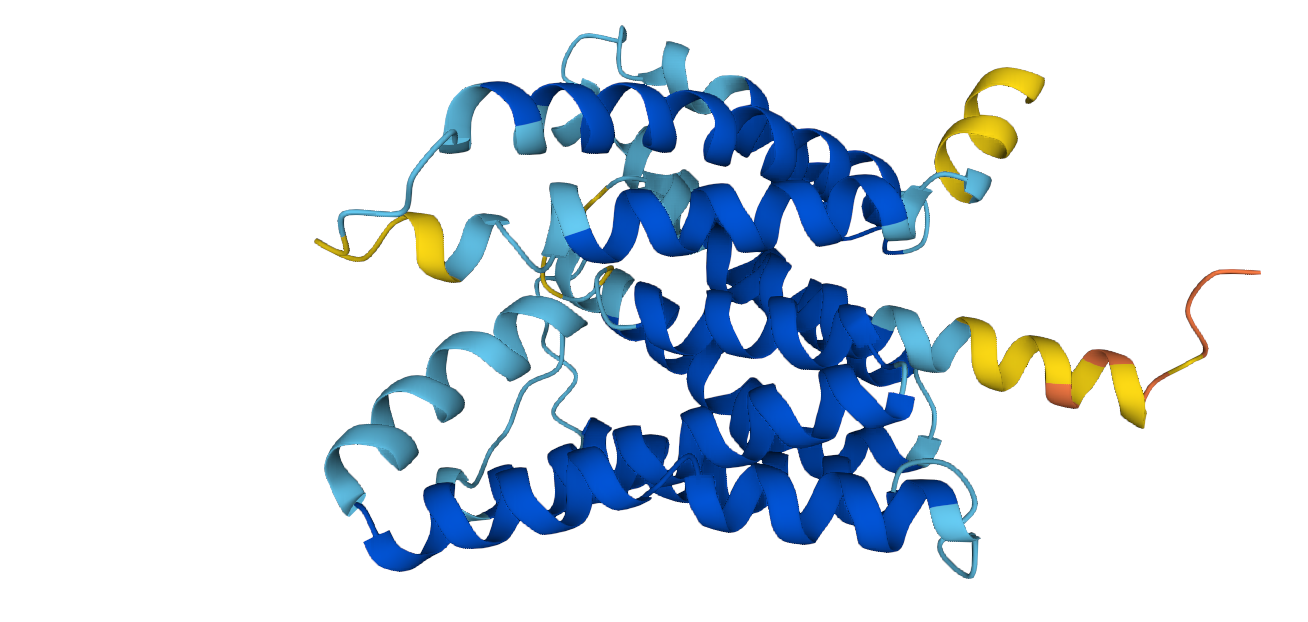
В данном разделе проведено предсказание топологии для выданного альфа-спирального белка TetB Streptomyces rimosus с помощью сервиса PPM 3.0 на сайте OPM.
Для запуска сервиса необходимо определиться с большим количеством параметров:
- Number of Membranes: 1
- Type of membrane: Archeabacteria cell membrane (по данным Wikipedia Saccharolobus solfataricus является археей)
- Allow curvature: no (чтобы не усложнять анализ выдачи)
- Topology (N-ter): in (по предсказанию DeepTMHMM)
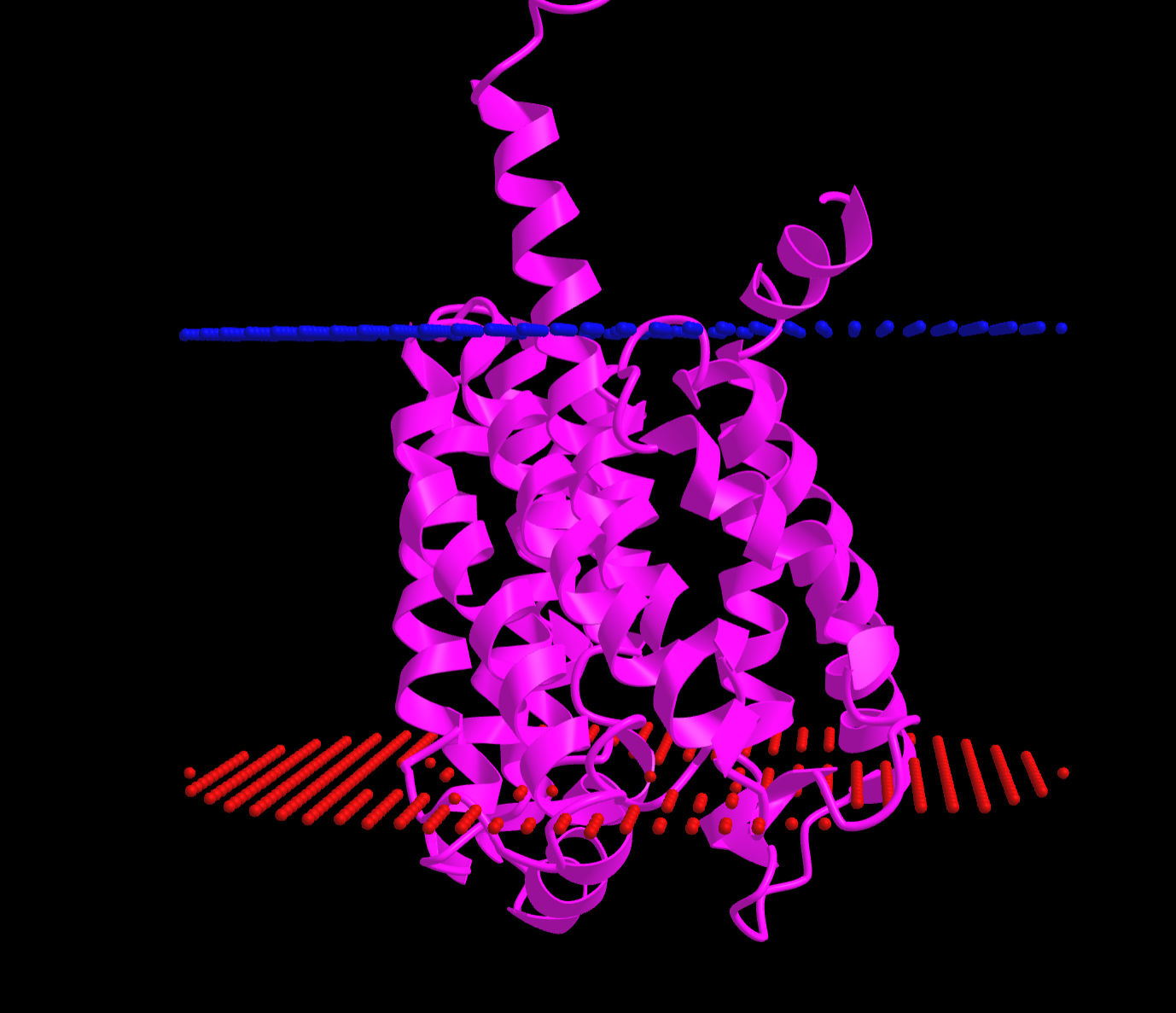
Для этого белка не существует достоверной структуры, однако существует ее модель, которая предсказана с помощью AlphaFold. Программе передавался файл с предсказанной структуры в формате pdb. С полученной моделью можно ознакомиться по ссылке.
| Толщина гидрофобной части (Глубина) | 30.2 ± 0.8 Å |
|---|---|
| ΔGtransfer | -80.1 kcal/mol |
| Угол изгиба | 16 ± 3° |
| Трансмембранные сегменты | 1( 10- 31), 2( 47- 71), 3( 76- 92), 4( 99- 126), 5( 127- 147), 6( 159- 176), 7( 183- 204), 8( 235- 257), 9( 258- 274),10( 280- 297) |
| Средняя длина трансмембранного сегмента | 12 остатков |
4. Сравнение алгоритмов предсказания трансмембранных участков
DeepTMHMM
Предсказанные трансмембранные участки:
- 14 - 28
- 54 - 69
- 78 - 90
- 100 - 118
- 129 - 144
- 156 - 175
- 186 - 202
- 234 - 249
- 260 - 272
- 280 - 293
PPM
Предсказанные трансмембранные участки:
- 10- 31
- 47- 71
- 76 - 92
- 99 - 126
- 127 - 147
- 159 - 176
- 183 - 204
- 235 - 257
- 258 - 274
- 280 - 297
Обсуждение
Можно с уверенностью сказать, что предсказания разных программ значительно похожи. Чаще всего, DeepTMHMM "пропускает" 2-3 остатка на C и N-концевых сторонах участков, однако число и общее положение трансмембранных спиралей совпадают.
Стоит отметить, что положение каждого остатка в предсказанной с помощью AlphaFold структуры характеризуется своим доверительным score'ом (насколько точно верно предсказание). Что интересно, участки трансмембранных α-спиралей с относительно низким весом (70 > pLDDT > 50 - желтый цвет) как раз отличаются в вышеполученных предсказаниях.
В целом, можно считать, что структура предсказана успешно, так как в состав предсказанных α-спиралей (хоть и с низким весом) входят остатки, чье положение PPM считает трансмембранным, как и остатки, которые достоверно предсказаны хорошо.