Трансмембранные белки
Знакомство с OPM
При работе с трансмембранными белками нередко необходимо определить его положение относительно мембранны.
Одним из возможных способ это узнать, поискать информацию в базе данных OPM, знакомство с которой стало нашей первой задачей в этом практикуме.
Классификация белков в базе данных устроена следующим образом:
1. Тип: положение структуры, относительно мембранны (трансмембранный белок, периферический белок и тд.)
2. Класс: вторичная структура белка (только альфа-спирали, тольео бета-листы и тд.)
3. Суперсемейство: эволюционно связанные белки, с совпадающей 3D-структурой
4. Семейство: гомологичные белки
При описании белка встречаются ссылки на PDB, PDBsum (БД с визуализацией PDB структур), MPKS (курируемая ДБ с 3D-структурой белков), MMDB (Molecular Modeling Database), Uniprot, Pfam, InterPro, TCDB (transporter classification database).
Далее в базе OPM был найден белок, у которого трансмембранным сегментом является бета-лист: Gasdermin-D.
Это белок человека, играющий ключевую роль в программируемой гибели клеток. Выбрал я его, потому что это белок
с наибольшим количестовм субъединиц (33) и вторичных структур (132) из всех поринов, содержащихся в OPM. В неактивном состоянии этот белок представлен отдельными субъединицами, которые при активации олигомерезуются и формируют пору в клеточной мембранне диаметром 10-20 нм, что нарушает осмотический баланс, клетка набухает и разрушается.
Основное задание
В данном задании мы продолжим изучение трансмембранных белков, на примере рассмотренного выше гасдермина D (gasdermin D)
ссылки на БД: GSDMD_HUMAN (Uniprot) и 6VFE (PDB)
Нам было интересно сравнить предсказание координат трансмембранных участков белка по последовательностям (предсказанных программой DeepTMHMM) с
предсказанием по трехмерной структуре (взятое из БД OPM).
Сперва нашли координаты трансмембранных участков в базе OPM, они оказались идентичны для всех субъедениц: 1( 91- 97), 2( 103- 108), 3( 180- 186), 4( 191- 197)
Далее по аминокислотной последовательности белка было необходимо получить предсказание о трансмембранной локализации участков с помощью программы DeepTMHMM, однако результаты получились неутешительными. Программа не нашла ни одного трансмембранного участка и определила локализацию белка как внутриклеточную. Скорее всего это связано с тем, что обычно белок правда локализован внутриклеточно, а в мембранну встраивается только после расщепления N-концевого фрагмента.
Далее для успешного выполнения задания мы обратились к белку сytochrome bc1 (цитохром-bc1) из предложенного списка трансмембранных альфа-спиральных белков.
Ссылки на БД: 4D6T (PDB) и список Uniprot ID: CY1_BOVIN, CYB_BOVIN, QCR1_BOVIN, QCR2_BOVIN, QCR6_BOVIN, QCR7_BOVIN, QCR8_BOVIN, QCR9_BOVIN, UCRI_BOVIN
Изучаемый белок (цитохром) - это главный генератор протонного градиента на внутренней мембране митохондрий, в моем случае митохондрий быка (Bos taurus)
Всего у этого белка 11 субъединиц, для вторичных структур которых характерны 5 различных координат:
1. Chain: C, P - TM segments: 1( 28- 50), 2( 82- 107), 3( 112- 130), 4( 180- 200), 5( 224- 245), 6( 289- 307), 7( 319- 340), 8( 348- 369)
2. Chain: D, Q - TM segments: 1( 204- 224)
3. Chain: E, R - TM segments: 1( 34- 59)
4. Chain: G, T - TM segments: 1( 43- 62)
5. Chain: J, W - TM segments: 1( 18- 39)
Далее аминокислотную последовательность в формате FASTA, взятую из базы PDB мы подавали на вход программе DeepTMHMM.
Программа предсказала только 8 трансмембранных сегментов со следующими координатами:
1. Chain: C, P - TM segments: 1( 30- 52), 2( 76- 103), 3( 114- 134), 4( 173- 200), 5( 223- 245), 6( 287- 307), 7(319- 339), 8(347- 365)
2. Chain: D, Q - TM segments: 1( 232- 246)
3. Chain: G, T - TM segments: 1( 42- 62)
4. Chain: J, W - TM segments: 1( 24- 47)
Ссылка на результаты
Предсказание DeepTMHMM заметно отличается от данных из OPM, количество найденных трансмембранных сегментов меньше (отсутвуют сегменты в цепях E и R), и границы найденных участков не совсем точно попадают в границы из базы OPM.
Аминокслотная последовательность для цепей E, R в границах аминокислот, формирующих трансмембранную альфа-спираль выглядит следующим образом:
VPATSESPVLDLKRSVLCRESLRGQA
Можно предположить, что из-за большого числа заряженных и полярных аминокислот, программа DeepTMHMM делает вывод о невозможности локализации этой последовательности трансмембранно, где преимущественно находятся гидрофобные аминокислоты.
Сдвиг границ трансмембранных участков, возможно, объясняется тем же. Или же различия заключаются в том, что программа DeepTMHMM
подругому моделирует границу мембранны, к примеру берет ее немного другой толщины, или не учитывает, что альфа-спираль может располагаться в мембранне не полностью/под наклоном, что
показывает лишь приближенную картину трансмембранных координат.
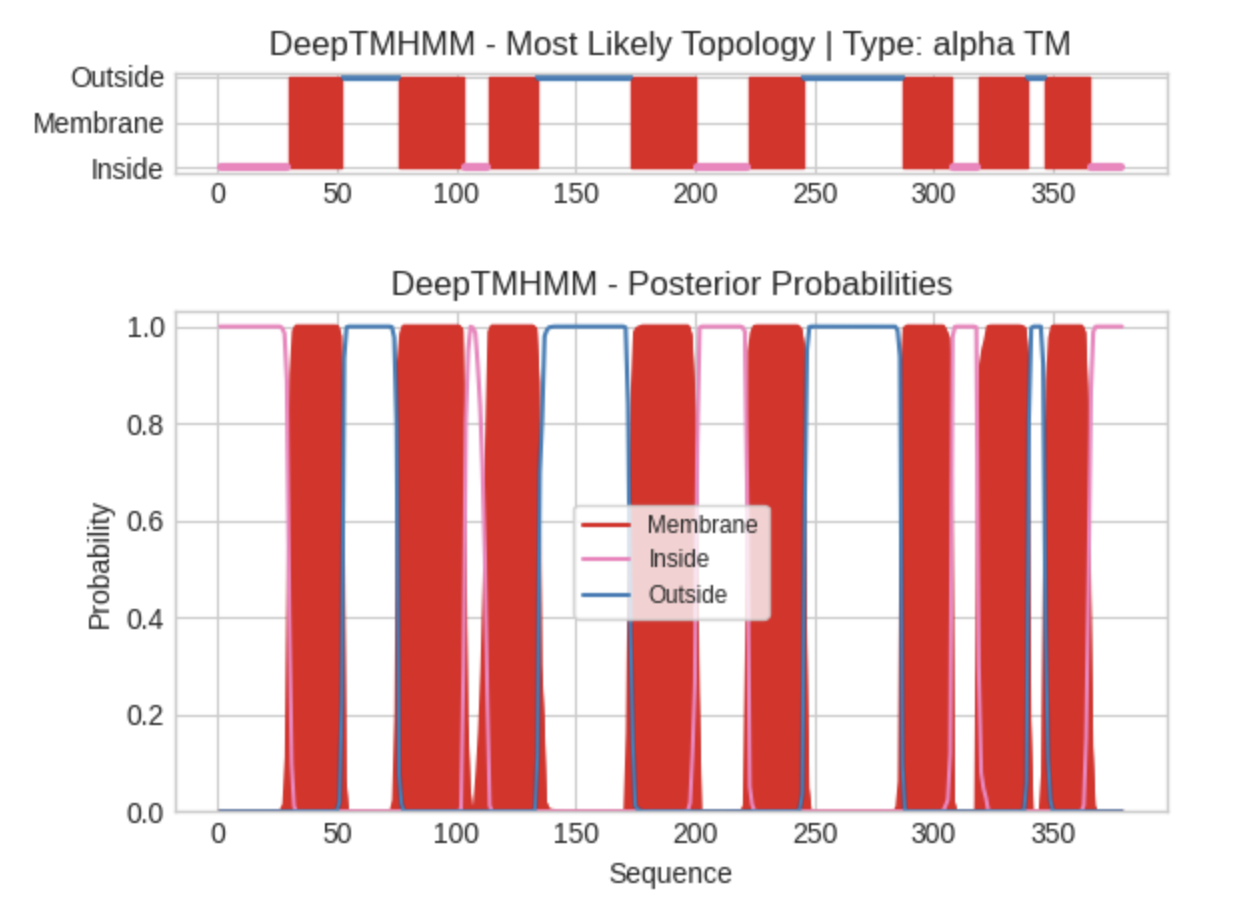 Рис. 1. Выдача программы DeepTMHMM для цепи C и P. Верхняя картина - наиболее вероятная топология субъеденицы, нижняя - топология с вероятностью нахождения аминокислот трансмембранно или по одну из сторон мембранны. По оси X - порядковй номер аминокислотного остатка.
Рис. 1. Выдача программы DeepTMHMM для цепи C и P. Верхняя картина - наиболее вероятная топология субъеденицы, нижняя - топология с вероятностью нахождения аминокислот трансмембранно или по одну из сторон мембранны. По оси X - порядковй номер аминокислотного остатка.