Обзор особенностей генома археи Halobacterium salinarum
Виолентий Виталий Викторович
Факультет биоинженерии и биоинформатики, Московский государственный университет имени М.В. Ломоносова
Аннотация. В данной работе были изучены некоторые особенности генома чрезвычайно галофильной, радиационно-устойчивой археи Halobacterium salinarum. Были рассмотрены гипотезы, объясняющие эти адаптации, а также произведён поиск белков, которые могут обеспечивать устойчивость к ионизирующему излучению.
Введение
Halobacterium salinarum (некорректное название – Methanobacterium salinarum) – аэробная гетеротрофная галофильная архея, обитающая в гиперсолёных местообитаниях. Она относится к домену Archaea, царству Metanobacteriati, филуму Methanobacteriota, классу Halobacteria, порядку Halobacteriales и семейству Halobacteriaceae, согласно NCBI Taxonomy (https://www.ncbi.nlm.nih.gov/datasets/taxonomy/2242/). H.salinarum была открыта в 1922 году, а сейчас представляет интерес как модельный организм для изучения адаптаций к гиперсолёной среде. На ней также изучались мембранные липиды, специфичные для архей, белки S-слоя и бактериородопсин [1].
Ещё одной примечательной особенностью H.salinarum является высокая устойчивость к радиации (ионизирующему излучению, далее – ИИ). Первоначально устойчивость к ИИ изучалась на примере бактерии Deinococcus radiodurans. Она была открыта в ходе эксперимента по стерилизации мясных консервов гамма-излучением, где вызывала их порчу [2]. Известно, что Deinococcus radiodurans может выдерживать очень высокие дозы ИИ (более 12 кГр) [3], в то время как, например, 99% клеток E.coli погибает от дозы в 700 Гр [4].
Было высказано немало гипотез насчёт того, чем может быть обусловлена такая высокая устойчивость к ИИ. Как ни странно, её не удаётся хорошо объяснить наличием высокоэффективных систем репарации ДНК [5]. Количество разрывов в ДНК, вызванных облучением, у устойчивых к ИИ бактерий оказывается примерно таким же, как у восприимчивых. Однако первые при этом могут восстановить повреждения ДНК (D.radiodurans выживает даже после образования 2000 двуцепочечных разрывов [2]), а вторые - нет. Главным выводом, сделанным по итогам многих лет исследований устойчивости к ИИ, стало то, что она в первую очередь обеспечивается защитой не ДНК, а белков от окислительного повреждения. Было показано, что она зависит от отношения концентраций марганца и железа в цитоплазме клетки (отношения Mn/Fe). В то время как железо может вступать в реакцию Фентона, приводящую к образованию опасных гидроксильных радикалов, марганец, наоборот, способен нейтрализовать активные формы кислорода, находясь в комплексе с различными малыми молекулами, такими как ортофосфат-ионы, нуклеотиды, аминокислоты и короткие пептиды. Антиоксидантные комплексы Mn2+ с пептидами и ортофосфатом были признаны важным элементом системы защиты от ИИ [3, 6]. Источник этих пептидов остаётся неизвестным – возможно, они поступают извне (D.radiodurans является протеолитической бактерией [7]), возможно – являются продуктами распада других белков, вызванного ИИ [8], или же синтезируются отдельно.
Как в процессе эволюции могла развиться устойчивость к таким дозам ИИ, которые в тысячи раз выше, чем естественный радиационный фон? Было замечено, что высокой устойчивостью отличаются бактерии, резистентные также к высыханию – многие виды Deinococcus встречаются в пустынных местообитаниях и часто подвергаются дегидратации [5, 9]. Аналогично, многие почвенные актинобактерии выдерживают большие дозы ИИ и при этом обладают устойчивостью к высыханию [10]. Можно провести параллель с галоархеями – они часто обитают в солёных пересыхающих водоёмах, поэтому также должны быть устойчивы к длительному высыханию. Дискуссионным вопросом является то, какой может быть продолжительность такого возможного анабиоза. Некоторые авторы полагают, что галоархеи могут сохранять жизнеспособность в кристаллах каменной соли на протяжении миллионов лет [11, 12].
Как и наиболее устойчивые виды Deinococcus – D.radiodurans и D.geothermalis – H.salinarum содержит много копий генома на клетку [13] (что, как предполагается, должно способствовать восстановлению ДНК путём гомологичной рекомбинации [2]), а также имеет высокое отношение Mn/Fe [14]. Кроме того, его геном содержит большое количество гомологов с D.radiodurans [15]. Это может указывать на наличие сходных механизмов устойчивости, в частности – механизма производства пептидов, связывающих ионы Mn.
Одной из адаптаций галофильных архей к гиперсолёной среде является повышенное содержание в белках кислых аминокислот. Считается, что это необходимо для повышения растворимости белков, предотвращения их агрегации и осаждения в условиях осмотического стресса [16]. Важно отметить, что особенно значительное обогащение кислыми аминокислотами показывают «участки с низкой сложностью» (LCR – low-complexity regions). LCR определяются как участки белка, в составе которых наблюдается значительное смещение в сторону каких-либо аминокислот, и часто соответствуют внутренне-неупорядоченным областям в белках. Помимо этого, известно, что LCR, содержащие остатаки аспартата, глутамата и гистидина (далее в тексте – «хелатирующие аминокислоты»), часто связывают металлы [17]. Стоит добавить, что некоторые из белков D.radiodurans, предположительно задействованных в устойчивости к ИИ, также имеют значительное содержание LCR [18].
Можно предположить, что если некий белок будет иметь высокое содержание LCR, которые при этом будут обогащены хелатирующими аминокислотами, то, возможно, он сможет эффективно связывать ионы Mn2+ и таким образом обеспечивать защиту от ИИ. Если содержание LCR в белке высокое, то, скорее всего, перечень его возможных функций будет сильно ограничен (как уже говорилось, LCR обычно не имеют стабильной укладки), так что такие гипотетические белки могут рассматриваться как кандидаты на роль белков, непосредственно задействованных в марганец-зависимом механизме защиты от ИИ. В то же время, если смещение в сторону LCR, обогащённых хелатирующими аминокислотами, (подобно тому, что наблюдается у галоархей), будет наблюдаться для большого количества белков отдельно взятой радиационно-устойчивой бактерии, можно будет предположить, что устойчивость к ИИ определяется связыванием ионов Mn2+ не специализированными для этого белками, а большой частью протеома.
Материалы и методы
Распределения длин белков и GC-состава генов были проанализованы при помощи методов электронных таблиц (см. С1). Кодирующие последовательности, соответствующие сборке генома GCF_000006805.1, были взяты с сайта FTP NCBI. Для выявления LCR в белках использовалась программа fLPS2 с настройками, рекомендованными разработчиком для поиска LCR [19, 20, 21] (см. С2), последовательности белков из референсных геномов были взяты с ресурса NCBI Genome (сборки GCF_000006805.1, GCF_000008565.1, GCF_000196275.1, GCF_000091545.1, GCF_000005845.2, GCF_000146165.2). Из полученных данных были исключены LCR, аннотированные как полная исходная последовательность. Затем с помощью Python для каждого белка перекрывающиеся LCR были объединены, был рассчитан процент содержания LCR в белке и процент содержания остатков аспарагиновой кислоты, глутаминовой кислоты и гистидина во всех LCR (см. С2). Построение диаграмм проводилось с помощью электронных таблиц. Для поиска гомологичных белков использовался инструмент Protein BLAST (https://blast.ncbi.nlm.nih.gov/Blast.cgi).
Результаты и обсуждение
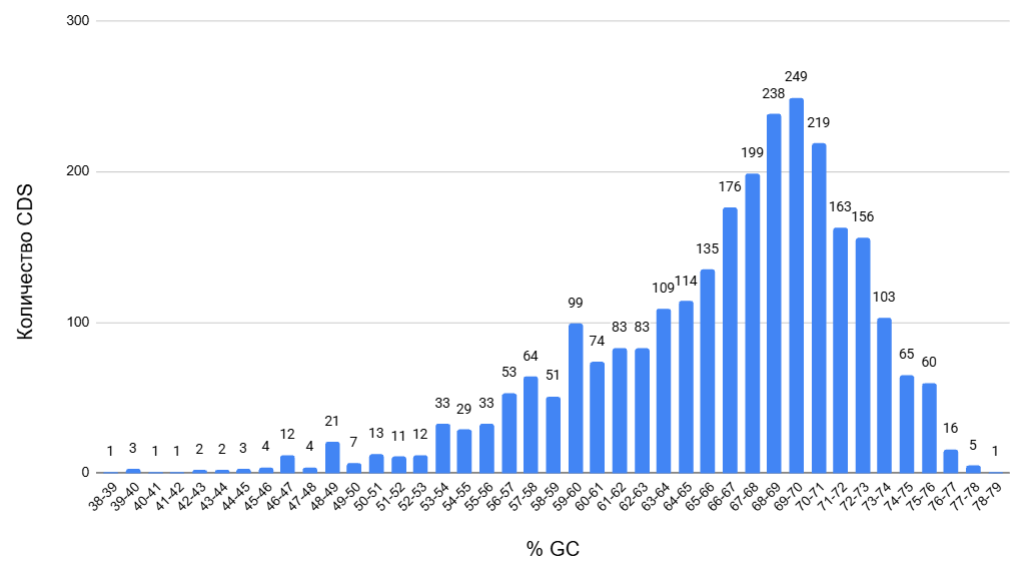
Распределение GC-состава (GC%) CDS. Была получена гистограмма, отражающая распределение CDS по GC-составу (рис. 1). Наблюдается распределение с пиком на 69-70%, содержащим 249 CDS. Кроме того, есть пик на 59-60%, и повышенное количество CDS для 48-49% и 46-47%. Эти значения, выбивающиеся из общей закономерности, могут быть свидетельством горизонтального переноса генов от организма с меньшим содержанием GC в геноме.
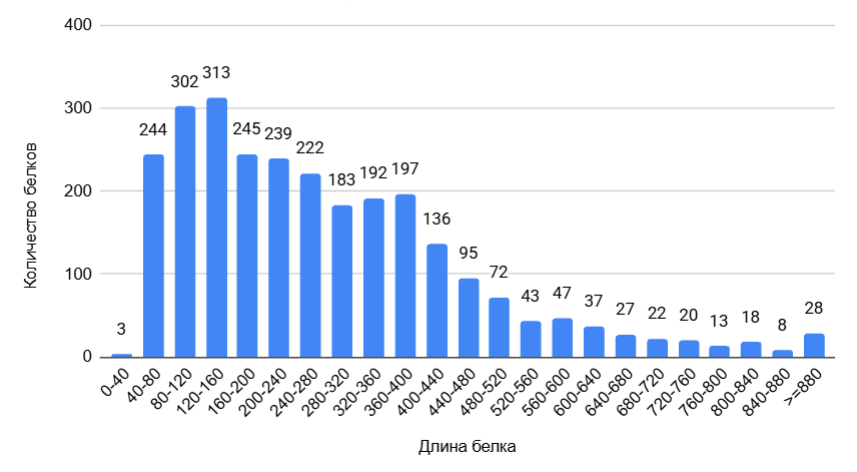
Распределение длин белков. Была получена гистограмма длин белков, закодированных в геноме H.salinarum (рис. 2). Наблюдается распределение с 2 пиками, из которых один соответствует белкам длиной 120-160 аминокислот и содержит 313 белков, а другой – белкам длиной 360-400 аминокислот, и содержит 197 белков. Средняя длина белка составляет 280 аминокислот; самый длинный белок, большая субъединица ДНК-зависимой ДНК-полимеразы II, содержит 1370 аминокислот; самый короткий, субъединица KdpF калиевой АТФазы, содержит лишь 29 аминокислот. Более коротких пептидов, аналогичных предполагаемым пептидам Deinococcus, не обнаруживается. Это, однако, не означает, что они не могут быть закодированы в геноме H.salinarum – современные алгоритмы аннотации генома не распознают такие короткие последовательности.
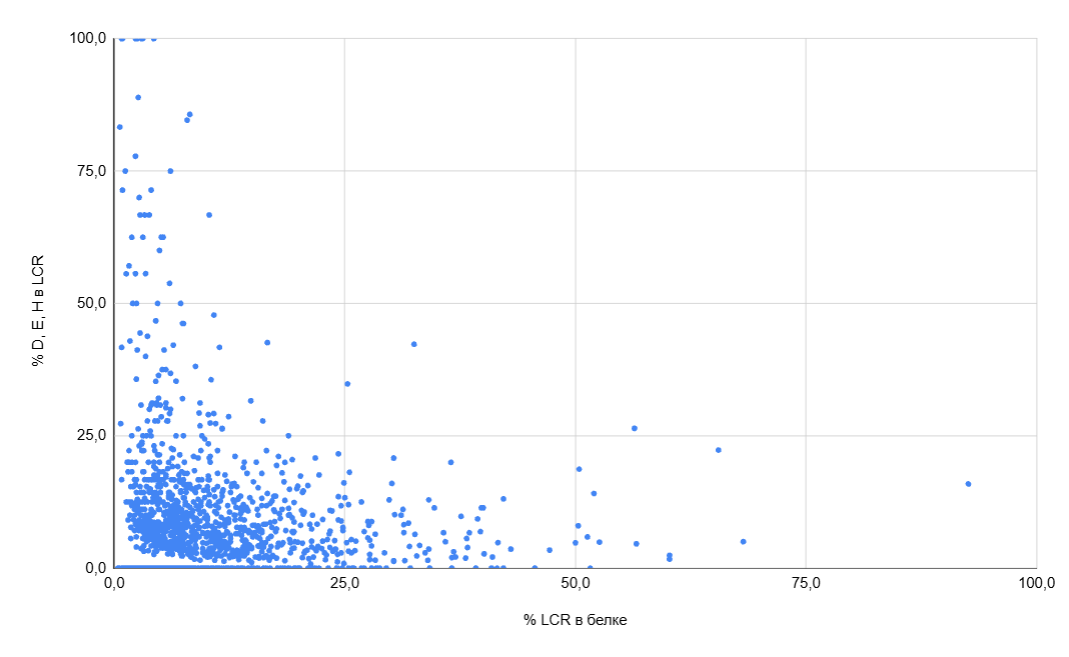
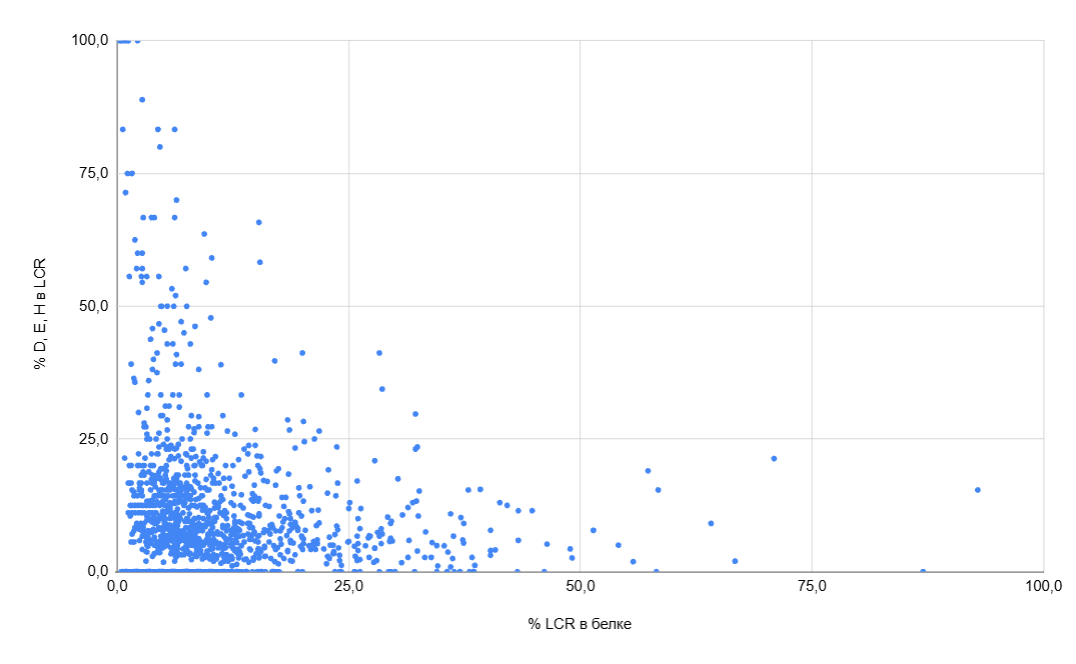
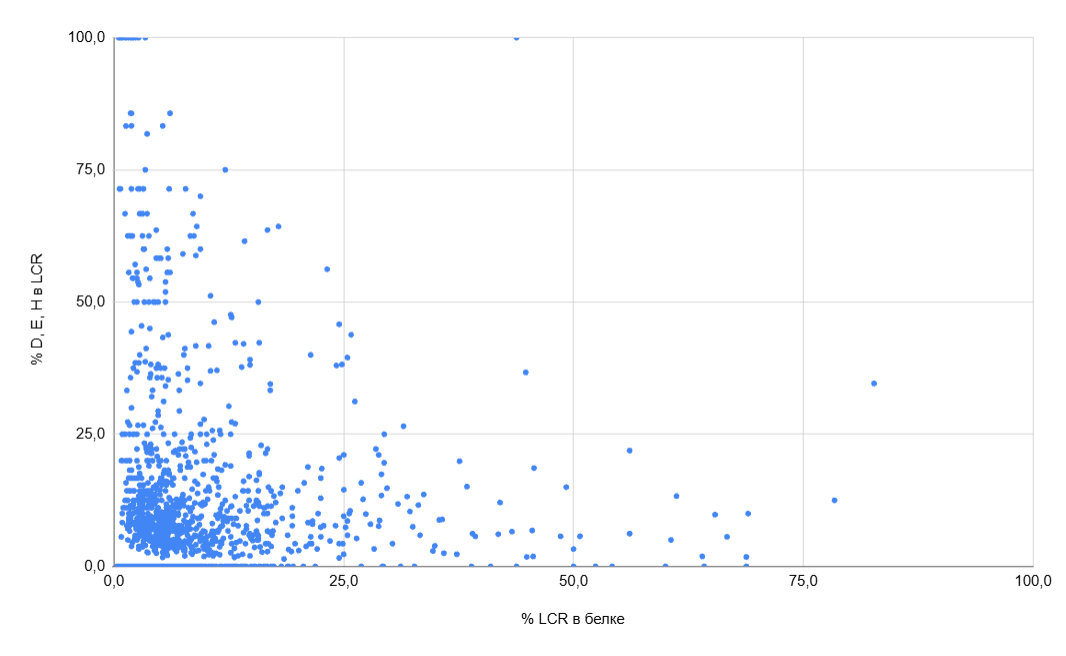
LCR в белках радиационно-устойчивых прокариот. Были построены диаграммы распределения белков по содержанию LCR и хелатирующих аминокислот в составе LCR для радиационно-устойчивых бактерий Deinococcus radiodurans (рис. 3) и D.geothermalis (рис. 4), для бактерий, обладающих меньшей устойчивостью - Thermus thermophilis (выбрана для сравнения как родственный к Deinococcus вид [18]) (см. С3), Escherichia coli (рис. 5), Shewanella oneidensis (одна из наиболее чувствительных к ИИ бактерий [3]) (см. С3), а также для археи Halobacterium salinarum (рис. 6). Эти диаграммы позволяют сделать несколько выводов:
1. По полученным данным не удаётся выявить паттерны, которые бы позволяли отличить устойчивых к ИИ бактерий от чувствительных по протеому. Это частично согласуется с выводами, сделанными Sghaier et al. [22]. В своей работе они изучали различия в аминокислотном составе белков у радиационно-устойчивых и неустойчивых бактерий и не выявили смещения в сторону хелатирующих аминокислот. Из рассмотренных протеомов значительно отличается от других лишь протеом H.salinarum, что согласуется с уже упомянутыми данными об LCR в белках галоархей.
2. При поиске гомологов белков, которые смещены «вправо» и «вверх» на диаграммах для видов Deinococcus, с помощью Protein BLAST, не выявляются белки, которые имеются у обоих видов и показывают высокое сходство между собой. Следуя идее, высказанной Макаровой et al. [18], можно заключить, что такие белки, вероятно, не вовлечены в устойчивость к ИИ.
Полученные данные не позволяют подтвердить истинность высказанных мной ранее гипотез. Возможно, ключ к разгадке устойчивости видов Deinococcus кроется в пептидах, находящихся сейчас за горизонтом наших возможностей по достоверной аннотации геномов. Недавно Lim et al. предположили, что в D.deserti антиоксидантную функцию выполняют пептиды длиной менее 20 аминокислот, непосредственно кодируемые безлидерными мРНК (lmRNA) [23]. К этой работе, однако, есть вопросы касаемо полученных результатов: авторы приходят к выводу, что эффективность нейтрализации АФК пептидами не зависит от наличия ионов Mn2+, а за антиоксидантную активность отвечают гидрофобные аминокислоты, что почти прямо противоречит результатам более ранних исследований [8]. Вопрос, несомненно, требует дальнейшего изучения.
3. При рассмотрении белков, смещённых «вправо» и «вверх» на диаграмме для H.salinarum, можно выделить несколько белков с неизвестной функцией, которые могут играть важную роль в защите от окислительного и осмотического стресса. Они имеют следующие идентификаторы:
WP_010903074.1, WP_010902209.1, WP_010904223.1, WP_010903006.1, WP_049892509.1, WP_010904068.1, WP_010902128.1, WP_010903035.1
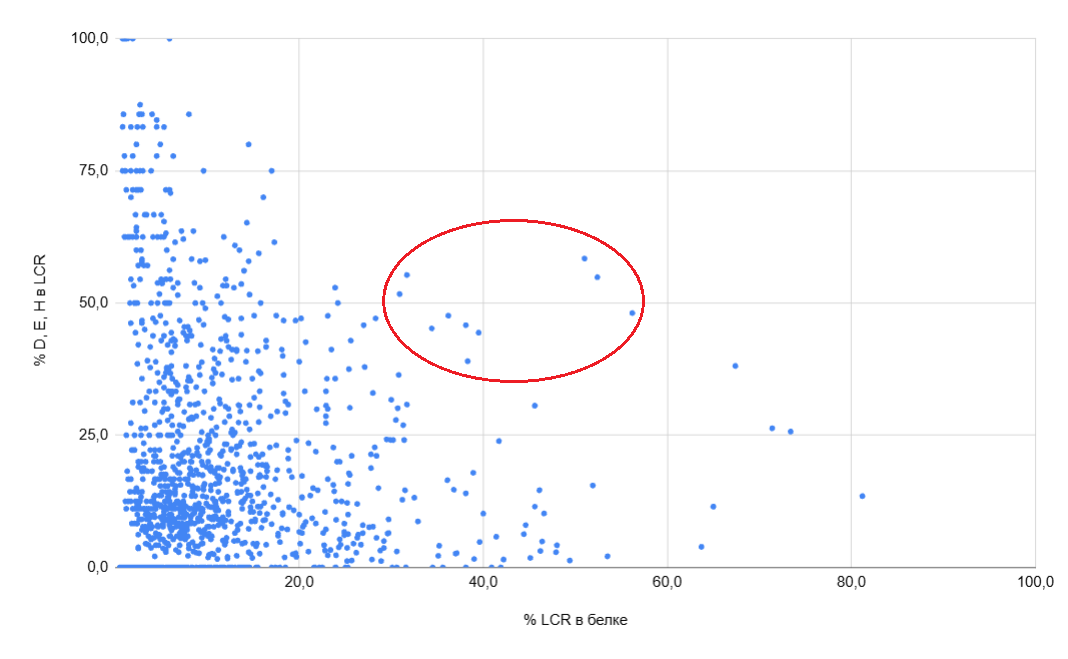
В одной из работ [24], посвящённых роли Mn в устойчивости H.salinarum к ИИ, были получены высоко-устойчивые мутантные линии. Авторы измерили уровни экспрессии генов в этих линиях и предположили, что гены, экспрессия которых была повышена относительно экспрессии в исходной линии, могут быть вовлечены в механизмы устойчивости к ИИ. Гены белков, выбранных ранее на диаграмме, среди них найти не удалось. Это не позволяет подтвердить значимость выбранных белков в защите от ИИ.
Заключение
Проведённый анализ протеомов высоко устойчивых и неустойчивых к ИИ прокариот не подтвердил высказанные гипотезы. Остаётся надеяться, что новые данные позволят прояснить детали механизмов защиты от ИИ.
Сопроводительные материалы
С1. Таблица свойств кодирующих последовательностей и гистограммы.
С2. Код для работы с LCR и пояснения к нему.
C3. Таблицы и диаграммы по LCR для всех рассмотренных организмов (DR - Deinococcus radiodurans, DG - D.geothermalis, TT - Thermus thermophilis, EC - Escherichia coli, SO - Shewanella oneidensis, HS - Halobacterium salinarum).
Список литературы
- Eichler, J. (2023). Halobacterium salinarum: Life with more than a grain of salt. Microbiology, 169(4), 001327.
- Slade, D., & Radman, M. (2011). Oxidative stress resistance in Deinococcus radiodurans. Microbiology and Molecular Biology Reviews, 75(1), 133–191.
- Daly, M. J. (2009). A new perspective on radiation resistance based on Deinococcus radiodurans. Nature Reviews Microbiology, 7(3), 237–245.
- Bruckbauer, S. T., Martin, J., Minkoff, B. B., Veling, M. T., Lancaster, I., Liu, J., ... & Cox, M. M. (2020). Physiology of highly radioresistant Escherichia coli after experimental evolution for 100 cycles of selection. Frontiers in Microbiology, 11, 582590.
- Krisko, A., & Radman, M. (2013). Biology of extreme radiation resistance: the way of Deinococcus radiodurans. Cold Spring Harbor Perspectives in Biology, 5(7), a012765.
- Peana, M., Medici, S., Pangburn, H. A., Lamkin, T. J., Ostrowska, M., Gumienna-Kontecka, E., & Zoroddu, M. A. (2016). Manganese binding to antioxidant peptides involved in extreme radiation resistance in Deinococcus radiodurans. Journal of Inorganic Biochemistry, 164, 49–58.
- He, Y. (2009). High cell density production of Deinococcus radiodurans under optimized conditions. Journal of Industrial Microbiology and Biotechnology, 36(4), 539–546.
- Daly, M. J., Gaidamakova, E. K., Matrosova, V. Y., Kiang, J. G., Fukumoto, R., Lee, D. Y., et al. (2010). Small-molecule antioxidant proteome-shields in Deinococcus radiodurans. PLOS One, 5(9), e12570.
- Mattimore, V., & Battista, J. R. (1996). Radioresistance of Deinococcus radiodurans: functions necessary to survive ionizing radiation are also necessary to survive prolonged desiccation. Journal of Bacteriology, 178(3), 633–637.
- Mohammadipanah, F., & Wink, J. (2016). Actinobacteria from arid and desert habitats: diversity and biological activity. Frontiers in Microbiology, 6, 1541.
- Fendrihan, S., Legat, A., Pfaffenhuemer, M., Gruber, C., Weidler, G., Gerbl, F., & Stan-Lotter, H. (2006). Extremely halophilic archaea and the issue of long-term microbial survival. Reviews in Environmental Science and Bio/Technology, 5(2), 203–218.
- Saralov, A. I., Baslerov, R. V., & Kuznetsov, B. B. (2013). Haloferax chudinovii sp. nov., a halophilic archaeon from Permian potassium salt deposits. Extremophiles, 17(3), 499–504.
- Zerulla, K., & Soppa, J. (2014). Polyploidy in haloarchaea: advantages for growth and survival. Frontiers in Microbiology, 5, 274.
- Kish, A., Kirkali, G., Robinson, C., Rosenblatt, R., Jaruga, P., Dizdaroglu, M., & DiRuggiero, J. (2009). Salt shield: intracellular salts provide cellular protection against ionizing radiation in the halophilic archaeon, Halobacterium salinarum NRC‐1. Environmental Microbiology, 11(5), 1066–1078.
- Ng, W. V., Kennedy, S. P., Mahairas, G. G., Berquist, B., Pan, M., Shukla, H. D., et al. (2000). Genome sequence of Halobacterium species NRC-1. Proceedings of the National Academy of Sciences, 97(22), 12176–12181.
- Frolow, F., Harell, M., Sussman, J. L., Mevarech, M., & Shoham, M. (1996). Insights into protein adaptation to a saturated salt environment from the crystal structure of a halophilic 2Fe-2S ferredoxin. Nature Structural Biology, 3(5), 452–458.
- Ntountoumi, C., Vlastaridis, P., Mossialos, D., Stathopoulos, C., Iliopoulos, I., Promponas, et al. (2019). Low complexity regions in the proteins of prokaryotes perform important functional roles and are highly conserved. Nucleic Acids Research, 47(19), 9998–10009.
- Makarova, K. S., Omelchenko, M. V., Gaidamakova, E. K., Matrosova, V. Y., Vasilenko, A., Zhai, M., et al. (2007). Deinococcus geothermalis: the pool of extreme radiation resistance genes shrinks. PLOS One, 2(9), e955.
- Harrison, P. M. (2017). fLPS: Fast discovery of compositional biases for the protein universe. BMC Bioinformatics, 18(1), 476.
- Harrison, P. M. (2021). fLPS 2.0: rapid annotation of compositionally-biased regions in biological sequences. PeerJ, 9, e12363.
- Harrison, P. M. (2024). Optimizing strategy for the discovery of compositionally-biased or low-complexity regions in proteins. Scientific Reports, 14(1), 680.
- Sghaier, H., Thorvaldsen, S., & Saied, N. M. (2013). There are more small amino acids and fewer aromatic rings in proteins of ionizing radiation-resistant bacteria. Annals of Microbiology, 63(4), 1483–1491.
- Lim, S., Song, H. Y., Park, H. R., & Ahn, K. B. (2024). A novel Deinococcus antioxidant peptide mitigates oxidative stress in irradiated CHO-K1 cells. Microorganisms, 12(11), 2161.
- Webb, K. M., Yu, J., Robinson, C. K., Noboru, T., Lee, Y. C., & DiRuggiero, J. (2013). Effects of intracellular Mn on the radiation resistance of the halophilic archaeon Halobacterium salinarum. Extremophiles, 17(3), 485–497.