ОБЩАЯ ХАРАКТЕРИСТИКА КОНТАКТОВ
В структуре белка 2WTZ были проанализированы несколько типов внутримолекулярных взаимодействий, имеющих значение для стабилизации пространственной организации белка.
В ходе работы были рассмотрены водородные связи, солевые мостики, наличие или отсутствие дисульфидных связей, а также ароматические взаимодействия между боковыми радикалами аминокислотных остатков.
Для поиска и визуализации контактов использовалась программа PyMOL, позволяющая анализировать межатомные расстояния и получать иллюстрации отдельных взаимодействий в структуре белка.
ВОДОРОДНАЯ СВЯЗЬ, ЗАТРАГИВАЮЩАЯ АТОМЫ ОСТОВА БЕЛКА
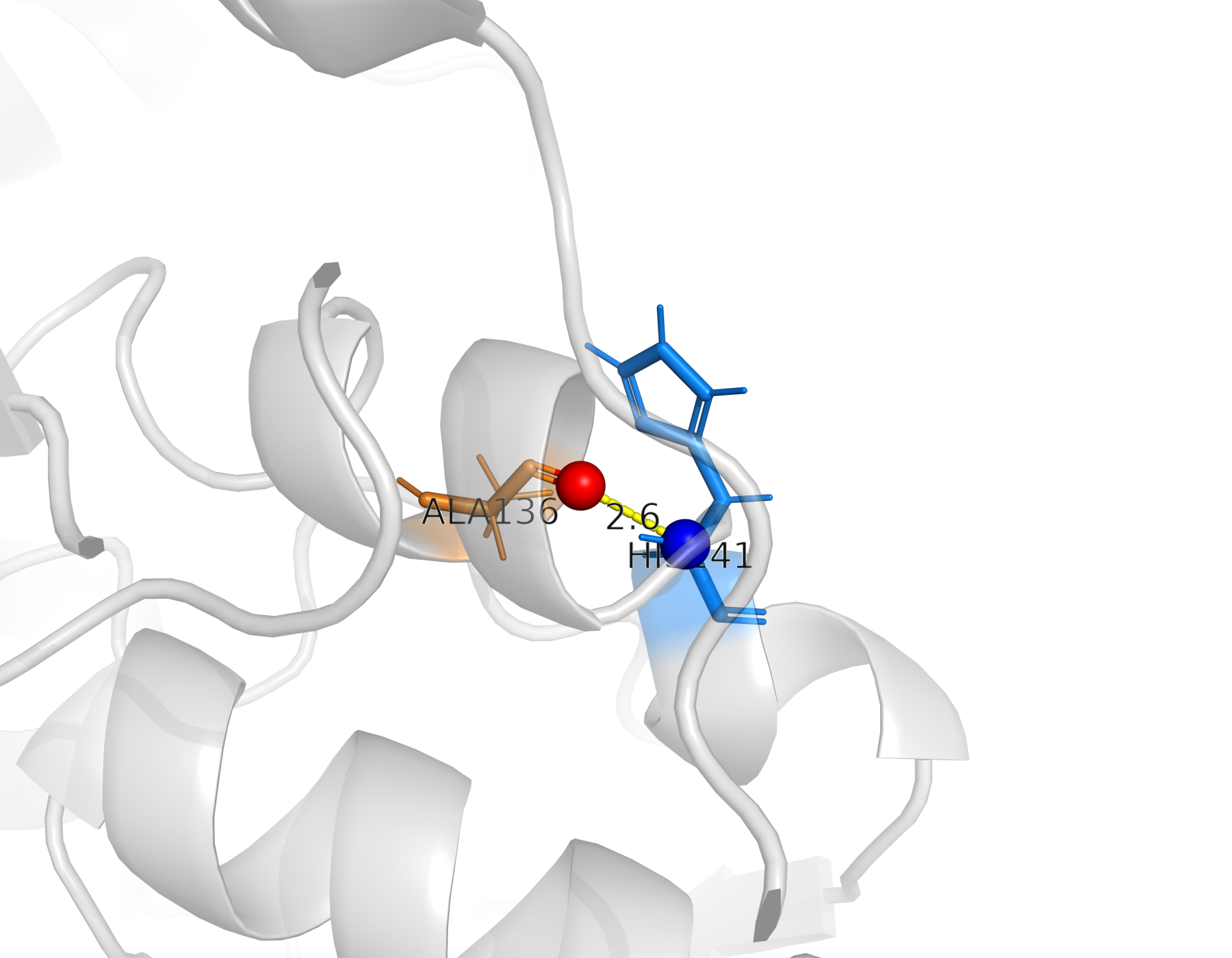
В структуре белка обнаружена водородная связь между атомами остова остатков ALA136 и HIS141.
Контакт образован между карбонильным атомом кислорода остатка ALA136 и амидным атомом азота остатка HIS141. Расстояние между атомами составляет 2.6 Å, что соответствует характерному диапазону для водородных связей в белках.
ВОДОРОДНАЯ СВЯЗЬ МЕЖДУ БОКОВЫМИ РАДИКАЛАМИ АМИНОКИСЛОТ
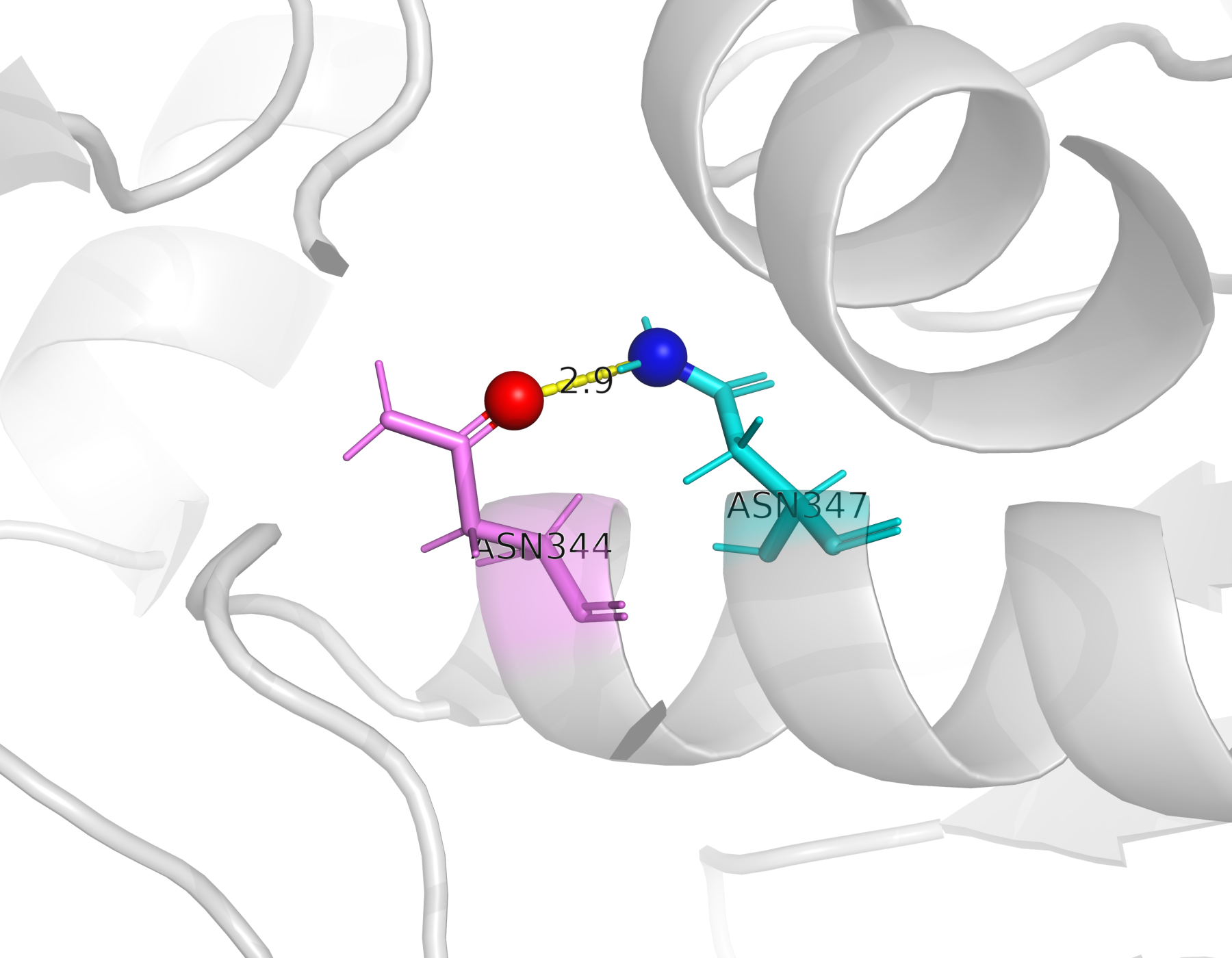
Также была обнаружена водородная связь между боковыми цепями аминокислотных остатков ASN344 и ASN347.
Контакт образован между атомом OD1 остатка ASN344 и атомом ND2 остатка ASN347. Расстояние между взаимодействующими атомами составляет 2.9 Å, что соответствует типичным значениям для водородных связей между боковыми радикалами.
СОЛЕВОЙ МОСТИК
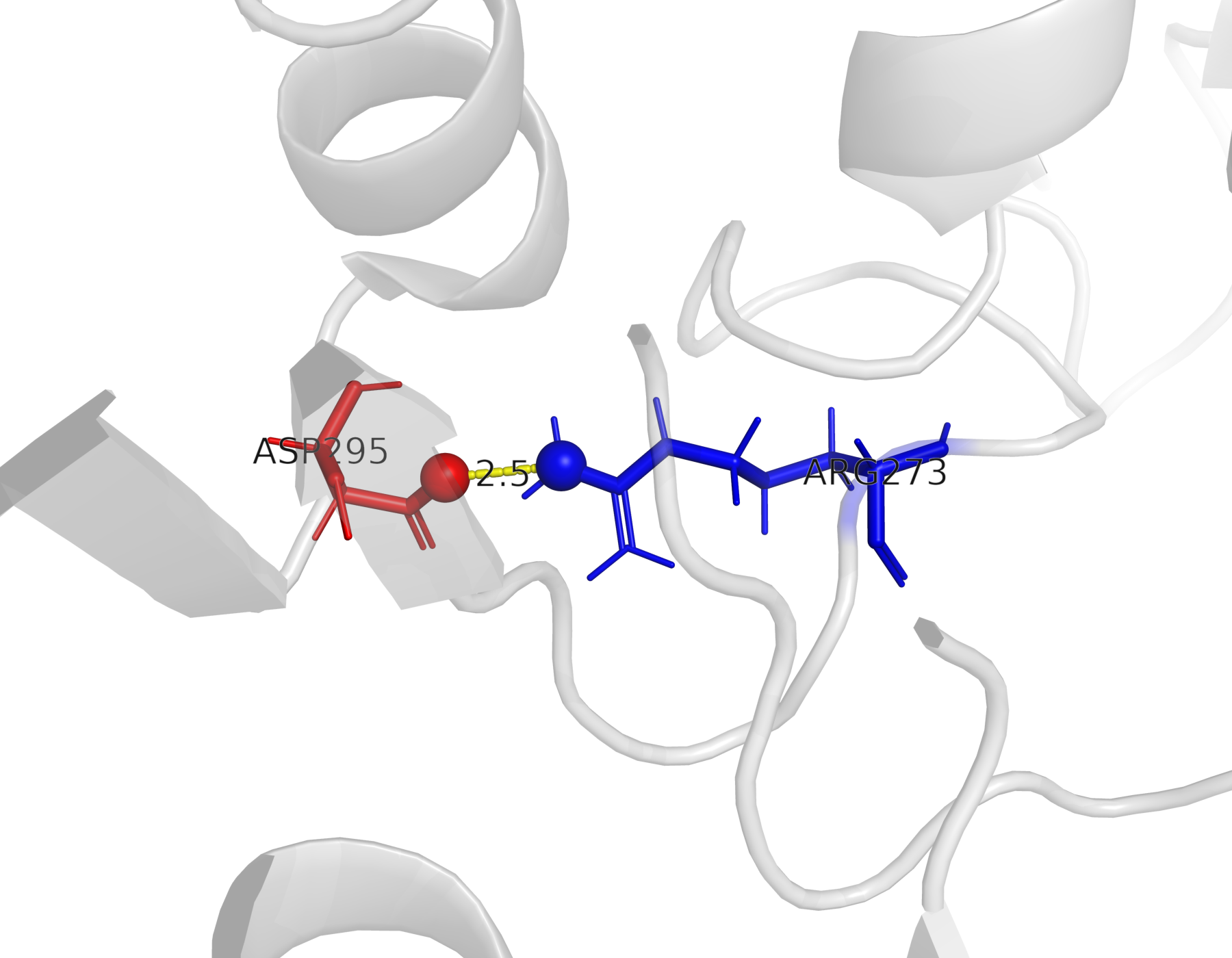
В структуре белка присутствует солевой мостик между положительно заряженным остатком ARG273 и отрицательно заряженным остатком ASP295.
Контакт образован между атомом NH2 аргинина и атомом OD2 аспартата. Расстояние между атомами составляет 2.5 Å, что соответствует характерным расстояниям для электростатических взаимодействий противоположно заряженных боковых радикалов.
ДИСУЛЬФИДНЫЕ СВЯЗИ
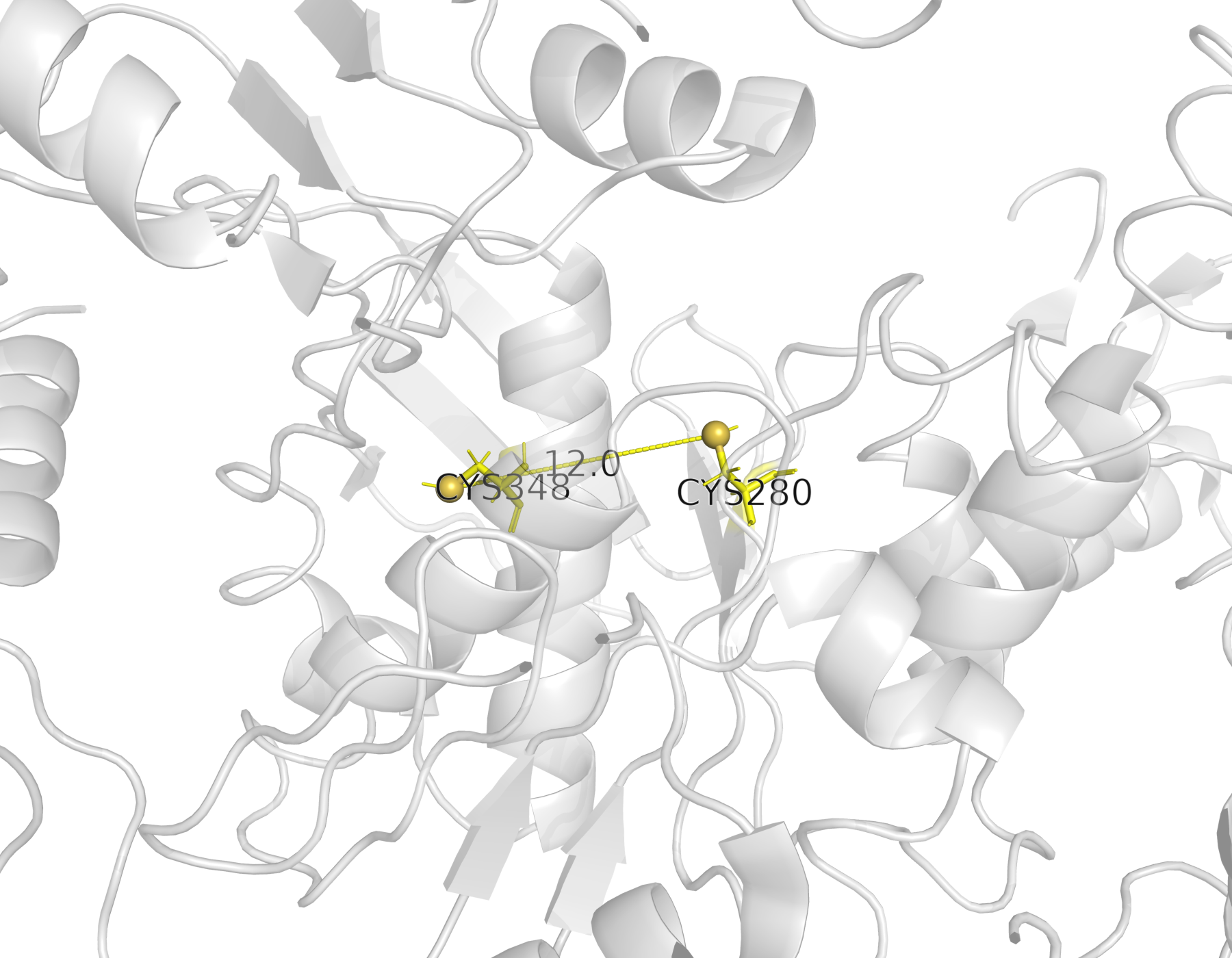
В исследуемой структуре белка дисульфидные связи отсутствуют.
В цепи A присутствуют остатки CYS280 и CYS348, однако расстояние между атомами серы (SG) составляет около 12 Å, что значительно превышает длину дисульфидной связи (~2.05 Å).
Следовательно, ковалентная связь S–S между этими остатками не образуется.
СТЕКИНГ АРОМАТИЧЕСКИХ КОЛЕЦ
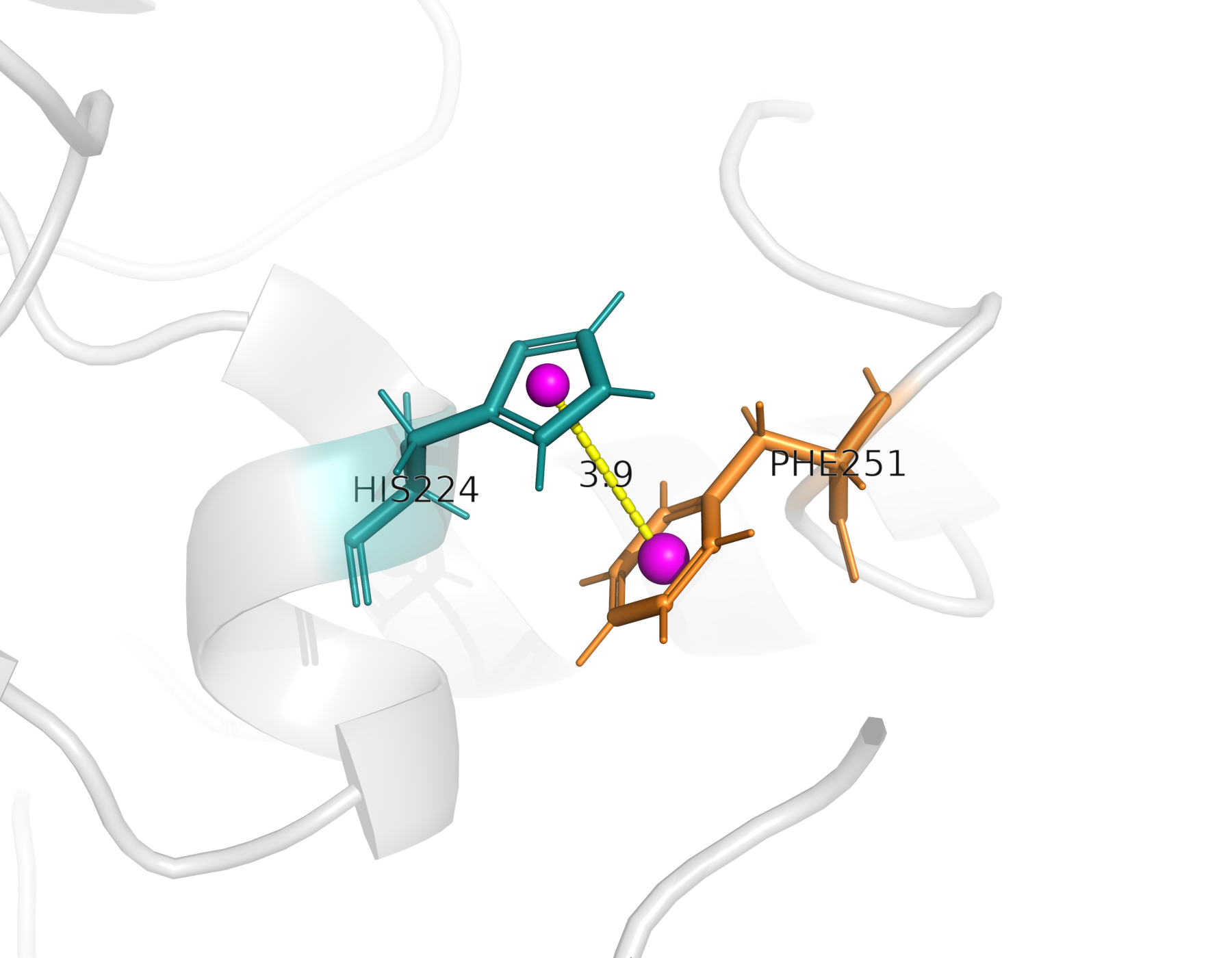
В структуре белка наблюдается ароматическое взаимодействие типа π–π стекинга между остатками HIS224 и PHE251.
Для оценки взаимодействия были определены центры ароматических колец, расстояние между которыми составляет 3.9 Å, что соответствует характерным значениям для ароматических взаимодействий в белках.
ВЫВОД
В структуре белка 2WTZ были проанализированы несколько типов внутримолекулярных контактов, включая водородные связи, солевые мостики, дисульфидные связи и ароматические взаимодействия.
Было показано, что в данной структуре присутствуют как контакты между атомами остова, так и взаимодействия между боковыми радикалами аминокислотных остатков. Дисульфидные связи в исследуемом белке отсутствуют, тогда как ароматические и электростатические взаимодействия вносят вклад в стабилизацию структуры.