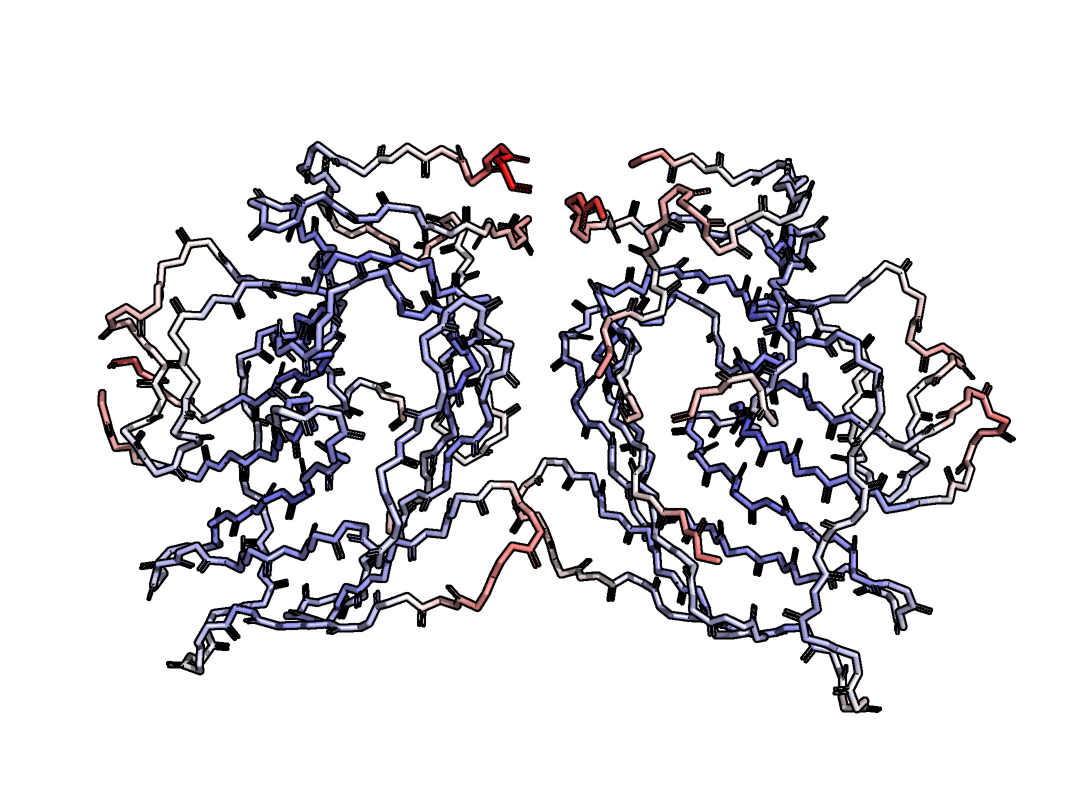
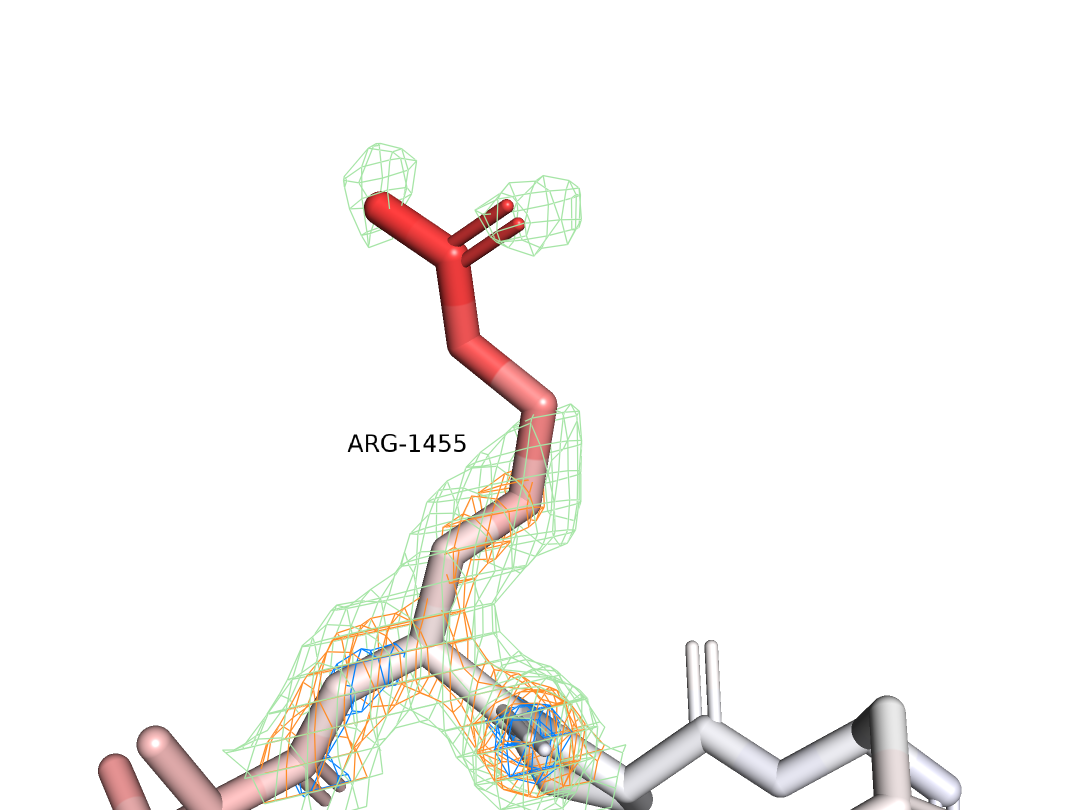
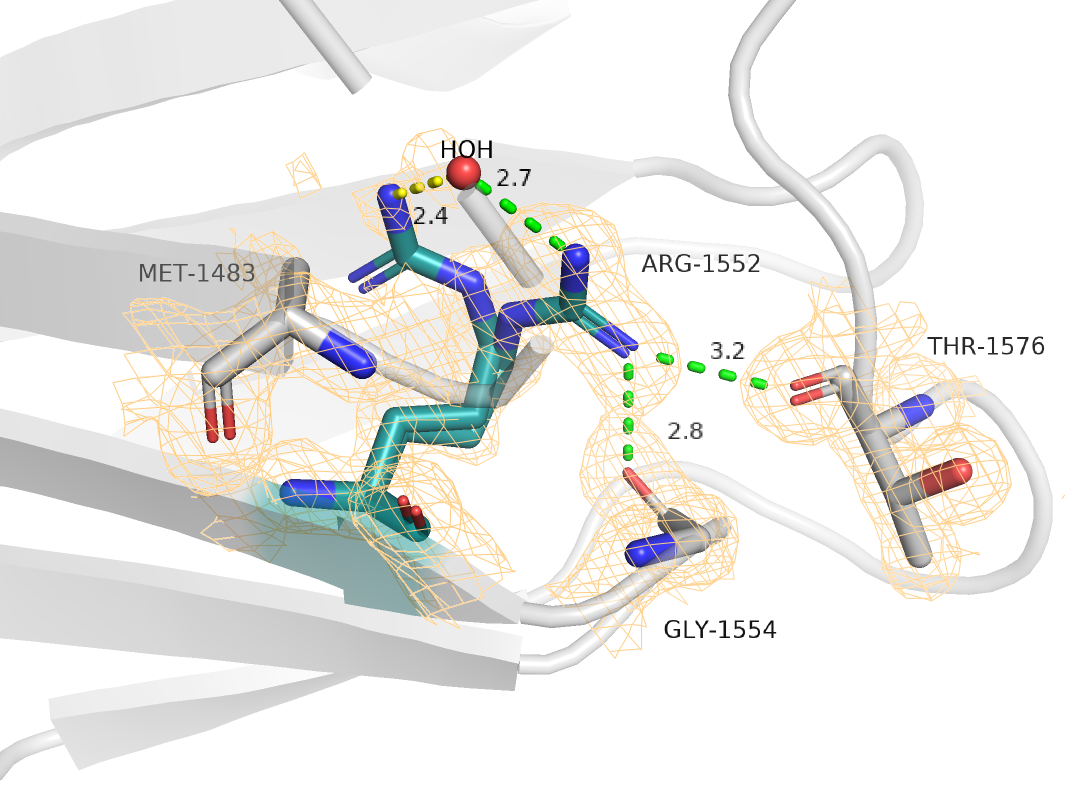
Для первого задания была дана структура 3PVE. В этом задании нам было интересно посмотреть, какие взаимодействия стабилизируют тот или иной альтлок ARG1552 (на B цепи). Рассмотрим сначала альтлок А (Рис.1).

Предполагаю, что он может быть стабилизирован следующими взаимодействиями:
1. водородная связь с HOH143 (dist=2.7, color="yellow")
2. водородная связь с Gly1554 (dist=2.8, color="green")
3. водородная связь с Thr1576 (dist=3.2, color="green")

Как можно увидеть, он стабилизирован следующим:
1. водородная связь с HOH143 (dist=2.4, color="yellow")
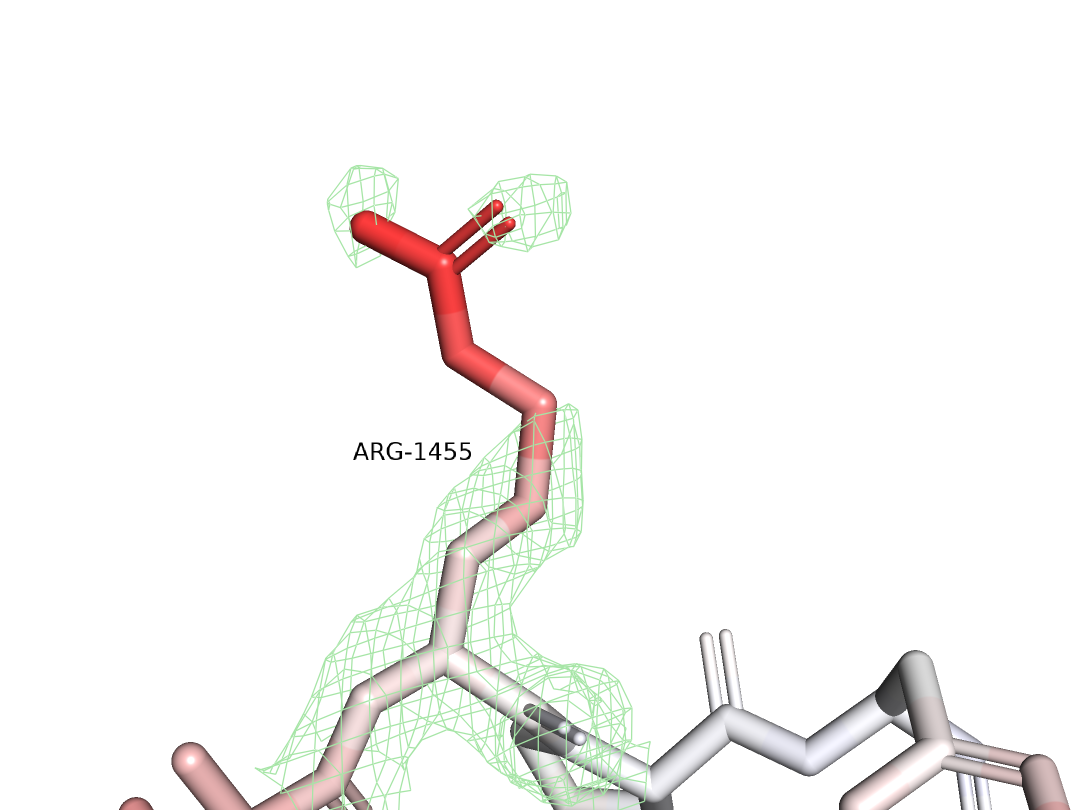
По рисункам видно, что альтлок А стабилизруется 3 взаимодействиями, а альтлок В всего 1, из чего можно предположить, что альтлок А более стабилен.Если заглянуть в PDB файл структуры, то occupancy атомов обоих альтлоков составляет 0,5, что весьма странно, учитывая количество взаимодействий альтлока А. Можно предположить, что это связано с разницей качества взаимодействий: во-первых, у альтлока А остатки, с которыми он взаимодействует находятся дальше (связь слабее), во-вторых, возможно, что углы водородной связи уменьшают ее силу (протоны в PyMol навешиваются случайным образом, поэтому просто сказать, как было на самом деле довольно сложно). Чтобы уточнить этот момент взглянем на электронную плотность (Рис. 3) (взаимодействия альтлока А обозначены зеленым, альтлока В - желтым).
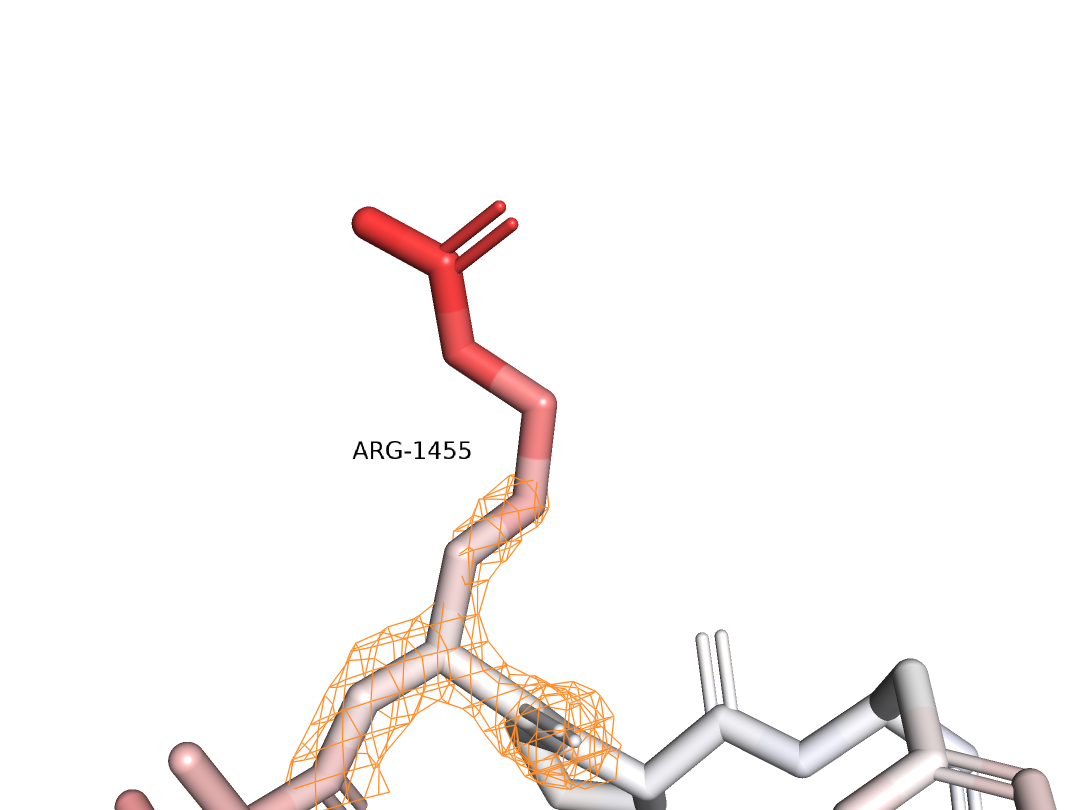
Действительно, можно заметить, что альтлок А имеет связь с Gly1554, а альтлок B с водой, тогда occupancy действительно будет одинаковой. Однако можно заметить, что альтлок В заметно хуже покрыт плотностью. Лучше это можно увидеть при уровне подрезки 3 (Рис. 4).
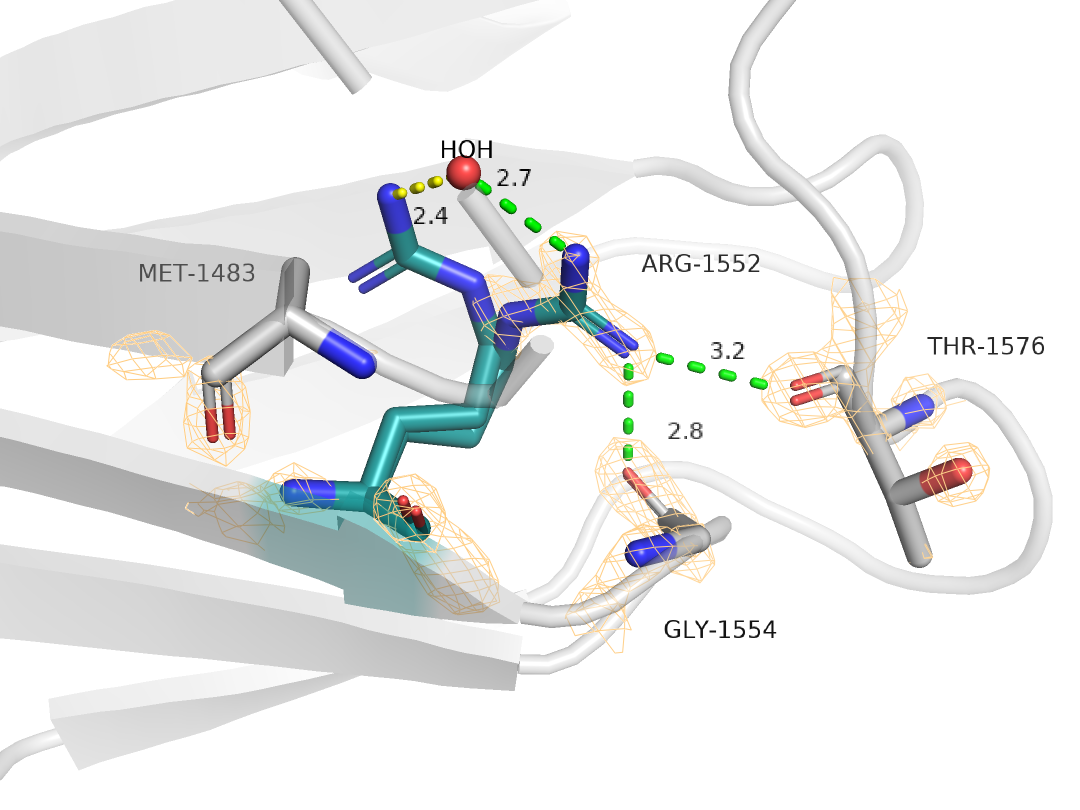
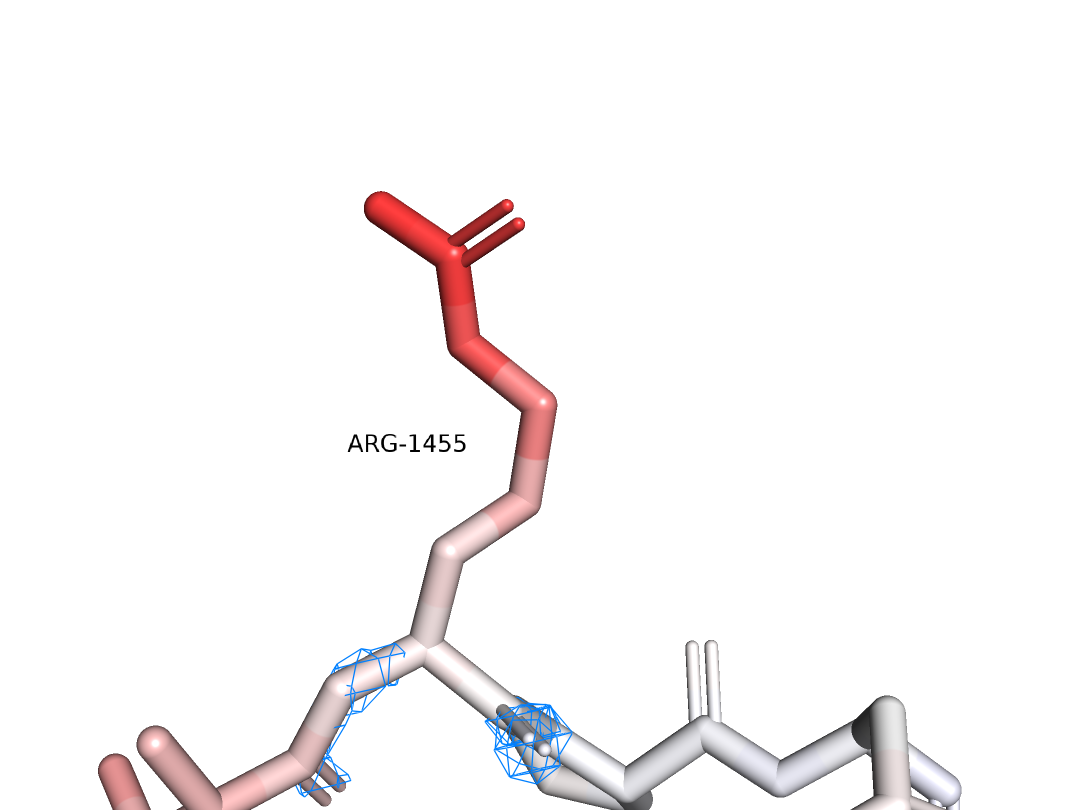
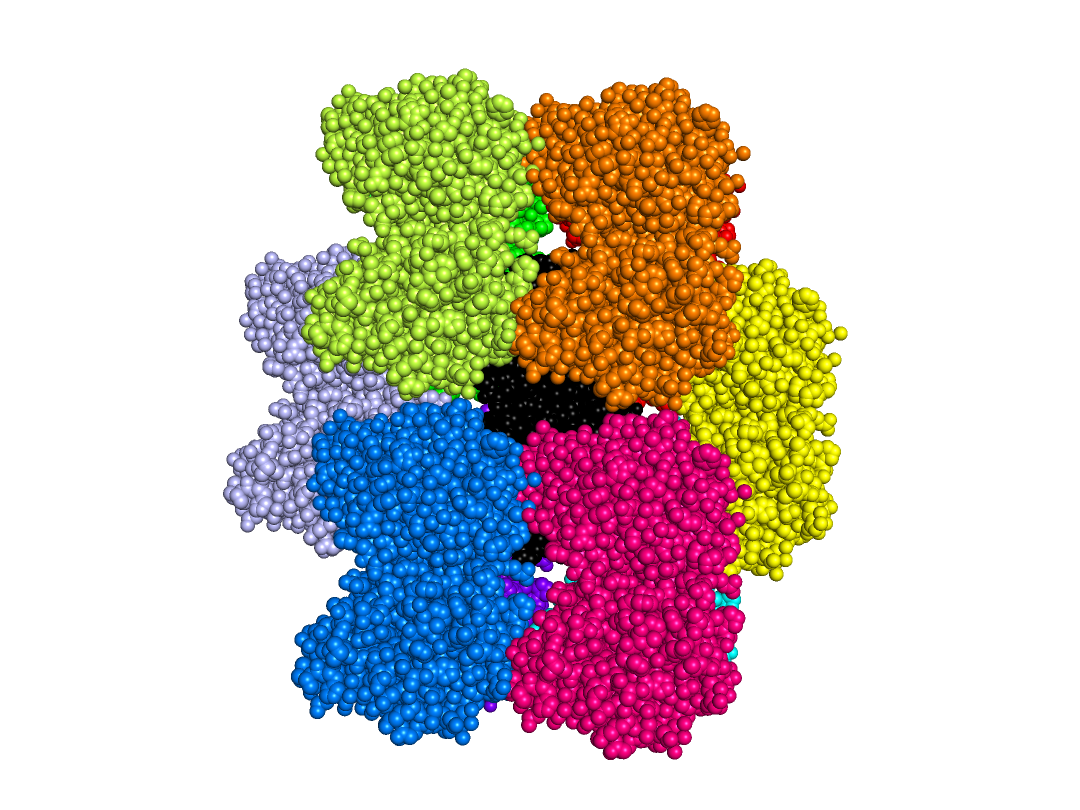
Как видно на рисунке, при таком уровне подрезки альтлок А почти полностью покрыт электронной плотностью, что само по себе странно. Кроме того, если рассмотреть электронную плотность всей структуры (Рис. 5), то можно заметить, что есть кусок плотности (обозначен стрелкой), который может принадлежать радикалу метионина (он тут очень обрезанный) или может быть водой, которая может взаимодействовать с альтлоком В.
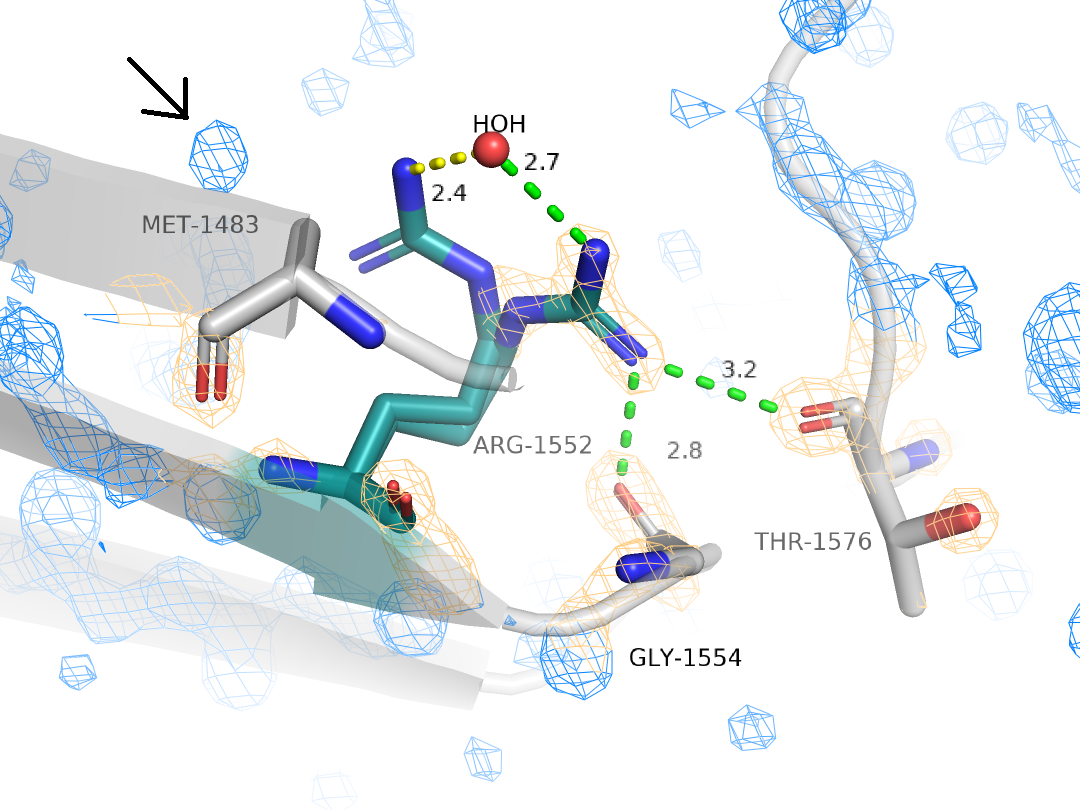
В общем, исходя из полученных данных, я бы все же не согласилась с данными pdb файла и сказала бы, что альтлок А все же более стабильный.