Выдача программы - в файле 1a40.dssp. H отмечены альфа-спирали, E - бета-тяжи.
В таблице ниже сведены данные программы DSSP и данные полей HELIX и SHEET в PDB-файле. Цветом выделены различия в приведенных данных.
| HELIX | SHEET | ||
| DSSP | PDB | DSSP | PDB |
| 13..27 | 13..27 | 3..8 | 3..8 |
| 38..46 | 38..46 | 30..35 | 30..35 |
| 61..67 | 61..67 | 52..55 | 52..55 |
| 97..105 | 97..105 | 69..83 | 69..73, 76..78, 79..83 |
| 114..119 | 114..119 | 94-95 | --- |
| 140..152 | 140..152 | 131..135 | 131..135 |
| 154..159 | 154..159 | 172..174 | 172..174 |
| 176..186 | 176..186 | 190..195 | 190..195 |
| 196..200 | 196..202 | 205-206 | --- |
| 221..227 | 221..228 | 208..210 | --- |
| 267..283 | 267..283 | 216-217 | --- |
| 285..290 | 285..291 | 253..261 | 253..255, 257..261 |
| 298..311 | 298..311 | 263-264 | --- |
| 294-295 | --- | ||
| 313-314 | --- | ||
Видно, что альфа-спирали определены почти одинаково, отличия в 1-2 аминокислотных остатках, без разрывов.
Только 6 бета-тяжей определены одинаково, 7 бета-тяжей были определены DSSP, но не указаны в PDB-файле, остальные в PDB-файле отмечены как отдельные бета-тяжи, программа DSSP определяет их как один.
Скрипт можно посмотреть здесь.

Изображение белка PSTS_ECOLI.
Вторичная структура: альфа-спирали показаны
коричневым цветом, фиолетовым - бета-тяжи,
розовым - остатки, углы &phi которых принимают положительные значения,
зеленым - неструктурные участки.
В файле aa.list перечислены остатки, имеющие положительные значения угла &phi(всего 21).
Как и следовало ожидать, в основном это остатки глицина, при этом все остатки, кроме глицина 77 и 8, расположены в неструктурных участках белка; глицины 77 и 8 попадают в бета-тяжи; также встречаются аспарагиновая(1) и глутаминовая(1) кислоты, аспарагин(3).
hbplus 1a40.pdb
Результат работы программы в файле 1a40.hb2. Файл содержит информацию о доноре, акцепторе электронной пары, длине водородной связи и др.
Примеры водородных связей:
a) стабилизирующих вторичную структуру:выбран участок цепи 1-35. На представленном ниже рисунке изображены водородные связи как в альфа-спирали, так и в бета-тяже.

Участок цепи 1-35.
b)между боковыми цепями аминокислотных остатков

Участок цепи 134-137.
c) между боковой цепью одного остатка и остовным атомом другого

Участок цепи 139-141.
d) между белком и фосфат-ионом(показаны некоторые связи лиганда с белком)
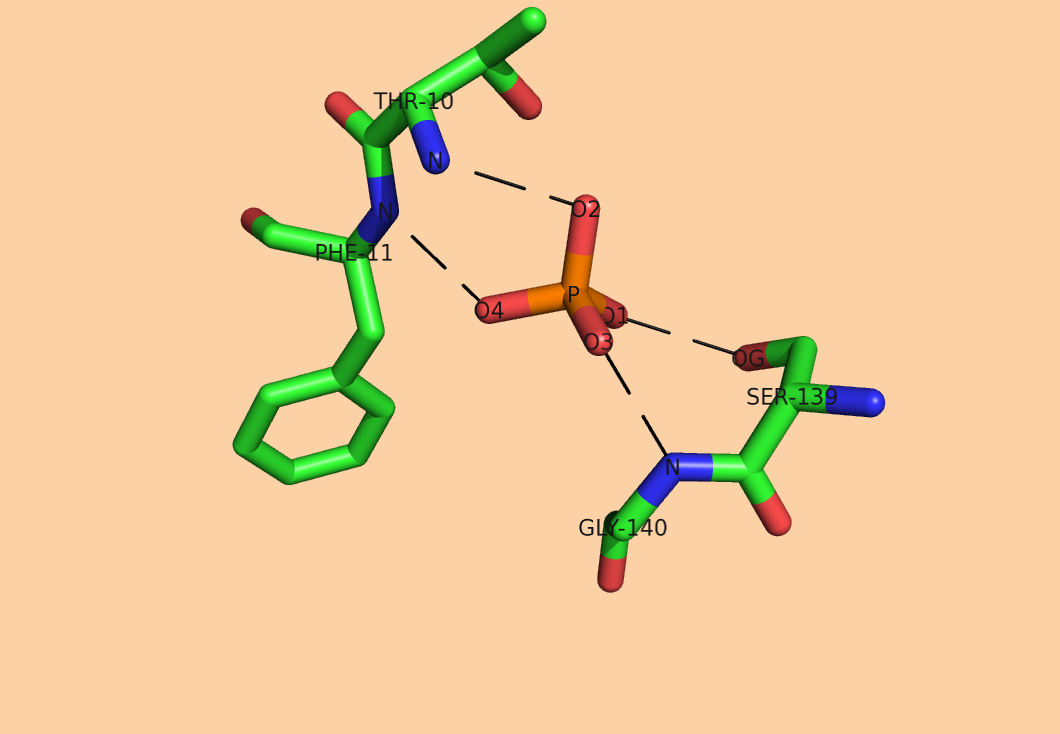
Участок цепи 10-11, 139-140.
e) водяные мостики
