Обзор структуры 7FQW
Структура в целом
7FQW представляет собой мономерный белок, состоящий из одной цепи А, которая включает 321 аминокислотный остаток [1].
Отдельные цепи
Данный белок выделен из организма человека (H. sapiens).
В базе данных PDB идентификатору 7FQW соответствует цепь А тирозин-протеинфосфатазы нерецепторного типа 1 (Tyrosine-protein phosphatase non-receptor type 1, P18031 · PTN1_HUMAN). Она действует как регулятор реакции эндоплазматического ретикулума на неправильное сворачивание белков. Опосредует дефосфорилирование EIF2AK3/PERK, инактивируя протеинкиназную активность EIF2AK3/PERK. Может играть важную роль в каскадах передачи сигналов, индуцированных CKII и p60c-src, и регулировать сигнальный путь EFNA5-EPHA3, который модулирует реорганизацию клеток и межклеточное отталкивание. Также может регулировать сигнальный путь рецептора фактора роста гепатоцитов посредством дефосфорилирования MET [2].
В последовательности из базы данных PDB 7FQW наблюдаются 2 инженерные мутации, отличающие её от референса из базы данных Uniprot (ID P18031).
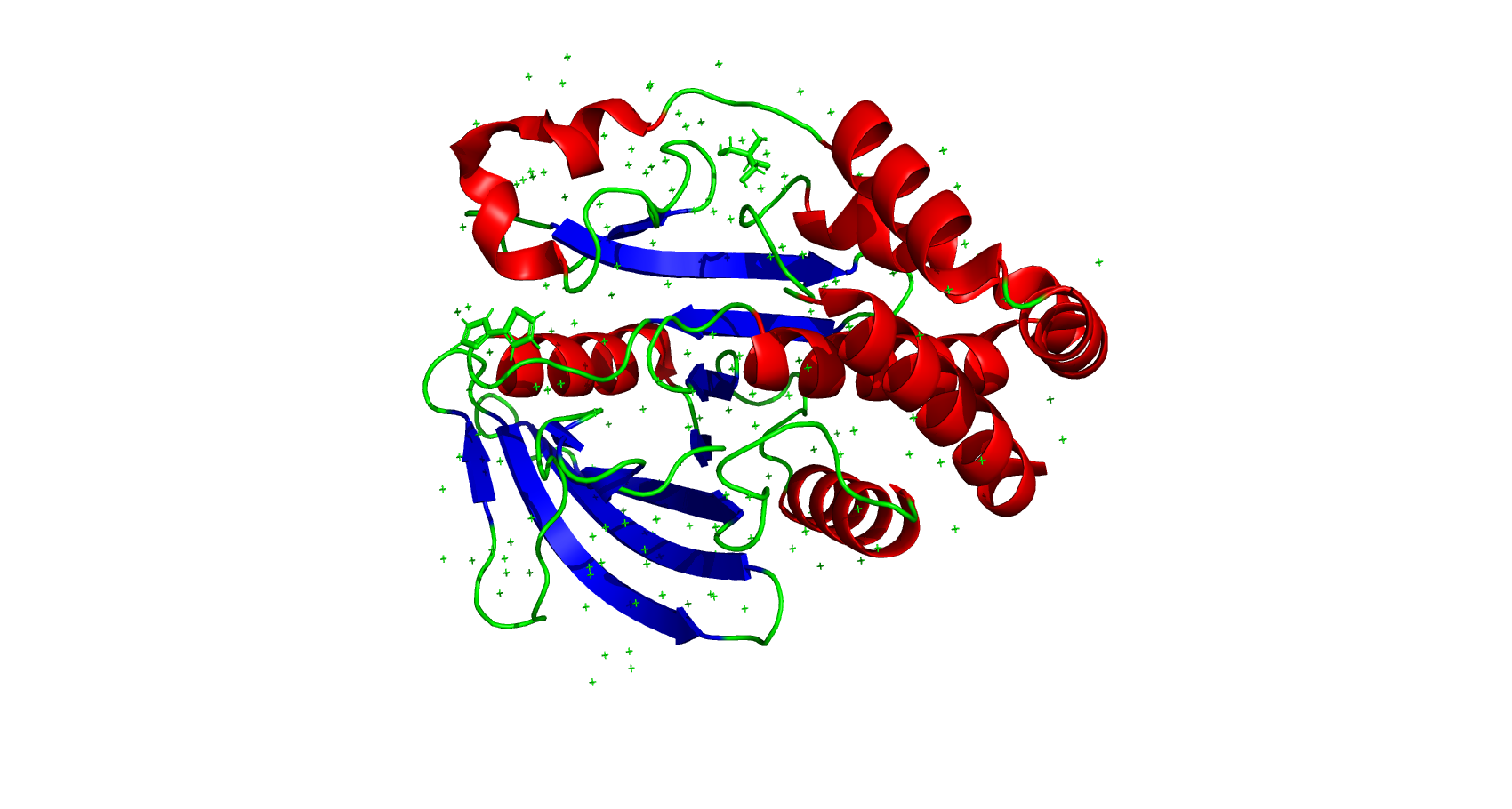
Во вторичной структуре имеются альфа-спирали, бета-тяжи и петли - неупорядоченные участки с первичной структурой (рис.2). При этом заметного преобладания какой-либо из этих структур над остальными не наблюдается.
Малые молекулы
В структуре фермента присутствуют 3 типа малых молекул: 2-(тиофен-2-ил)-1H-имидазол (2-(thiophen-2-yl)-1H-imidazole, JG4) и 2-амино-гидроксиметил-пропан-1,3-диол (2-AMINO-2-HYDROXYMETHYL-PROPANE-1,3-DIOL, TRS), а также молекулы воды (HOH, Water) [1].
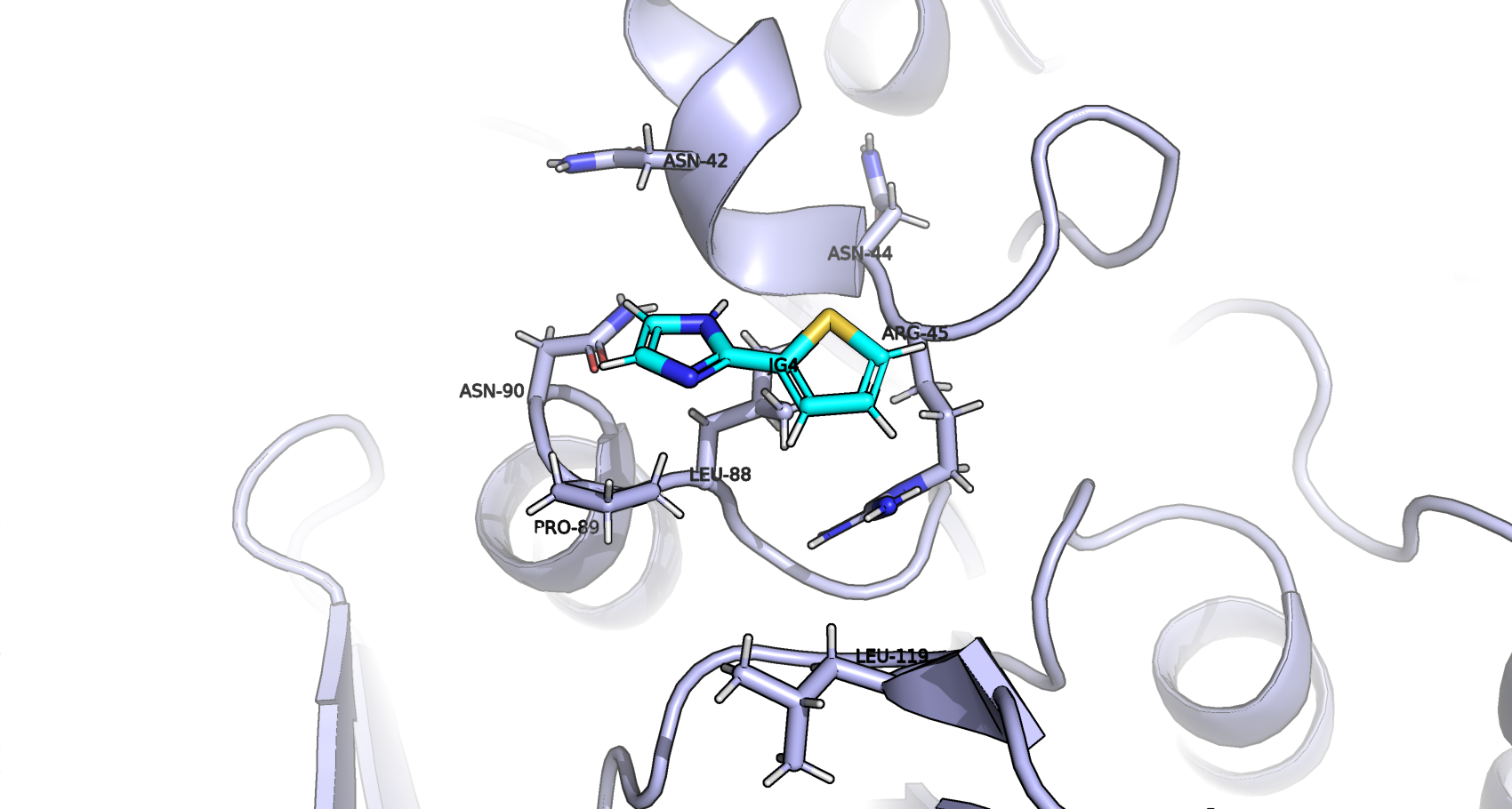
Взаимодействия между аминокислотными остатками
Водородные связи в остове белка (рис.4) образуются между атомом кислорода карбонильной группы одного аминокислотного остатка и атомом азота амидной группы другого остатка в той же цепи. Эти связи стабилизируют вторичную структуру белка (α-спирали, β-листы и т.п.).
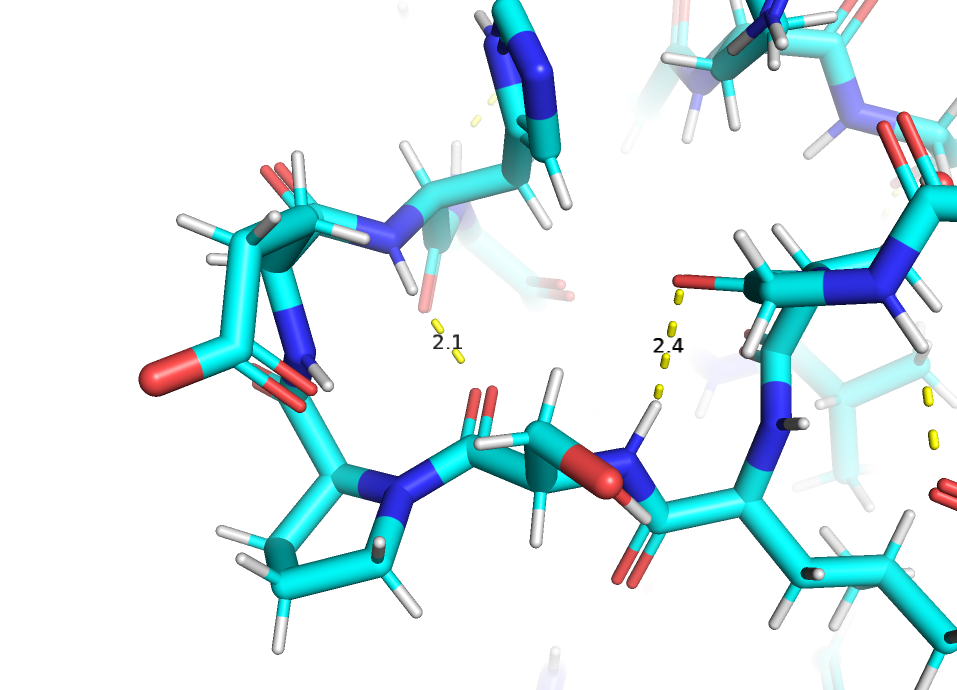
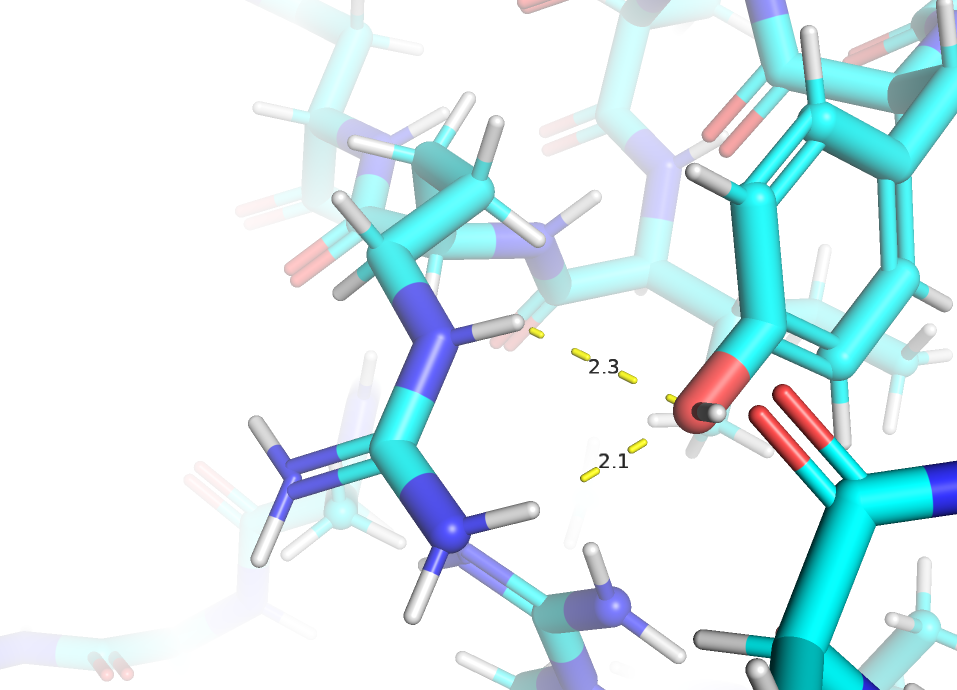
Водородные связи между атомами боковых радикалов аминокислот (рис.5) участвуют в формировании третичной и четвертичной структуры белка, стабилизации вторичной структуры белка, формировании активного центра ферментов и рецепторов.
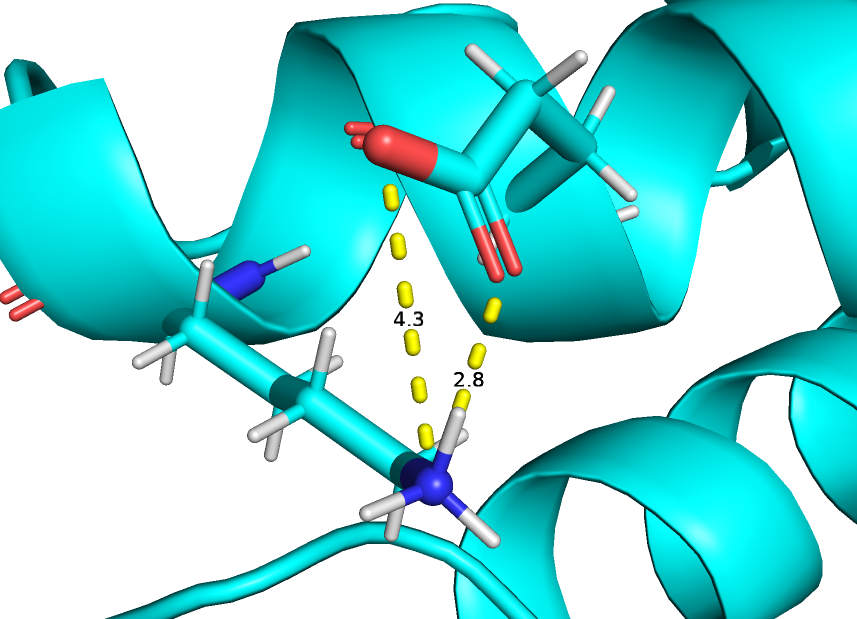
Солевые мостики (рис.6) - это электростатические взаимодействия между положительно и отрицательно заряженными боковыми радикалами аминокислот, которые стабилизруют третичную структуру белка. При физиологическом pH к положительно заряженным аминокислотам относят аргинин и лизин, к отрицательно заряженным аминокислотам - глутаминовую и аспарагиновую кислоту.
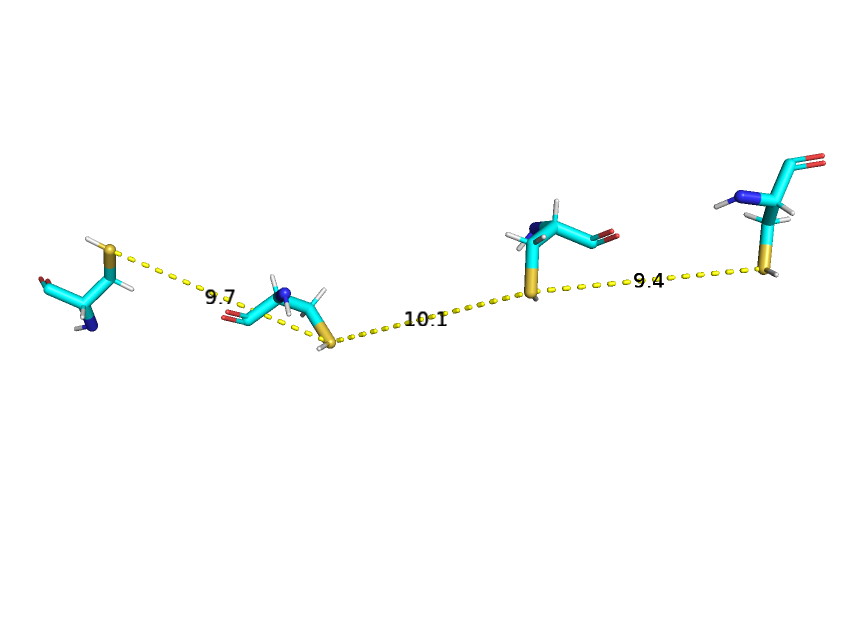
Дисульфидные связи (рис.7) образуются между атомами серы боковых радикалов цистеинов. В белке 7FQW цистеины находятся на расстоянии, превышающем среднюю длину связи в дисульфидном мостике (около 2,05 Å), поэтому в рассматриваемом белке этот тип взаимодействия отсутствует.
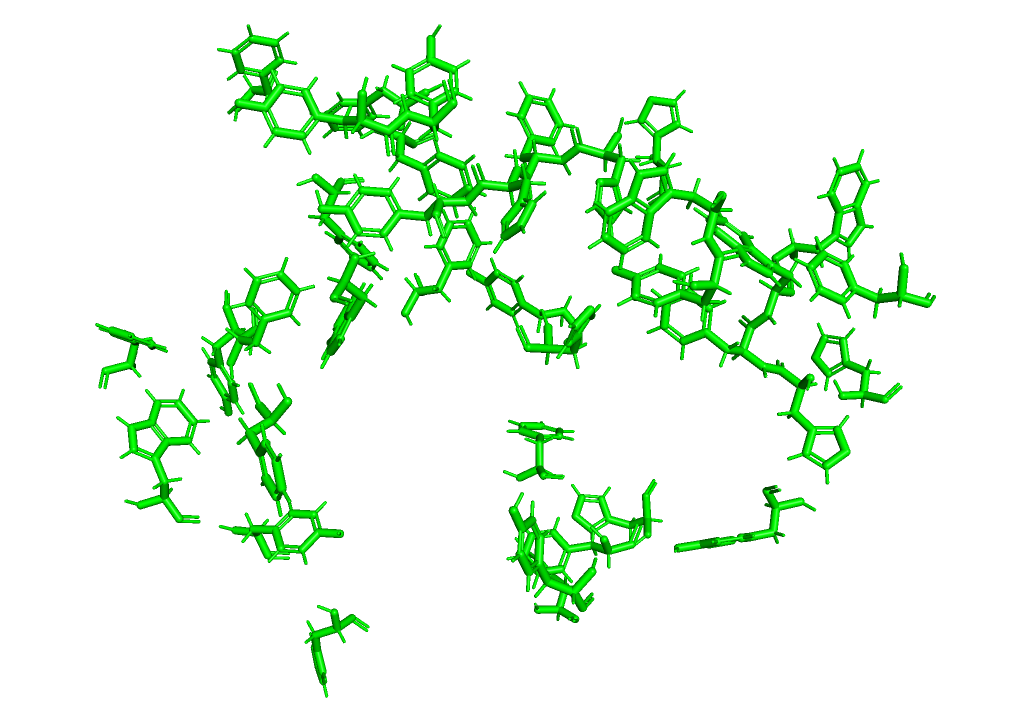
Стекинг-взаимодействия (рис.8) между ароматическими p-сопряженными системами боковых цепей аминокислот стабилизируют вторичную и третичную структуру, могут участвовать в формировании активного центра фермента или рецептора. В исследуемом белке такие взаимодействия не были обнаружены.
Список литературы
[1] https://www.rcsb.org/structure/7FQW
[2] UniProt Consortium. (2024). P18031 · PTN1_HUMAN. UniProt. https://www.uniprot.org/uniprotkb/P18031/entry