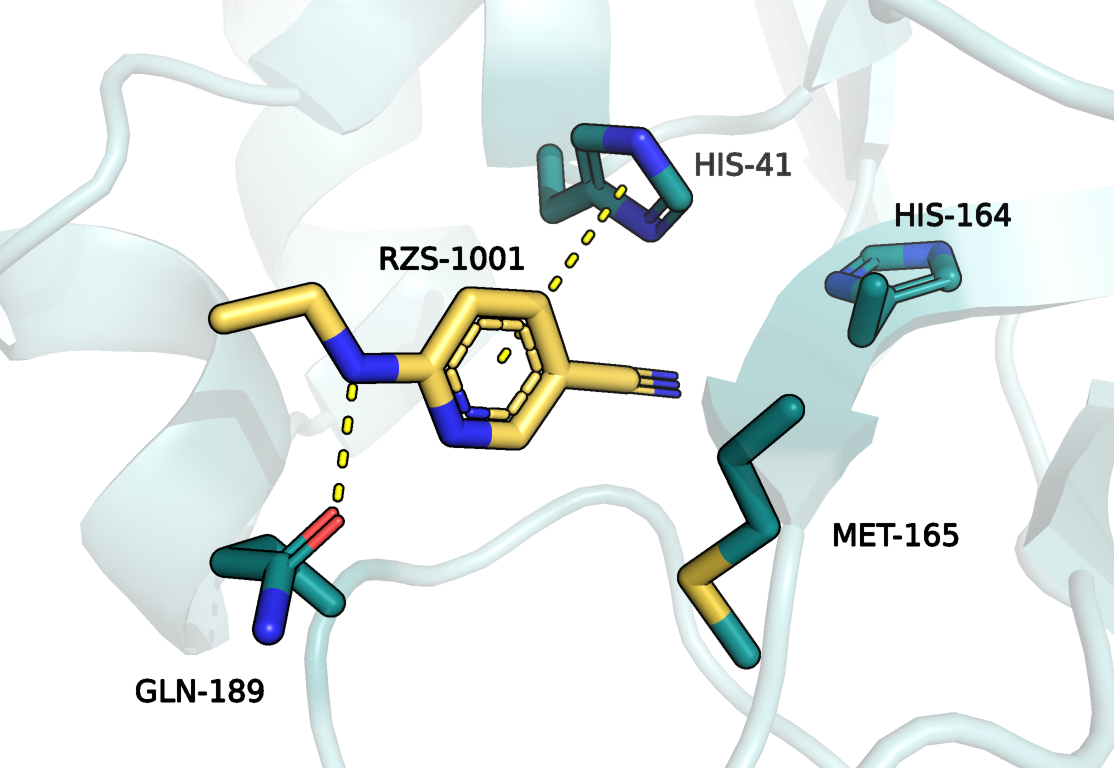
Атомы, выделенные синим - азот, красным - кислород, желтым в составе MET-165 - сера.
Для работы нам был дан PDB ID (5R82) структуры,
полученной в ходе работы консорциума PanDDA над
способами связывания низкомолекулярных фрагментов с главной протеазой коронавируса Sars-COV-2.
Нашей задачей было показать фрагмент и окружающие остатки так, чтобы было понятно где он
располагается и с чем потенциально взаимодействует.
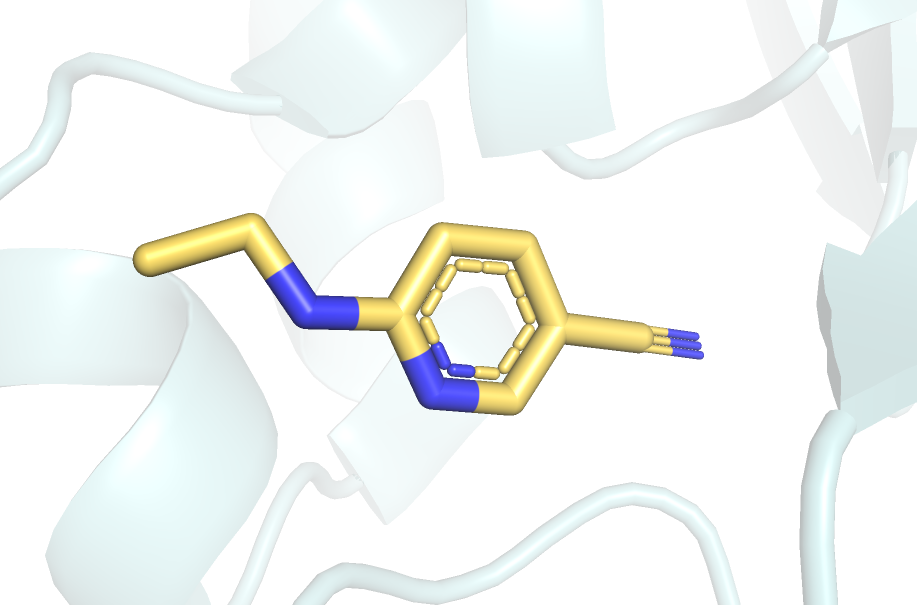
Лиганд RZS - 6-(ethylamino)pyridine-3-carbonitrile.
Он образует водородную связь с глутамином (GLN-189),
а также происходит стэкинг-взаимодействия с гистидином (HIS-41).
Сессия в PyMOL.

Атомы, выделенные синим - азот, красным - кислород, желтым в составе MET-165 - сера.
В этом задании нам были даны два PDB ID, которые соответствуют двум
кристаллографическим расшифровкам одного и того же белка, однако с различным качеством.
В целом, данные структуры не сильно отличаются. Но сразу видно, что у 2H5C большое
количество сульфат-ионов, которых нет у 1GBI.
Далее, с помощью mesh были изучены карты электронной плотности данных структур.
На рисунках 2 и 3 представлены обе плотности: у 2H5C хорошо видны формы атомов, в отличие от 1GBI.
Отсюда можно сделать вывод, что разрешение первой структуры хорошее, а второй - плохое.
Также можно предположить, что структура 1GBI получена раньше,
чем 2H5C, что и сказывается на разрешении.
И данные выводы подтверждаются информацией с сайта RCSB:
1GBI имеет разрешение 2.30 ангстрем и загружен в 1996 (!) году,
тогда как 2H5C имеет разрешение 0.82 ангстрем и загружен в 2006 году.
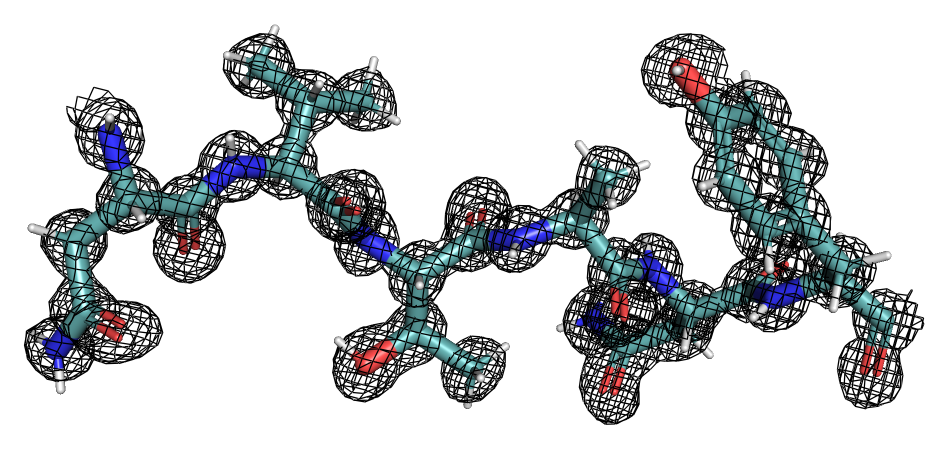
Атомы, выделенные синим - азот, красным - кислород. Уровень подрезки 1, carve = 1. |
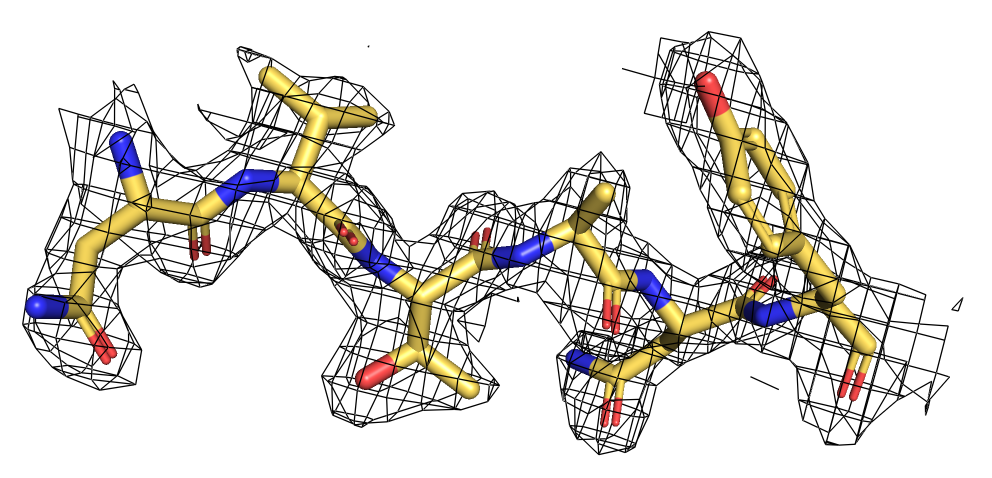
Атомы, выделенные синим - азот, красным - кислород. Уровень подрезки 1, carve = 1.5. |
Здесь нам нужно было взять белок из задания 1 (PDB ID 5R82)
и построить электронную плотность вокруг всего остова с разным уровнем подрезки (1, 2, 3).
При изменении уровня подрезки некоторые области структуры перестают быть покрытыми электронной плотностью:
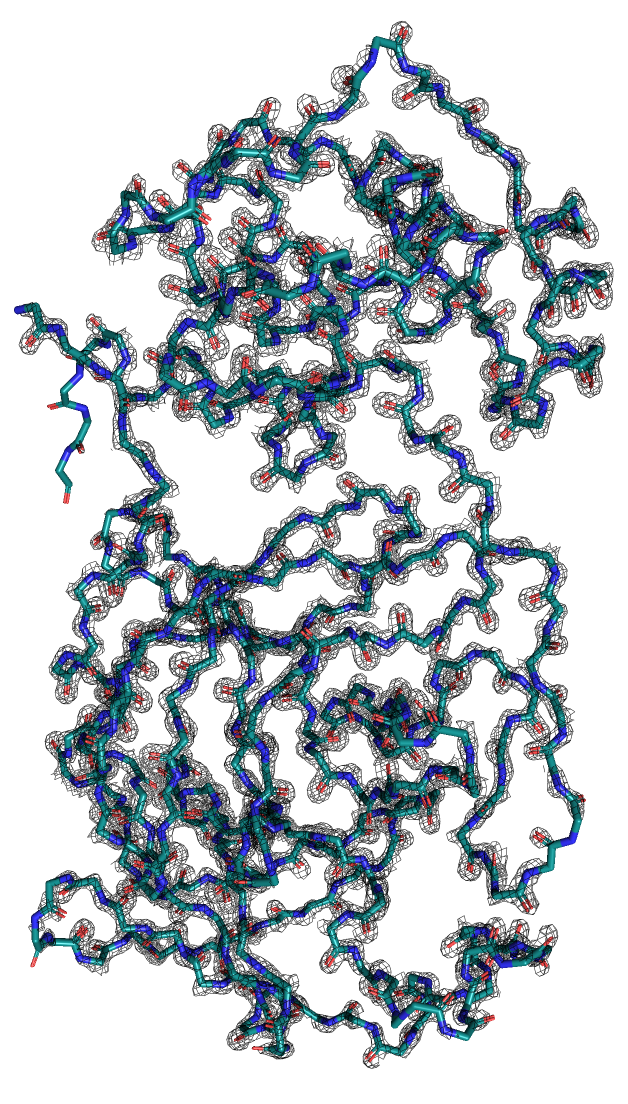
На уровне подрезки 1 (рисунок 4) ЭП окружает весь остов белка.
На уровне подрезки 2 (рисунок 5) ЭП "уходит" с более подвижных регионов (менее структурированные части).
На уровне подрезки 3 (рисунок 6) ЭП остается в основном вокруг атомов кислорода.
Таким образом, можно сделать вывод, что "исчезание" ЭП связано с подвижностью молекул
и отдалении от центра белка, а также с электроотрицательностью
(чем более ЭО атом, тем дольше сохраняется ЭП).

остова белка (PDB ID 5R82). Атомы, выделенные синим - азот, красным - кислород. Уровень подрезки 1, carve = 1.5. |
остова белка (PDB ID 5R82). Атомы, выделенные синим - азот, красным - кислород. Уровень подрезки 2, carve = 1. |
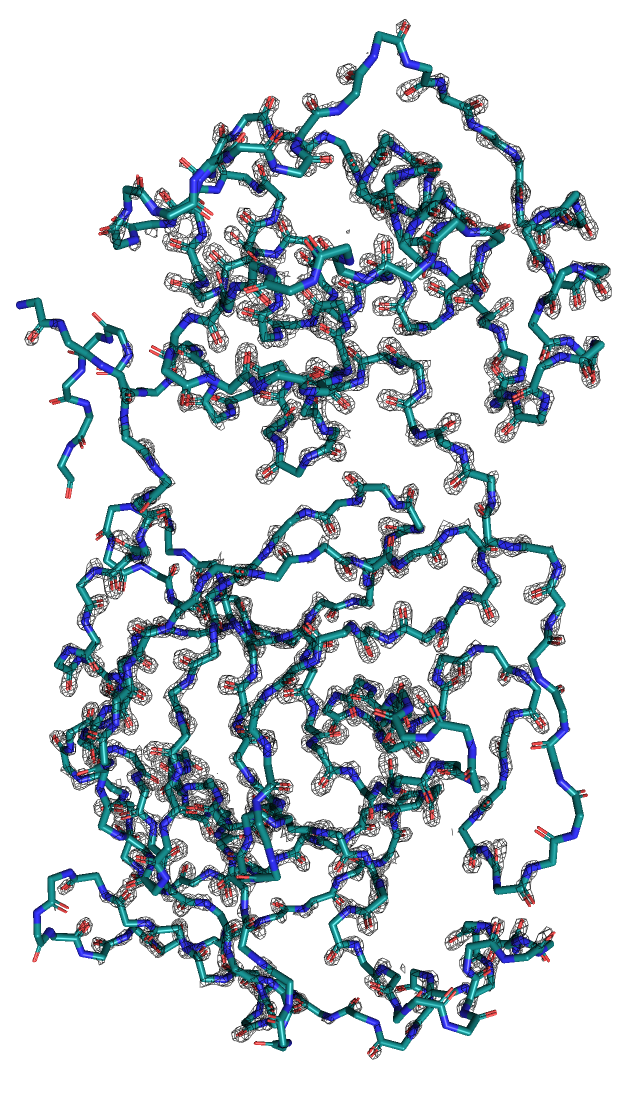
остова белка (PDB ID 5R82). Атомы, выделенные синим - азот, красным - кислород. Уровень подрезки 3, carve = 1. |
В данном задании нам было нужно построить электронную плотность вокруг
лиганда из 1 задания с изменением уровней подрезки (1, 2, 3).
На уровне подрезки 1 (рисунок 8) ЭП окружает в основном области атомов азота.
На уровне подрезки 2 (рисунок 9) ЭП остается только в небольшой отдельной области.
На уровне подрезки 3 (рисунок 10) ЭП "исчезает" полностью.
Такое быстрое "исчезание" ЭП происходит из-за того, что в составе лиганда есть атомы азота, но нет
атомов кислорода или серы (которые более электроотрицательны и дольше сохраняют ЭП при подрезке).
Так как ЭП очень быстро исчезла, было сделано еще одно изображение с уровнем подрезки 0.5 (рисунок 7).
Тут хорошо видно ЭП, охватывающую практически весь лиганд.
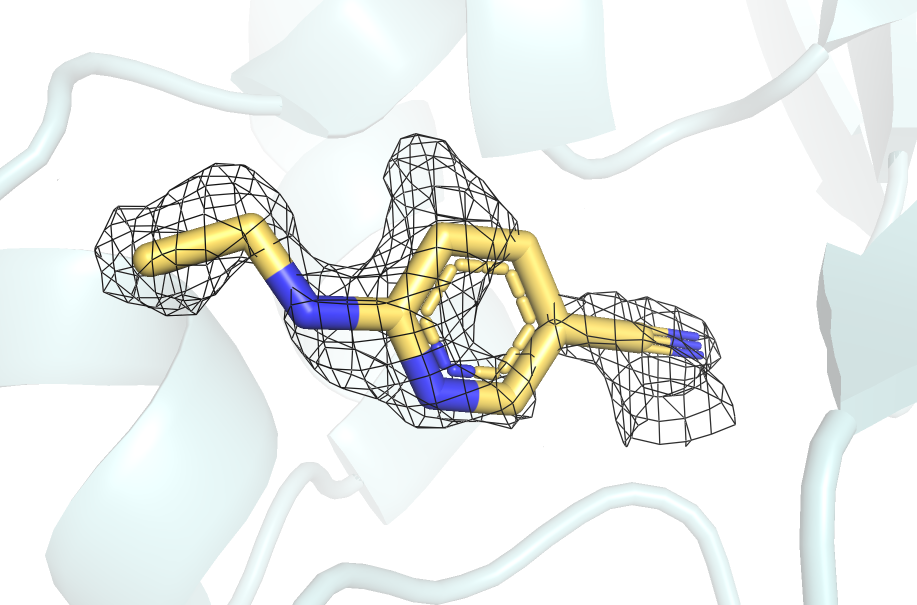
Атомы, выделенные синим - азот. Уровень подрезки 0.5, carve = 2. |
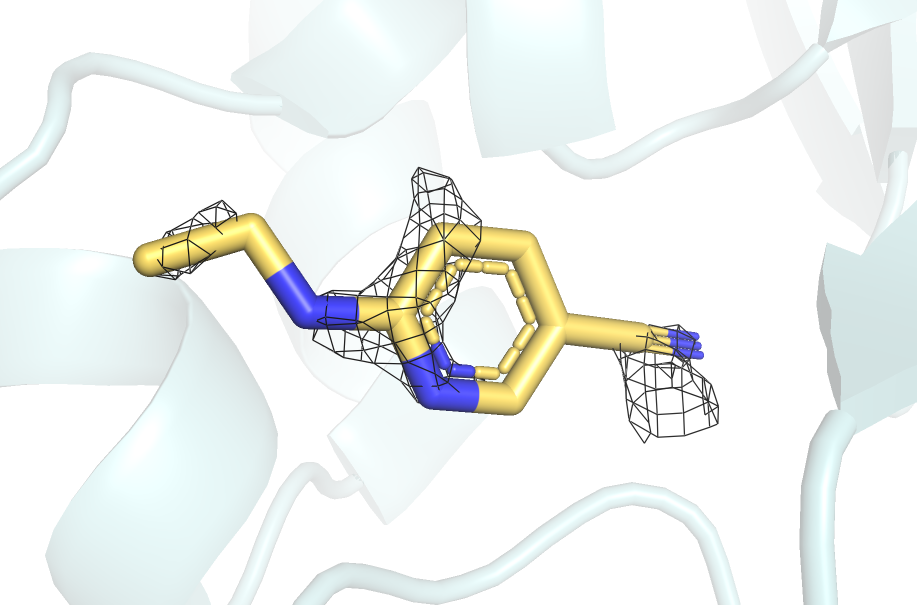
Атомы, выделенные синим - азот. Уровень подрезки 1, carve = 2. |
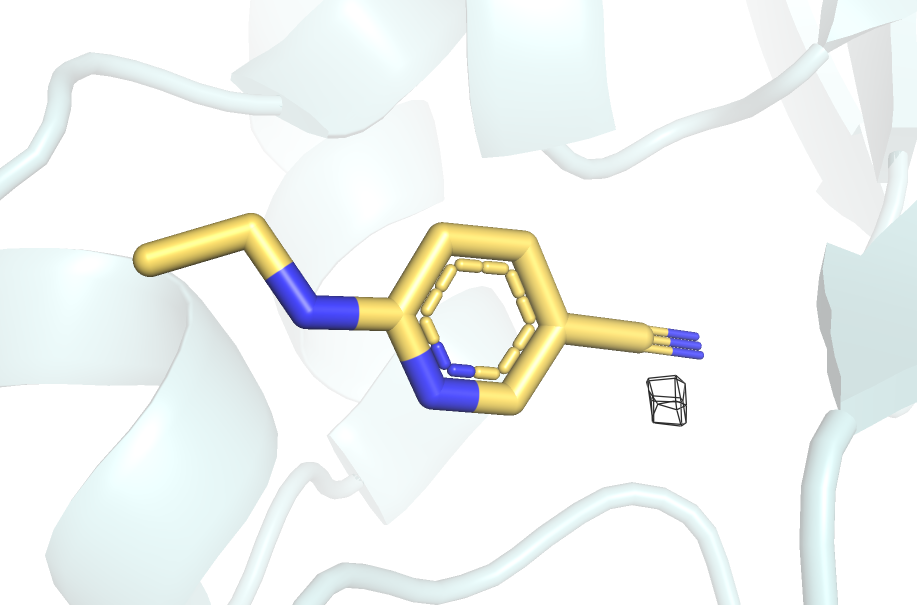
Атомы, выделенные синим - азот. Уровень подрезки 2, carve = 2. |
Атомы, выделенные синим - азот. Уровень подрезки 3, carve = 2. |
© Наумова Юлия, 2020