Задание 1. Альтернативные положения.
Вот изображения, которое мне удалось получить:
альтернативные конформации А и В белка 4AF8:
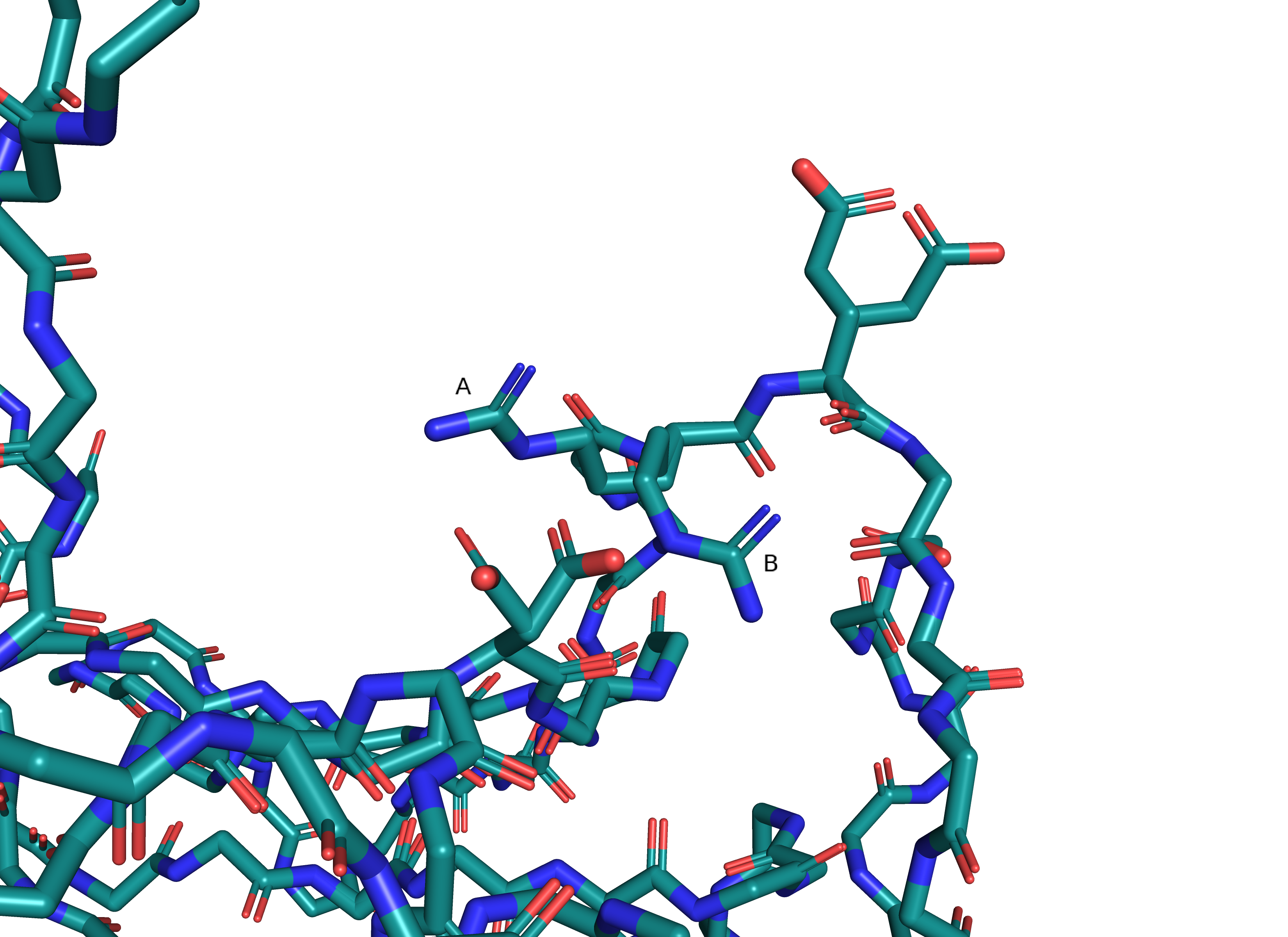
| конформация А: | конформация В: |
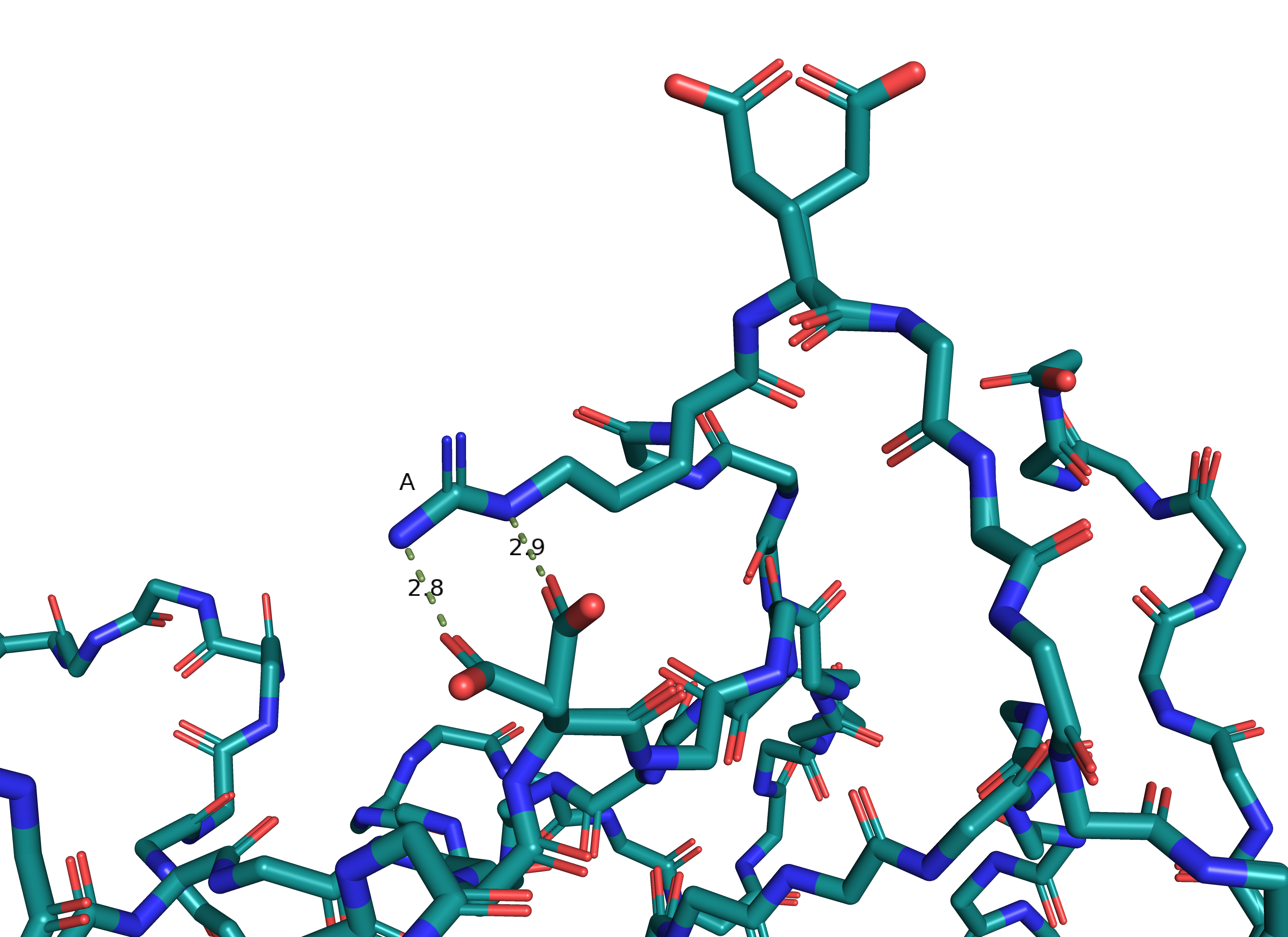 |
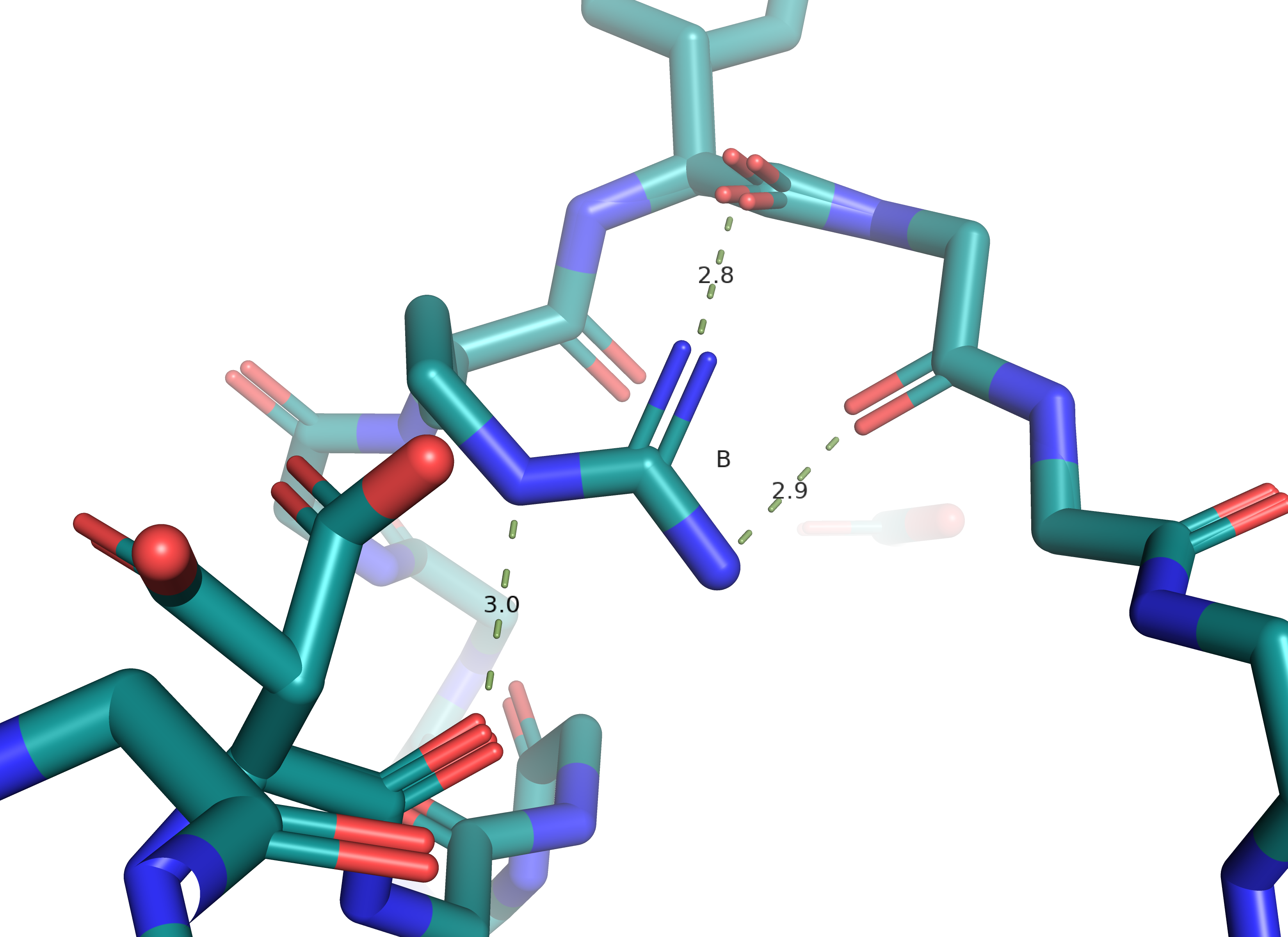 |
Пунктиром обозначены водородные связи, все они средней силы. У конформации А их две, а у конформации В - три. Поэтому я бы сказала, что альт-лок В стабильнее и оказалась бы при этом не права, потому что населённость у всех атомов альт-лока А = 0.7, а у В = 0.3.
Задание 2. B-фактор.
На рисунке ниже мой белок 4AF8, покрашенный по B-фактору в цветовой схеме blue_white_red.
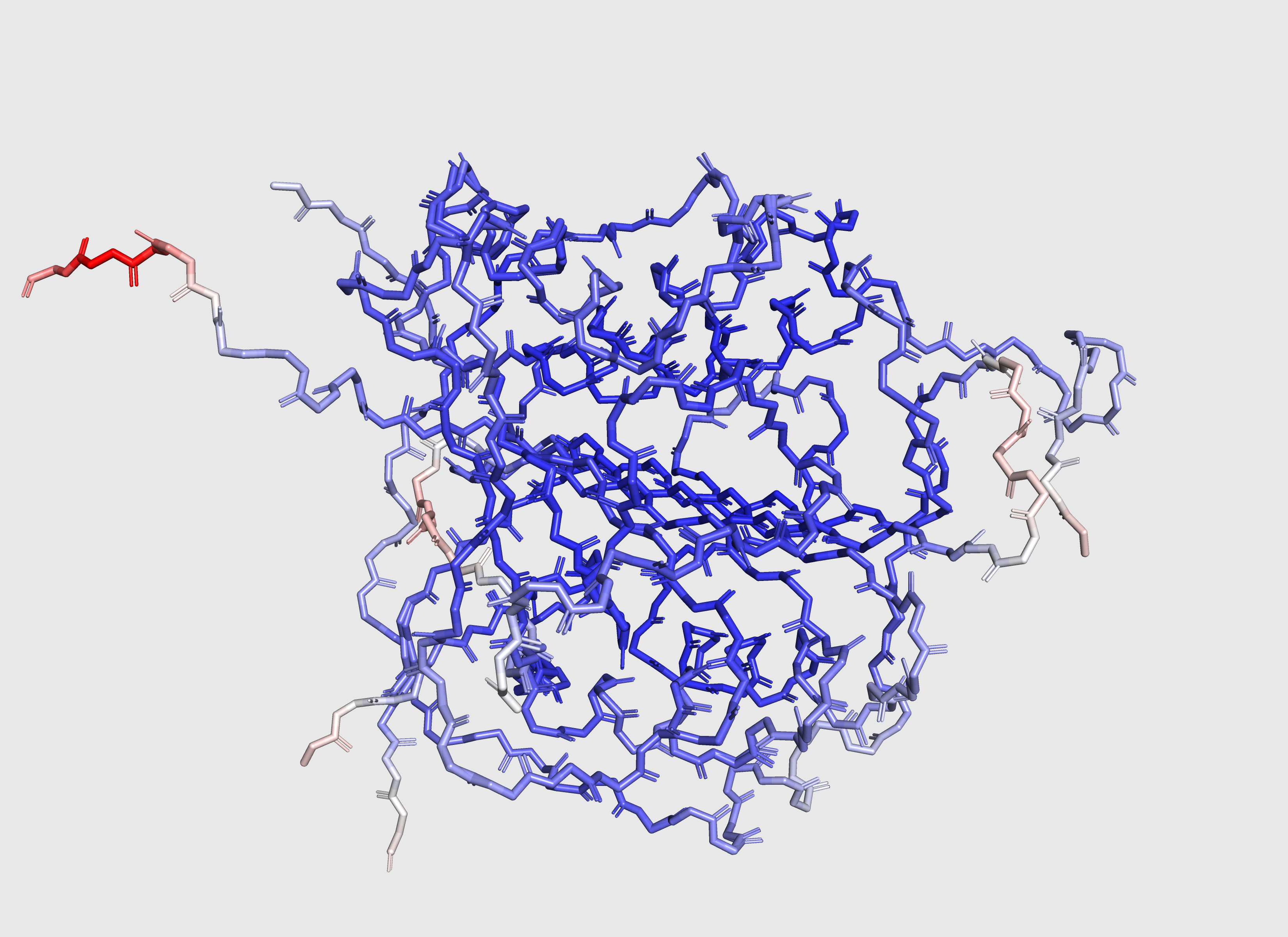
Видно, что значение B-фактора тем больше, чем атом дальше от центра глобулы белка. Чем больше B-фактор, тем более "размытой" мы представляем себе ЭП данного атома, и тем менее определённо для нас его положение в пространстве. То есть, чем чем ближе атом к центру белковой глобулы, тем точнее мы определяем его положение с помощью ЭП. Это кажется очень даже интуитивным, потому что, чем дальше атом от центра глобулы, тем меньше у него ближайших соседей, и, соответственно, тем больше у него вариантов расположения в пространстве. Ведь мы определяем положения атомов не только по данным об их собственной ЭП, но и по данным об ЭП их соседей и из наших общих знаний об устройстве белка.
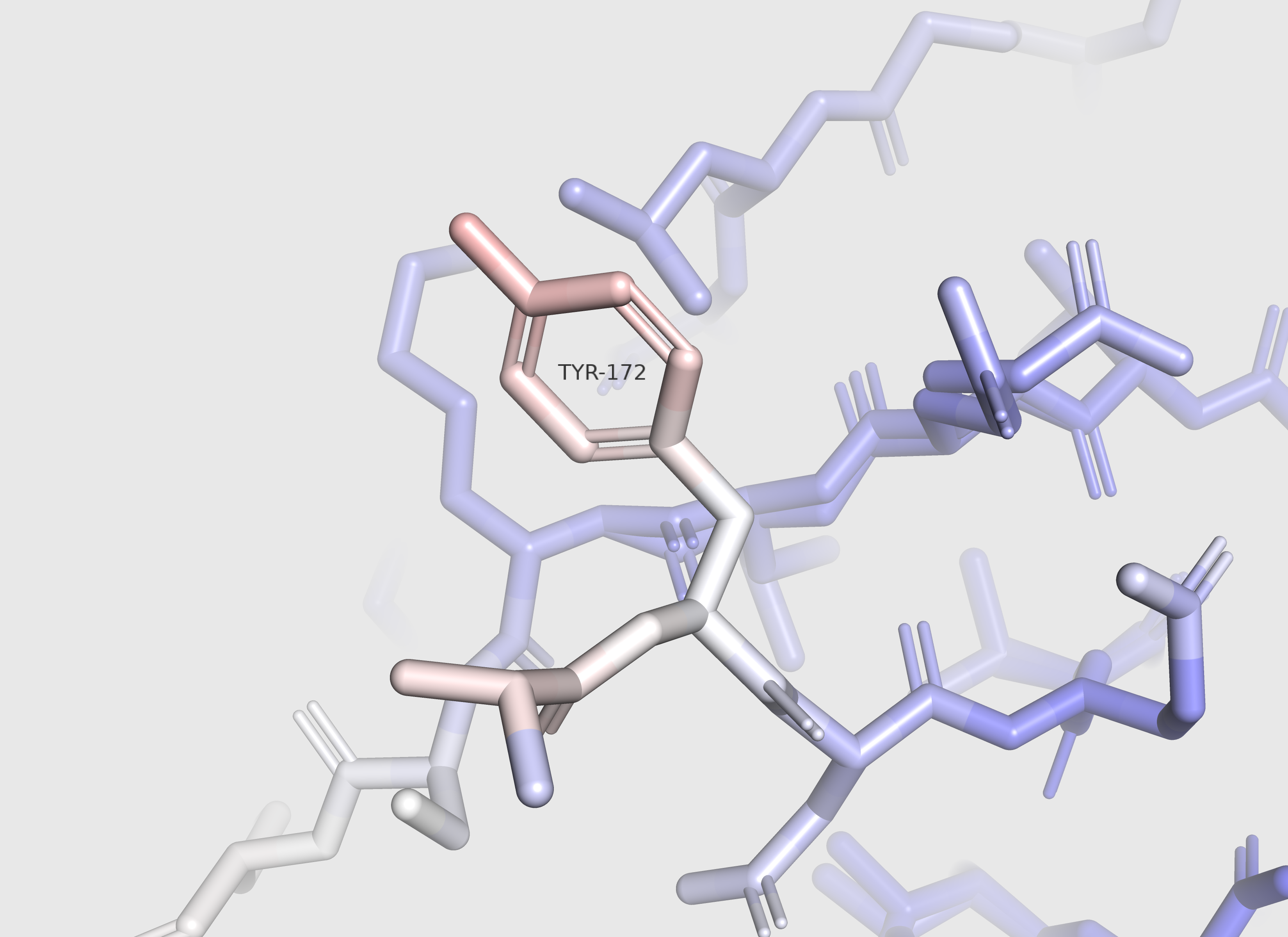
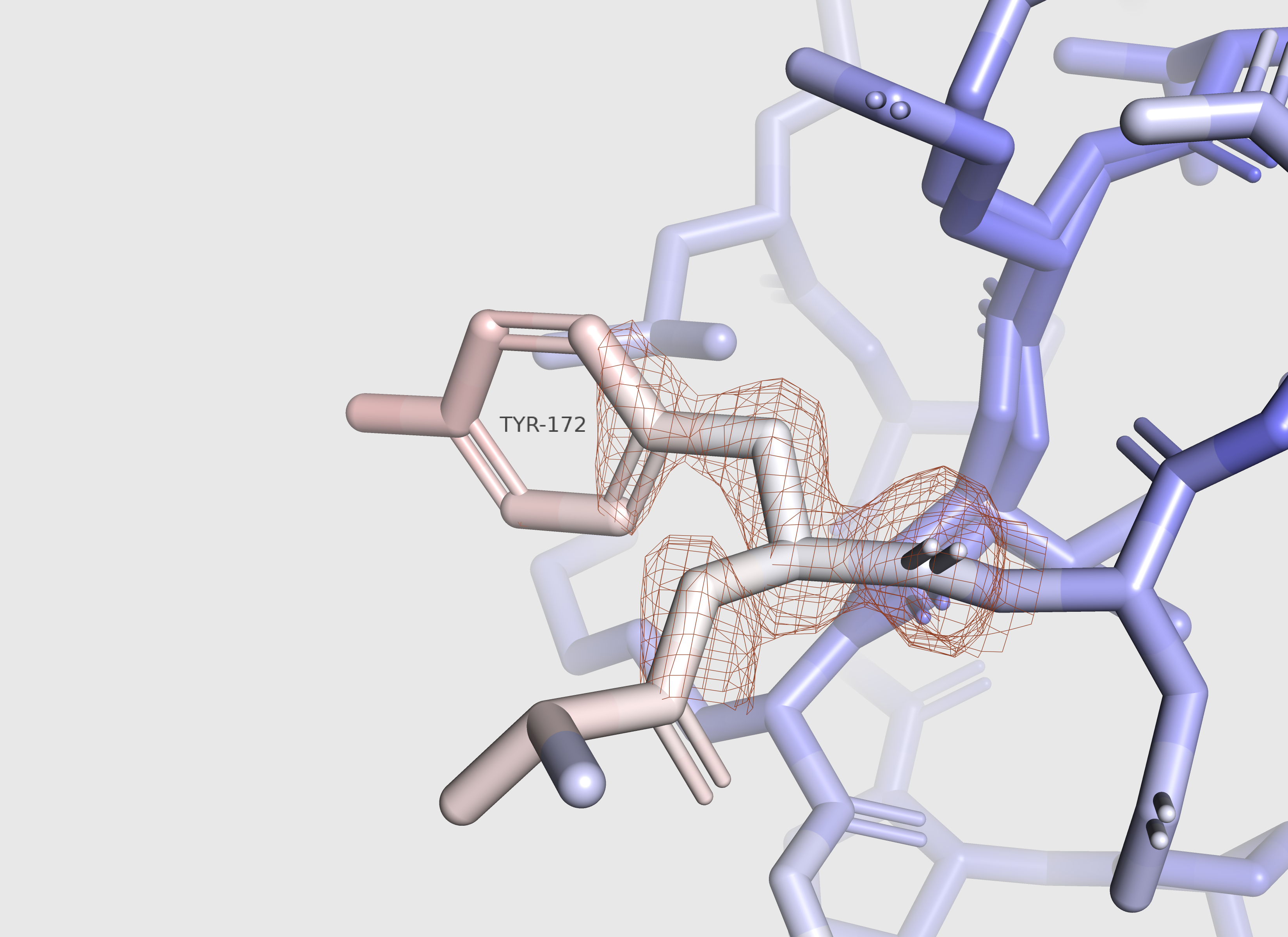
На рисунках ниже показан остаток TYR-172, на котором неплохо видно увеличение В-фактора к концу бокового радикала, и электронная плотность этого остатка на уровне подрезки 1 и со значением carve = 1.5.
| TYR-172 | ЭП TYR-172 |
 |
 |
Также я решила привести рисунок с ЭП "хвоста" из нескольких аминокислот, экспонированного в раствор. Значения В-фактора этих аминокислот заметно больше значений для всех остальных атомов белка. На рисунке видно, что и для "хвоста", чем больше значение В-фактора, тем меньше ЭП (уровень подрезки 1 и carve = 1.5).
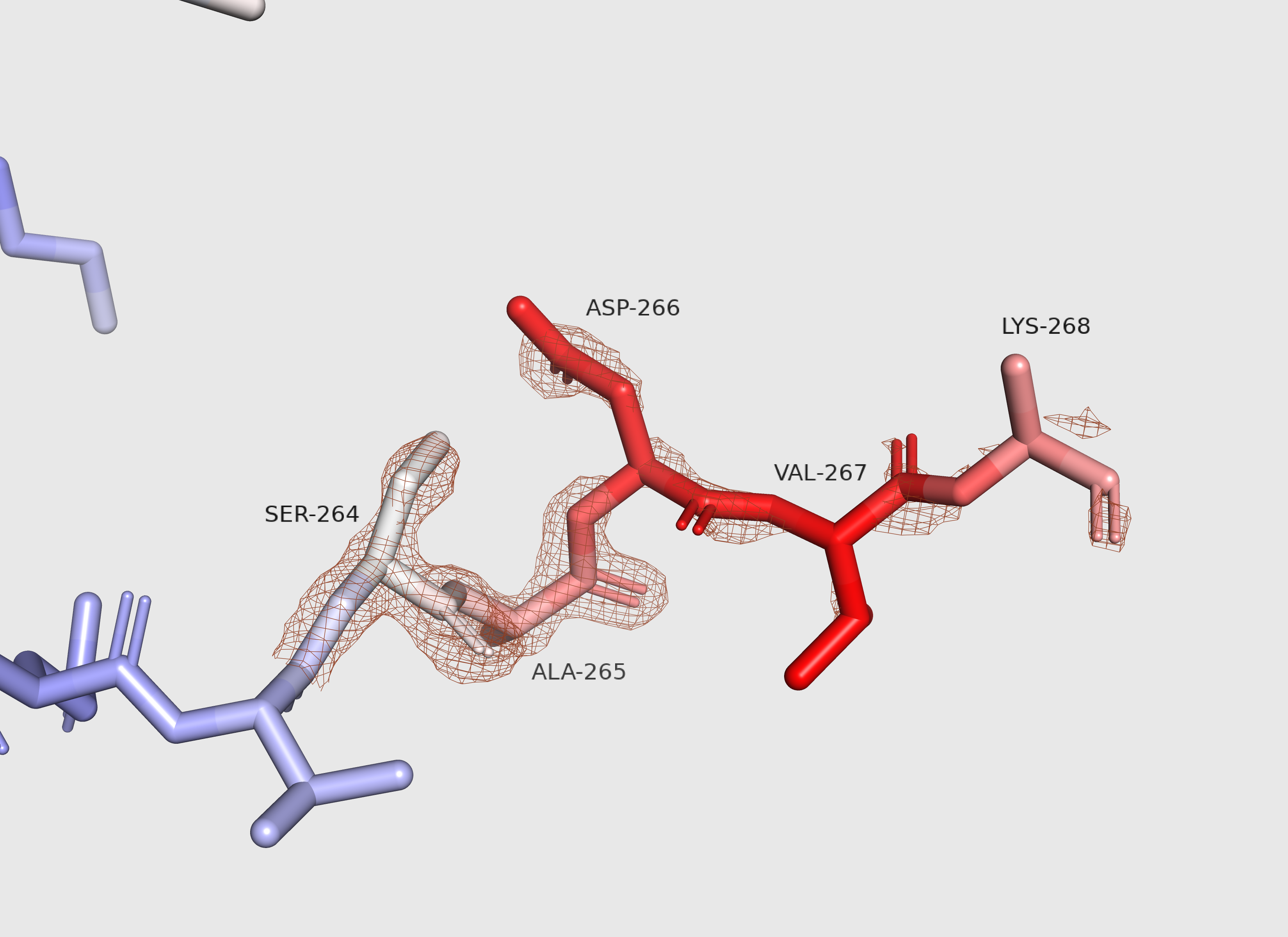
То есть ЭП в экспериментальных данных явно меньше у атомов с высоким В-фактором. Я думаю, это связано с тем, что вокруг этих атомов ЭП "рамазана" и, соответственно, разрежена. Ведь ЭП - это вероятность нахождения электрона в этой точке пространства, а при высоком В-факторе эта вероятность еще умножается на вероятность нахождения атома в этой точке, то есть становится меньше. Поэтому она с бOльшим трудом детектируется.
Задание 3. Соседи.
На рисунках ниже показаны все соседи исходного белка, попадающие в радиус 12 ангстремов, и только те соседи, которые контактируют с исходным белком (он показан черным).
 |
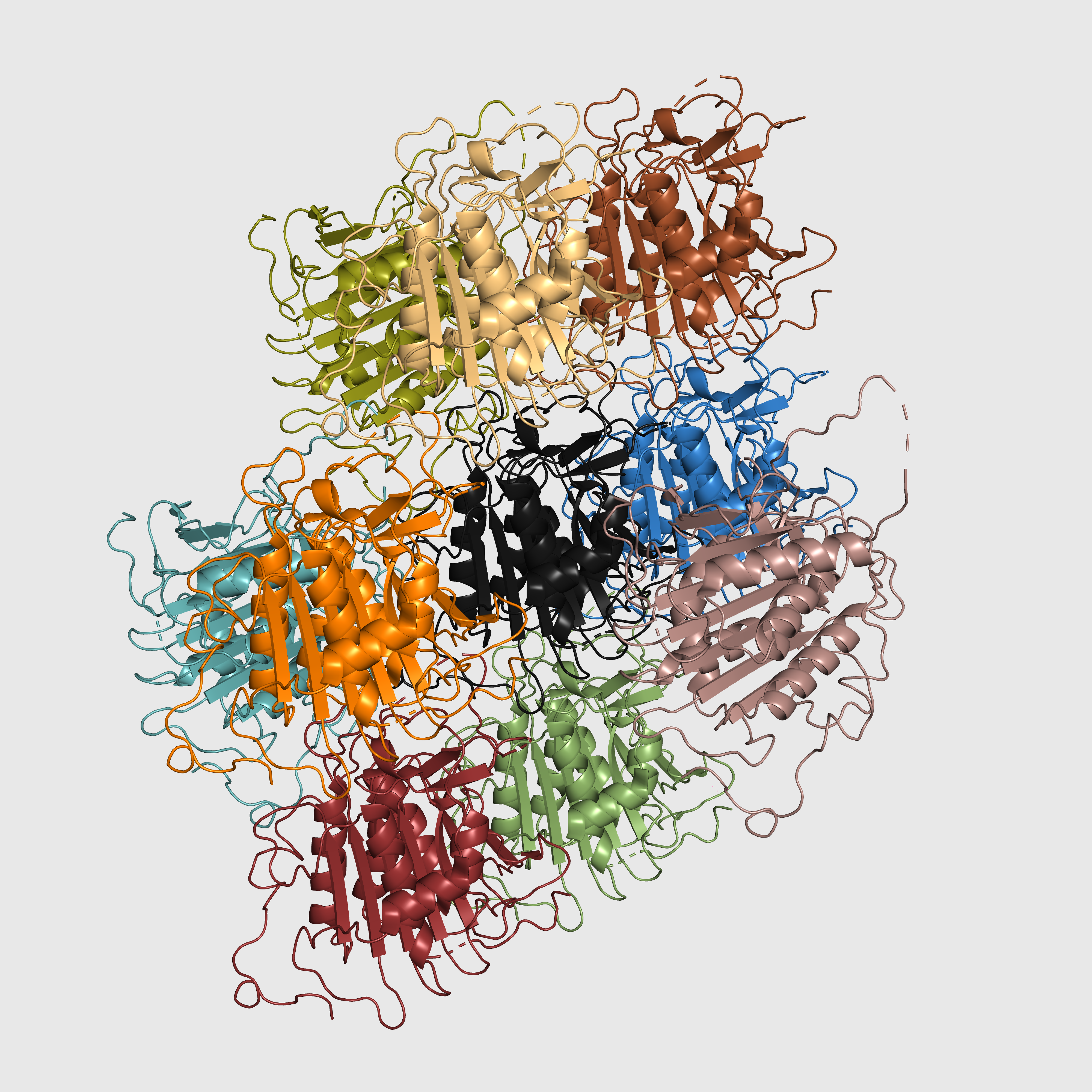 |
На первом рисунке хорошо видна упорядоченная структура кристалла. На втором рисунке оставлены только 9 соседей.