- Измерение торсионных углов остатка Asp10 в белке DHBE_BACSU, цепь А
|
Название
двугранного угла |
Угол определяется по координатам атомов |
Данный угол описывает поворот вокруг связи |
Результат измерения
с помощью RasMol |
| φ |
|
Ni — C&alphai | -47,86 |
| ψ |
|
C&alphai — Ci | -43,32 |
| ω |
|
Ci — Ni+1 | -179,17 |
Названия атомов, по которым определяется угол, даны в соответствие с синтаксисом RasMol: первые три буквы — название аминокислоты, потом записан её номер и индикатор цепи; после точки — атом (углерод карбоксильной группы — C, C&alpha — CA, азот аминогруппы — N). Например, PRO9A.C — карбонильный углерод пролина, 9-го остатка цепи А.
- Схема нахождения угла
скрипт для получения изображения
- Карты Рамачандрана
Карта Рамачандрана для множества свех остатков (all), остатков глицина (Gly), и пролина (Pro) белка DhbE.
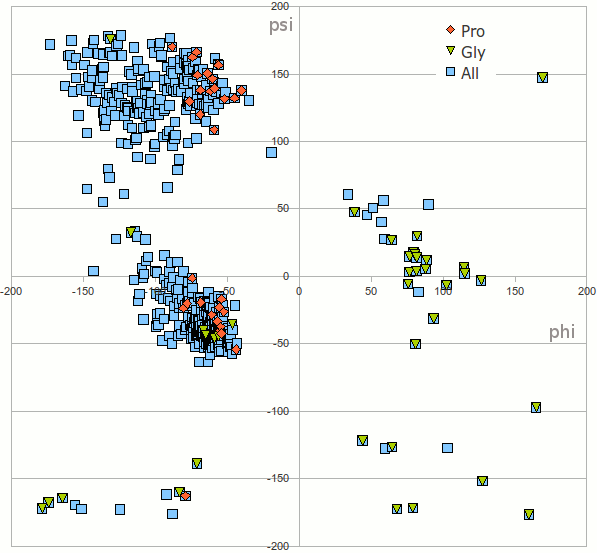
Для большинства аминокислот в составе DhbE характерны значения φ [-175; -25] и ψ [-75; 180]
Значительную часть аминокислот, значения углов которых лежат в других интервалах, составляет глицин. Это, вероятно, связано с тем, что радикал глицина(водород) не сильно затрудняет вращение вокруг связей Ni — C&alphai и C&alphai — Ci
Значение угла φ у пролина лежит в относительно узкой области: [-100; -25]. Что, вероятно, связано со строением иминокислоты: её гетероцикл сильно ограничивает вращение вокруг Ni — C&alphai.
Карта Рамачандрана для множества всех остатков (all), остатов, входящих в состав α-спиралей (helix) и остатков, входящих в состав β-листов (sheet) белка DhbE.
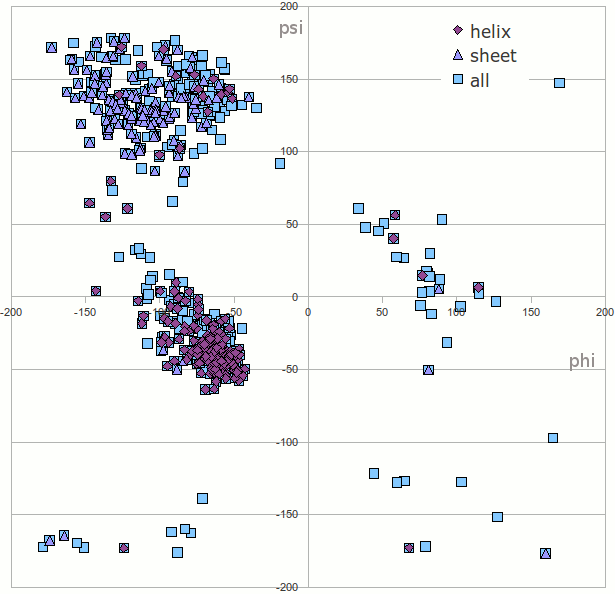
Для остатков α-спиралей и β-складок характерны относительно узкие интервалы φ и ψ, что, вероятно, связано с их регулярностью и тем, что водородные связи в их структуре ограничивают вращение.
α-спирали: φ [-125; -25] и ψ [-75; 25]
β-листы: φ [-175; -50] и ψ [100; 175]