Описание области контакта белка и лиганда Mn2+ в структуре 2VO9
Лиганды в структуре 2V09
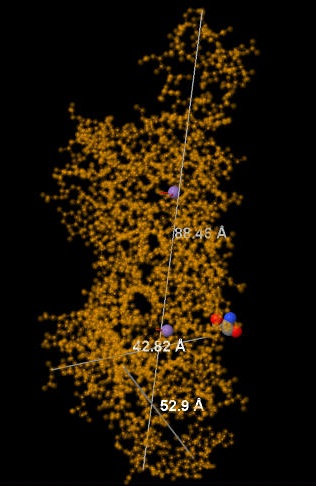 Рис.1 Оксалат-декарбоксилаза (одна субъединица) показана оранжевым, ионы марганца - сиреневыми сферами,
атомы в молекуле Tris показаны сферами (углерод - серый, кислород - красным, азот - синим).
Для получения изображения использовалась программа Jmol
Рис.1 Оксалат-декарбоксилаза (одна субъединица) показана оранжевым, ионы марганца - сиреневыми сферами,
атомы в молекуле Tris показаны сферами (углерод - серый, кислород - красным, азот - синим).
Для получения изображения использовалась программа JmolДля выполнения работы использовалась адаптированная под предполагаемую структуру белка в клетке модель (biological assembly). В белке присутствуют два типа лигандов: ионы Mn2+ и трис-гидроксиметил-аминометан (рис. 1). Второе вещество, вероятно, присутствует в модели в силу того, что является компонентом популярного буфера, а не в силу наличия функциональной связи с белком. Об этом свидетельствует, в том числе, очень малое число взаимодействий между белком и трис. Марганец, вероятно, является коферментом
В таблице 1 приведены линейные размеры белка и лигандов. Заметно, что ион марганца значительно крупнее небольшого органического лиганда TRIS
| Таблица 1 | |
| Длина белка | 8.84 nm / 88.46 angstrom / 8.84*10-9m |
| Ширина белка | 4.28 nm / 42.82 angstrom / 4.28*10-9m |
| Высота белка | 5.92 nm/ 59.2 angstrom / 5.92*10-9m |
| Радиус иона Mn2+ | 0.9 nm / 9 angstrom / 9*10-10m |
| Относительный размер (отношение радиуса иона к длине/ширине/высоте белка) | 0.1/0.21/0,15 |
| Размер лиганда TRIS | 0.41 nm / 4.16 angstrom / 4,16*10-10m |
| Относительный размер (отношение размеров лиганда к размерам белка) | 0,05/0,1/0,07 |
Анализ области контакта белка из структуры PDB 2V09 и лиганда Mn2+
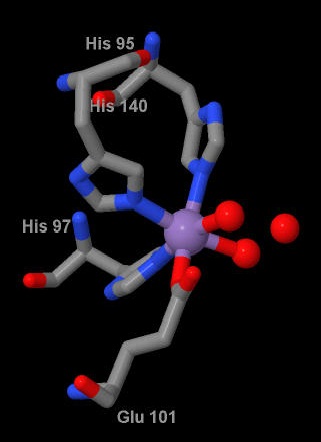 Рис. 2 Модель связывающего лиганд центра.
Показаны связи между атомами, кислород обозначен красным, азот - синим, углерод
- серым, вода - красными сферами, марганец - сиреневой сферой.
Для получения изображения использовалась программа Jmol
Рис. 2 Модель связывающего лиганд центра.
Показаны связи между атомами, кислород обозначен красным, азот - синим, углерод
- серым, вода - красными сферами, марганец - сиреневой сферой.
Для получения изображения использовалась программа JmolВ каждой субъединице (всего их шесть) оксалат - декарбоксилазы имеются два связанных иона марганца. Один из них связан шестью координационными связями, другой - пятью (оба иона координируются одинаковым набором аминокислот с примерно одинаковым расположением, различие заключается только в числе молекул воды) Однако, поскольку координационное число 6 характерно для иона марганца, а 5 - не характерно, далее приводится информация для шестикоординационного центра. Этот ион марганца образует координационные (по донорно-акцепторному механизму) связи с тремя гистидинами (95,97,140) и одним глутаматом (101), а также двумя молекулами воды (рис. 2, рис. 3). На рисунке 4 представлена схема взаимодействия аминокислотных остатков и лиганда.
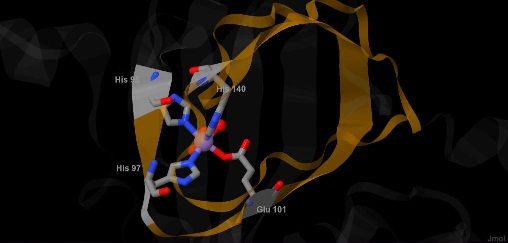 Рис. 3 Расположение координирующих магний аминокислотных остатков в цепи А белка (оранжевым выделены остатки в
промежутках между теми, что связаны с магнием). Прочие обозначения аналогичны таковым на рисунке 2.
Для получения изображения использовалась программа Jmol
Рис. 3 Расположение координирующих магний аминокислотных остатков в цепи А белка (оранжевым выделены остатки в
промежутках между теми, что связаны с магнием). Прочие обозначения аналогичны таковым на рисунке 2.
Для получения изображения использовалась программа Jmol
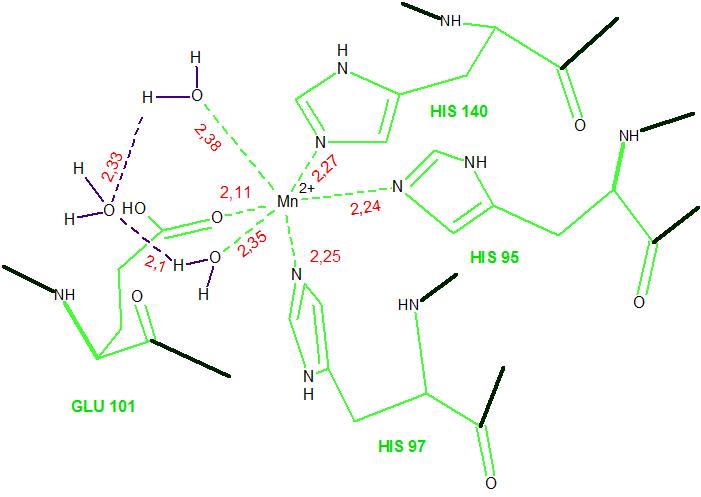 Рис. 4 Схема связей лиганда и координирующих его аминокислотных остатков оксалат-декарбоксилазы
(обозначены салатовым, связи с другими остатками - тёмно-зелёным). Вода обозначена фиолетовым. Водородные и координационные связи показаны пунктиром.
Приведены расстояния координационых связей белок-лиганд и водородных связей с водой (обозначены красным, единица измерения - ангстрем).
Выявить, какими остатками координируются обозначенные молекулы воды, не представляется возможным (расстояния до ближайших сильноэлектроотрицательных атомов больше четырёх ангстрем).
Для получения изображения использовалась программа Chemsketch.
Рис. 4 Схема связей лиганда и координирующих его аминокислотных остатков оксалат-декарбоксилазы
(обозначены салатовым, связи с другими остатками - тёмно-зелёным). Вода обозначена фиолетовым. Водородные и координационные связи показаны пунктиром.
Приведены расстояния координационых связей белок-лиганд и водородных связей с водой (обозначены красным, единица измерения - ангстрем).
Выявить, какими остатками координируются обозначенные молекулы воды, не представляется возможным (расстояния до ближайших сильноэлектроотрицательных атомов больше четырёх ангстрем).
Для получения изображения использовалась программа Chemsketch.
Скрипт
Получить рисунки 1,2 можно с помощью следующего скрипта