Для выполнения задания был выбран белок 5ikq, содержащий альфа-спирали и бета-тяжи. На рисунке 1 представлена его структура с раскраской по вторичной структуре, указанной в header pdb файла.
 Рис.1. Вторичная структура белка 5ikq
Рис.1. Вторичная структура белка 5ikq
Для анализа были выбраны 1 альфа-спираль и 1 бета-лист с каждой субъединицы. Всего 4 структуры. Выбранные элементы визаулизированы на рисунке 2.
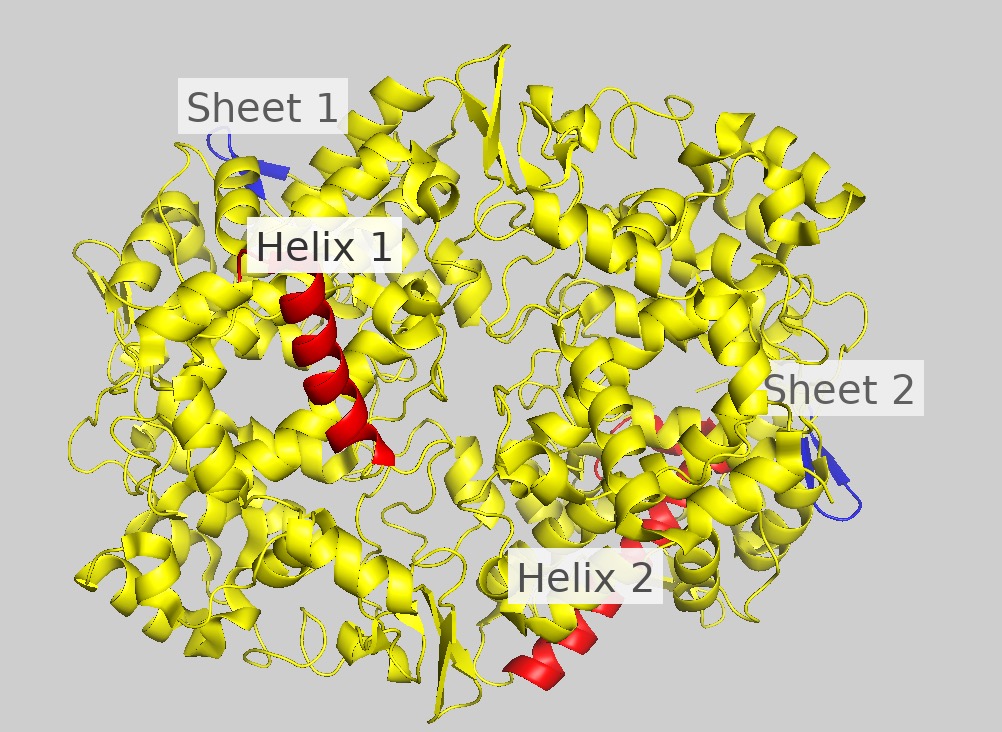 Рис. 2. Выбранные для анализа элементы вторичной структуры
Рис. 2. Выбранные для анализа элементы вторичной структуры
Вторичная структура исследуемого белка была определена с помощью веб-сервиса
Stride. Результат выдачи доступен для скачивания по
ссылке . В таблице приведено сравнение разметки, полученной с использованием Stride, и разметки, содержащейся в заголовке pdb файла.
| Структура |
Границы в PDB |
Границы в Stride |
| Helix 1 (A) |
ILE 105 - HIS 122 |
PRO 106 - SER 119 |
| Helix 2 (B) |
VAL 296 - HIS 321 |
PRO 106 - SER 119 |
| Sheet 1 (A) |
GLN 255 - ILE 257
GLU 260 - TYR 262 |
GLN 255 - ILE 257
GLU 260 - TYR 262 |
Sheet 2 (B) |
PHE 396 - ILE 398
GLN 401 - TYR 403 |
PHE 396 - ILE 398
GLN 401 - TYR 403 |
Видно, что разметка бета-листов полностью совпала, а вот при разметке альфа-спиралей stride "отрезает" крайние остатки.
На рисунке 3 зеленым цветом показаны фрагменты цепи А, образующие мостики и завитки (согласно Stride).
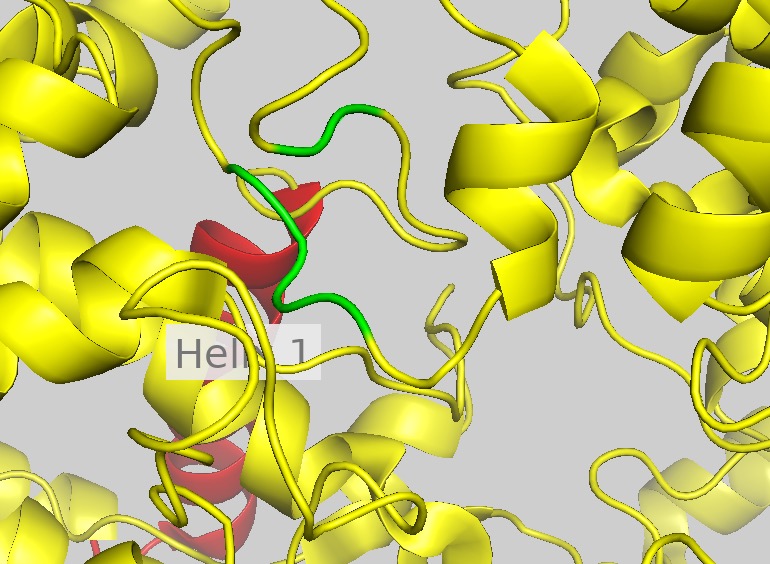 Рис. 3. Мостики и завитки
Рис. 3. Мостики и завитки


