Файл PDB.
- Введение
В данном практикуме изучаются такие особенности рентгеноструктурной модели белка, как альтернативные положения, B-фактор, расположение внутри кристалла. Я использовал структуру 6HMQ. Это структура каталитической субъединицы киназы белков CK 2, она получена с очень хорошим разрешением 0.97 Å, эксперимент проводился при температуре 100 К. Внутри ассиметрической единицы находится одна молекула белка.
- Задание 1. Альтернативные положения.
В данном задании предлагается изучить альтернативные конформации аминокислотных остатков внутри структурной модели. Я рассмотрел взаимное расположение двух остатков - фенилаланина-122 и тирозина-126 - и их альтернативные конформации. Так как эти остатки располагаются рядом, некоторые их положения не могут быть совместимы. В PDB-файле доля ячеек с тем или иным положением атома боковой цепи описывается полем occupancy, параметром, который вычисляется при обработке рассчитанной электронной плотности. PHE-122 принимает конформацию A в 35% ячеек, а конформацию B - в 65% ячеек. Конформации TYR более равномерно встречаются в кристалле: A - 49%, B - 51%.
На Рисунке 1 представлено сочетание конформации А фенилаланина и конформации В тирозина. Боковые цепи накладываются друг на друга, такое сочетание невозможно. На Рисунке 2 представлено сочетание ВPHE и BTYR. Фенилаланин может удерживаться Т-стекингом с гистидином-161, а тирозин соединяться водородной связью через молекулу воды с валином-163. На Рисунке 3 предсавлено такое сочетание, где тирозин принимает конформацию А. Он может образовывать водородные связи с растворителем. На Рисунке 4 представлено последнее возможное сочетание: APHE и ATYR. Боковая цепь PHE обращена в гидрофобный карман, образованный остатками метионина, лейцина, изолейцина, пролина.
Проанализируем наблюдаемые частоты конформаций и предположим встречаемость разных сочетаний на основании данных о населенности. Положим, что сочетание 1 не встречается вообще. Тогда во всех ячейках, где тирозин встречается в конформации В, присутствует сочетание 2 с частотой 0.51. Но фенилаланин принимает конформацию В с частотой 0.65, значит 0.65 - 0.51 = 0.14 приходится на сочетание 3. Сочетание 4 появляется с частотой 0.35 при боковой цепи фенилаланина, обращенной внутрь глобулы.
Кажется логичным, что сочетание 3 может быть встречено реже всего: в структуре образуется гидрофобная полость, где у воды не получится образовать водородные связи с аминокислотными остатками. Энергетически более выгодным мне видится сочетание 4, так как реализуется гидрофобное взаимодействие, а тирозин становится более доступным для образования водородных связей с растворителем и другими боковыми цепям. Однако стоит учесть, что эти рассуждения основаны лишь на модели, которая предсказывает достаточно дискретные положения остатков и может сильно отличаться от ситуации в растворе.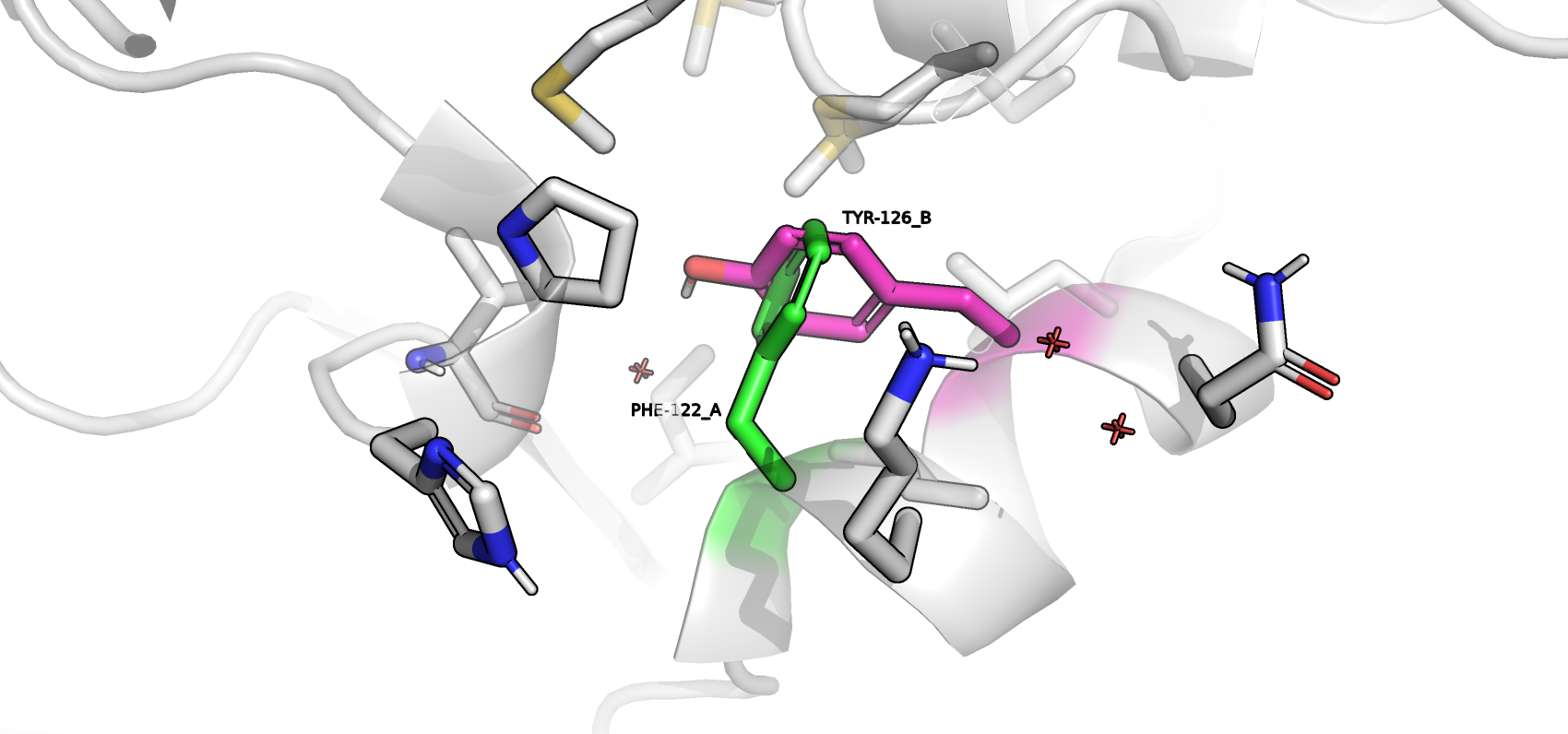
Рисунок 1. Сочетание 1.
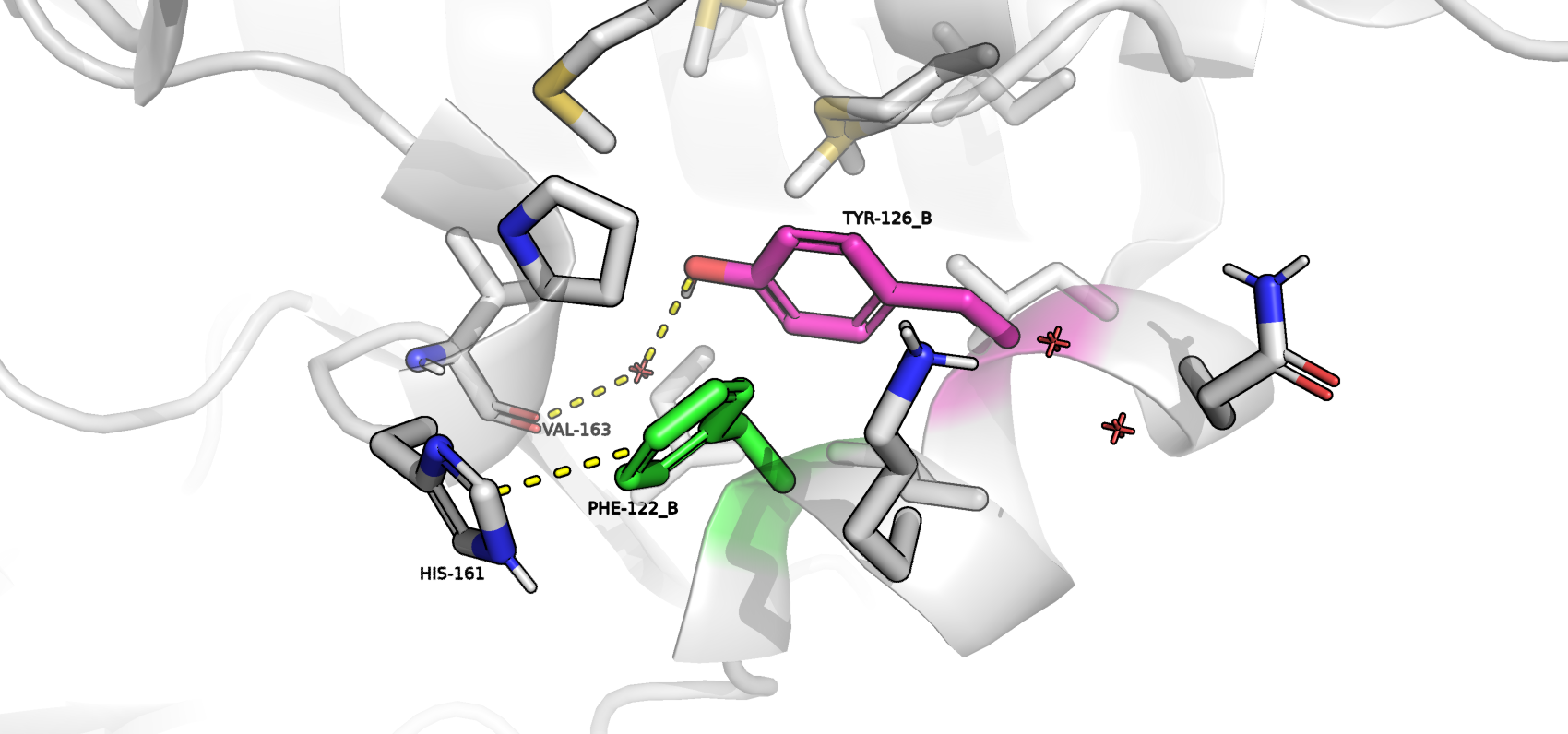
Рисунок 2. Сочетание 2.
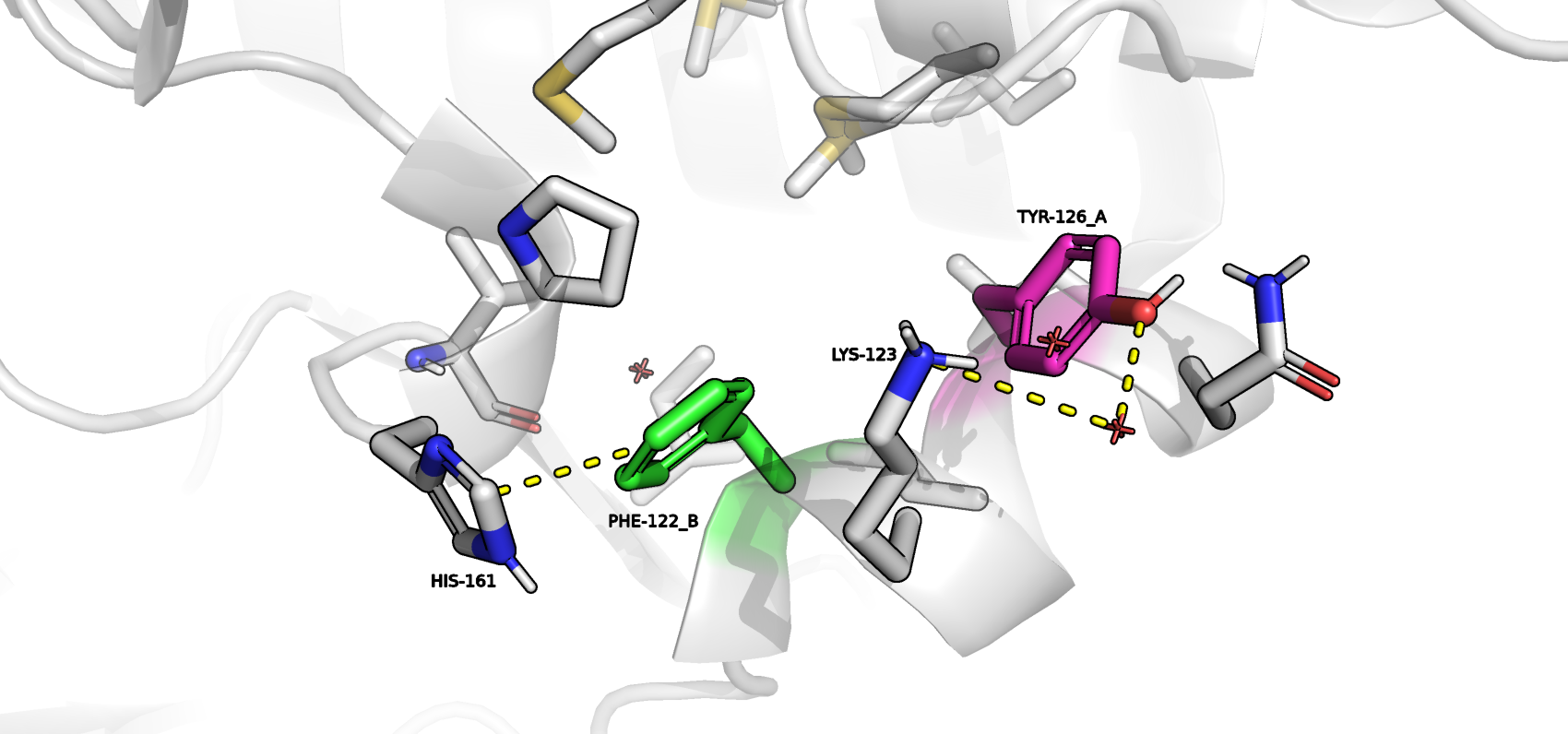
Рисунок 3. Сочетание 3.
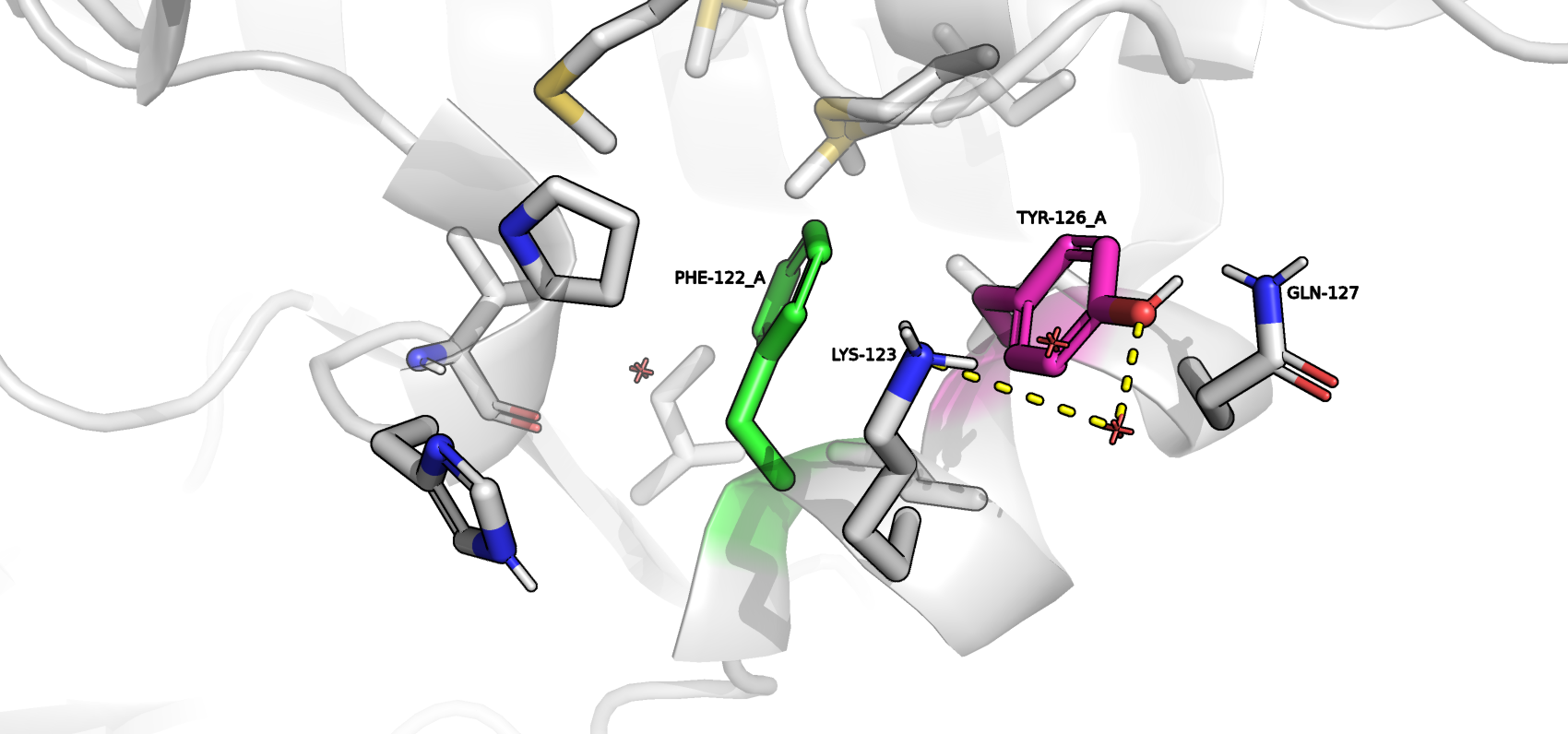
Рисунок 4. Сочетание 4.
- Задание 2. B-фактор.
Для анализа полученной электронной плотности используют также B-фактор или температурный фактор. Он позволяет показать, насколько сильно позиция каждого атома структуры может отклоняться от позиции, усредненной по всему кристаллу. Такой показатель необходим, так как в кристалле и при кристаллизации атомы могут совершать тепловые движения.
На Рисунке 5 представлен остов структуры 6HMQ, покрашенный по B-фактору. Синие учатки соответсвуют меньшим значениям, красные - большим. Можно заметить, что красный оттенок появляется в 3 местах: рядом с пролином-73, серином-333 и глицином-7. Первый участок соединяет α-спираль с β-листом, а второй и третий - C- и N-конец соответственно. По-видимому, эти остовы слабо стабилизированы водородными связями, удерживающими вторичные структуры, и другими нековалентными взаимодействиями, что допускает их тепловые колебания с большей амплитудой.
На Рисунках 6-8 изображна аминокислота ARG-90 с очерченной вокруг нее электронной плотностью на разных уровнях подрезки. Структура также раскрашена по B-фактору. С увеличением уровня подрезки ЭП перестает отображаться около атомов с большим значением B-фактора (красных), но остается вокруг атомов с малым значением. Это согласуется с моими наблюдениями в Практикуме 2. Значения B-фактора возрастают от 13.72 у CA до 47.9 у NH1 и NH2. При этом стоит отметить, что на уровне подрезки 1 ЭП все еще отображается вокруг атома CZ. Мне кажется, что это обусловлено высокой электронной плотностью всей гуанидиновой группы. Также у меня есть предположение, что у данного остатка возможна альтернативная конформация. От атома CD отходит отрисовка электронной плотности, не описанная вокруг какого-то атома (Рисунок 6 и 7). Вероятно, вокруг связи CG-CD возможно вращение, в результате чего гуанидиновая група меняет свое положение и обращается "вниз", и из-за этого в данном месте предсказаны высокие значения ЭП, которые, кажется, не объясняются молекулами воды, лигандами, или другими боковыми цепями.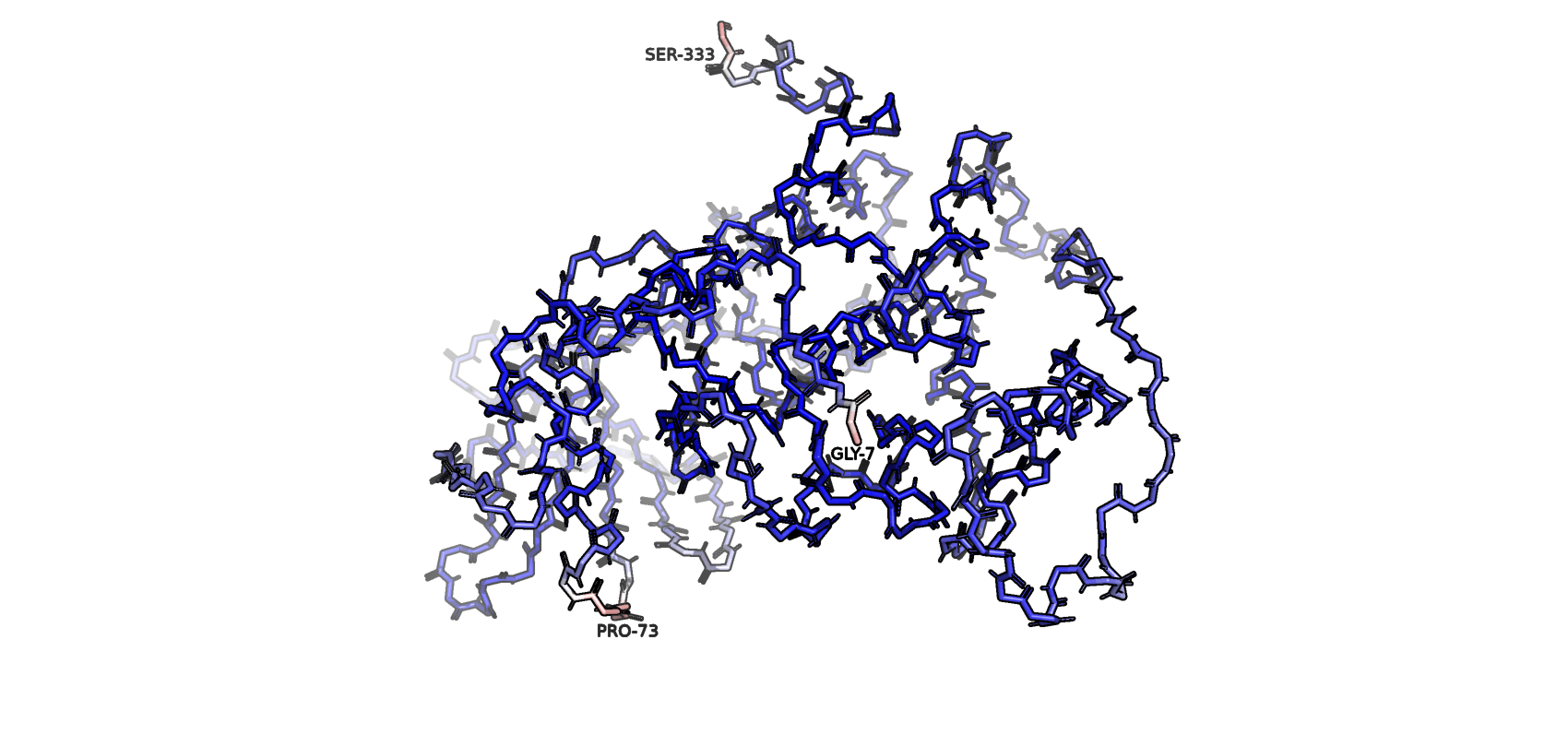
Рисунок 5. ЭП остова белка на уровне подрезки 1.
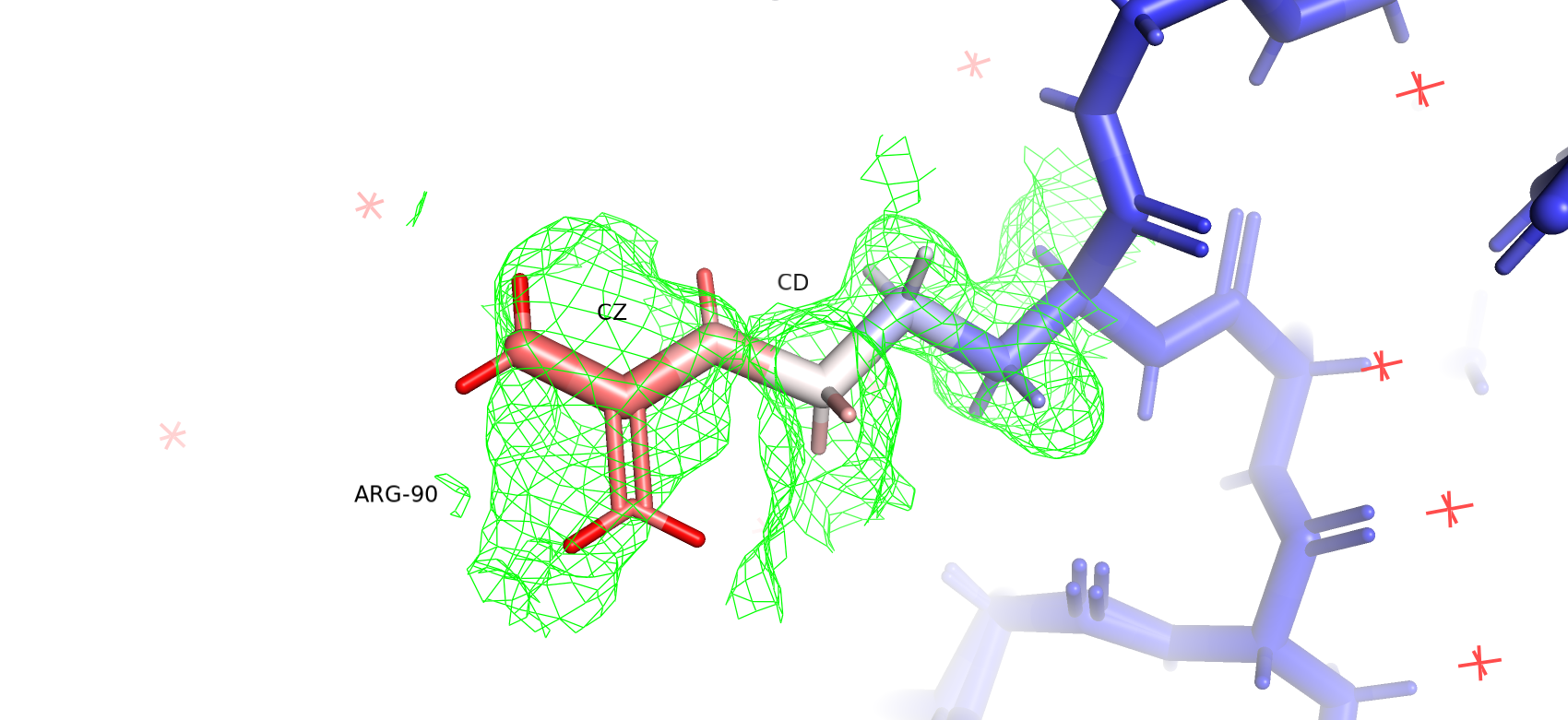
Рисунок 6. ЭП ARG-90 на уровне подрезки 0.25.
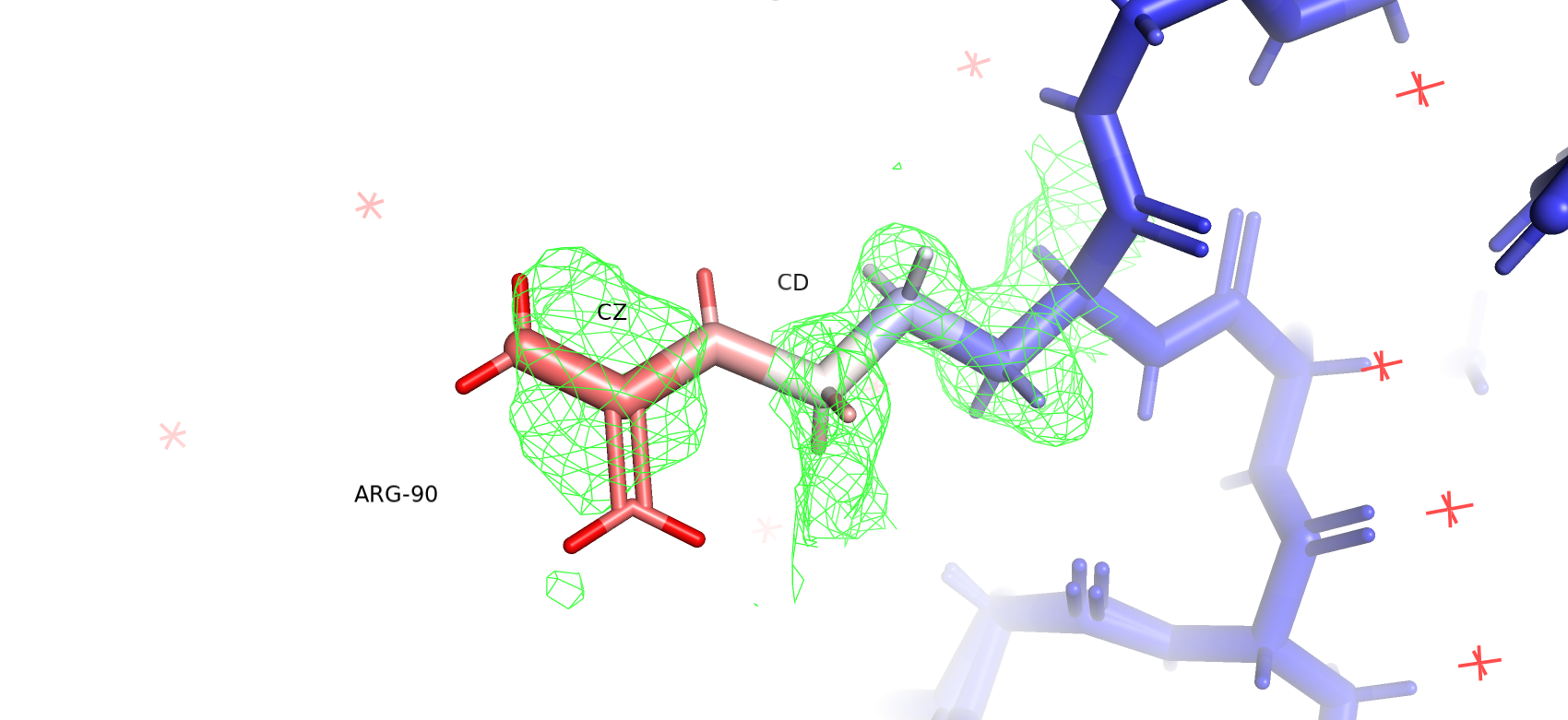
Рисунок 7. ЭП ARG-90 на уровне подрезки 0.5.
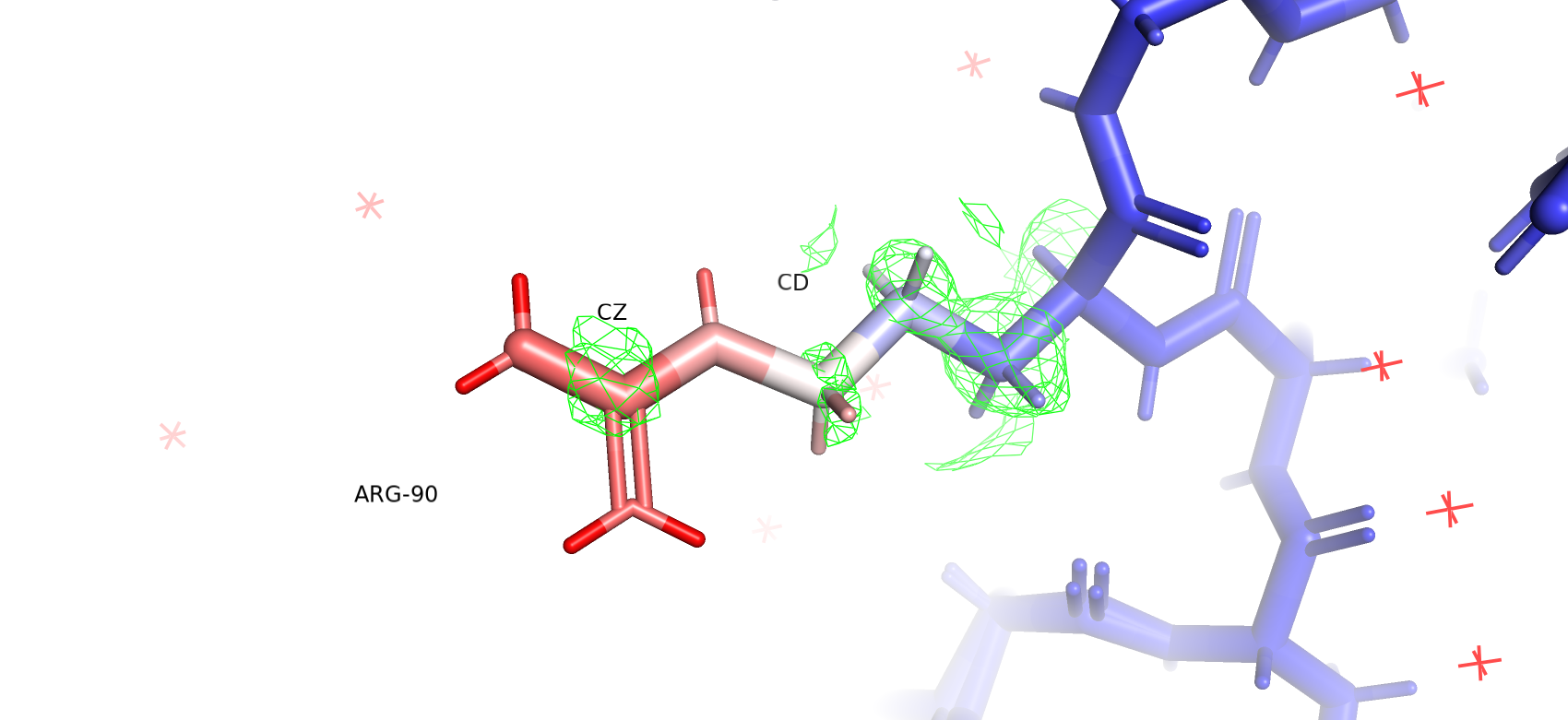
Рисунок 8. ЭП ARG-90 на уровне подрезки 1.
- Задание 3. Кристалл.
В данном задании я рассмотрел расположение белковых молекул данной субъединицы внутри кристалла. На Рисунке 9 сгенерированы соседние молекулы на отсечке 20. Хорошо видно, что внутри кристалла молекулы располагаются упорядочено, сохраняя свою ориентацию в пространстве. На Рисунке 10 показаны только соседи исходной молекулы на отсечке 2. Исходная молекула соприкасается с 6 соседями, при этом только 3 области контакта являются уникальными.
В базе данных PDB мне удалось найти полную структуру данного фермента, казеин киназы 2 - 1JWH. Она состоит из 4 субъединиц; две β-субъединицы образуют димер, осуществляют регуляцию фермента. Каждая из 2 α-субъединиц взвимодействует с таким димером, не формируя при этом контактов между собой. Молекула из структуры 6HMQ аналогична как раз такой α-субъединице. На Рисунке 11 представлена структура 1JWH, выравненная на 6HMQ с помощью команды super (RMSD 0.792). Оригинальная α-субъединица целого фермента не показана. На Рисунке 12 изображена исходная молекула 6HMQ с одним из соседей. Похоже, область взаимодействий молекул белка в кристалле перекрывается с областью взаимодействия цепей внутри фермента.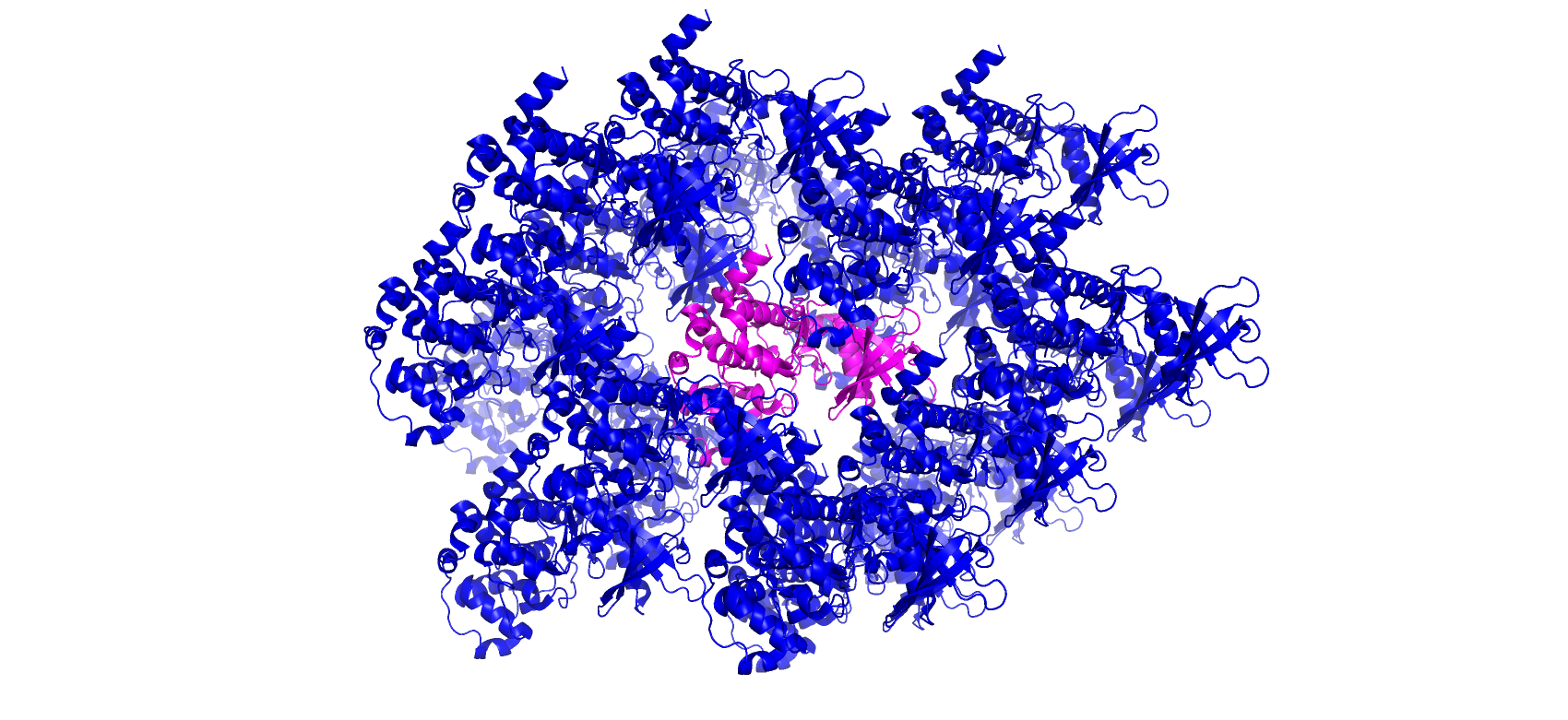
Рисунок 9. Соседние молекулы на отсечке 20.
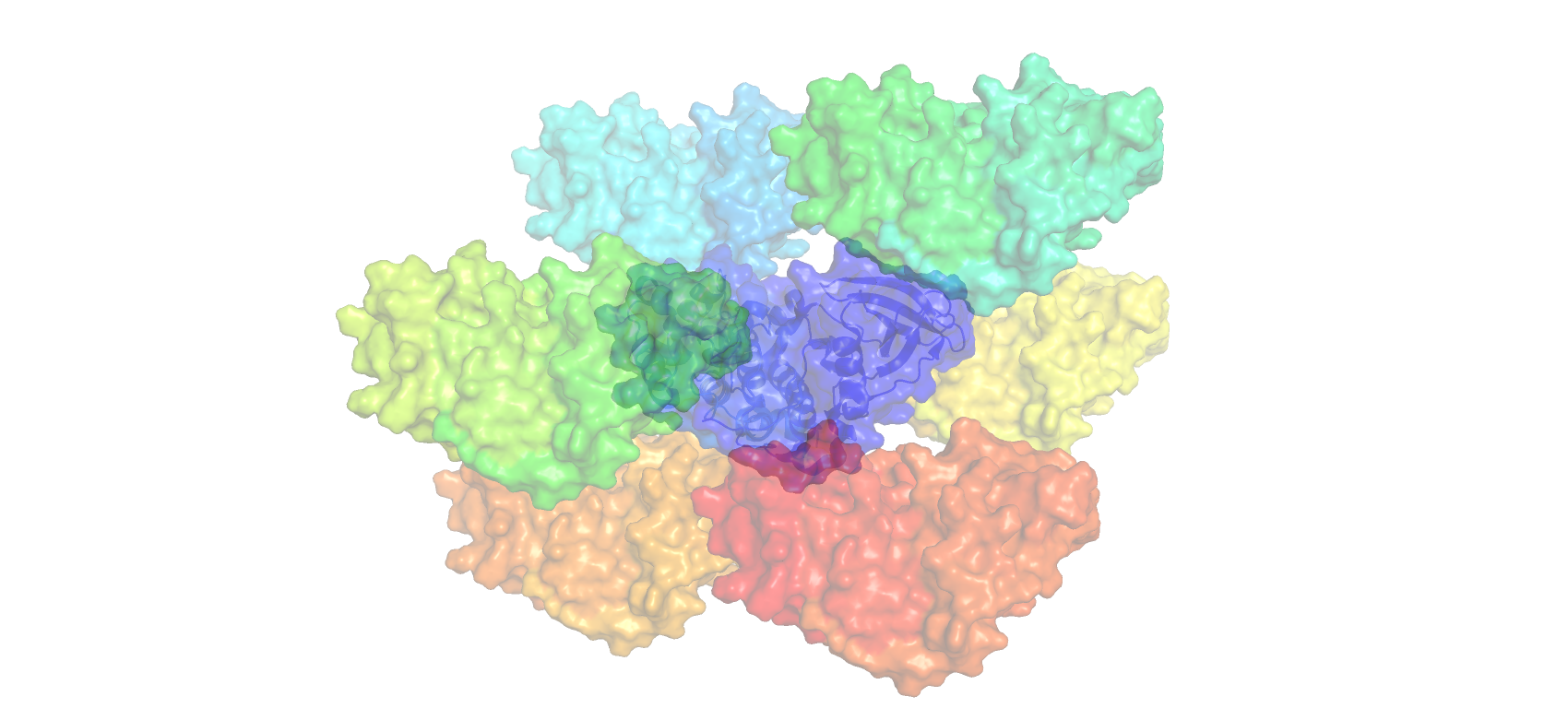
Рисунок 10. Соседние молекулы на отсечке 2.
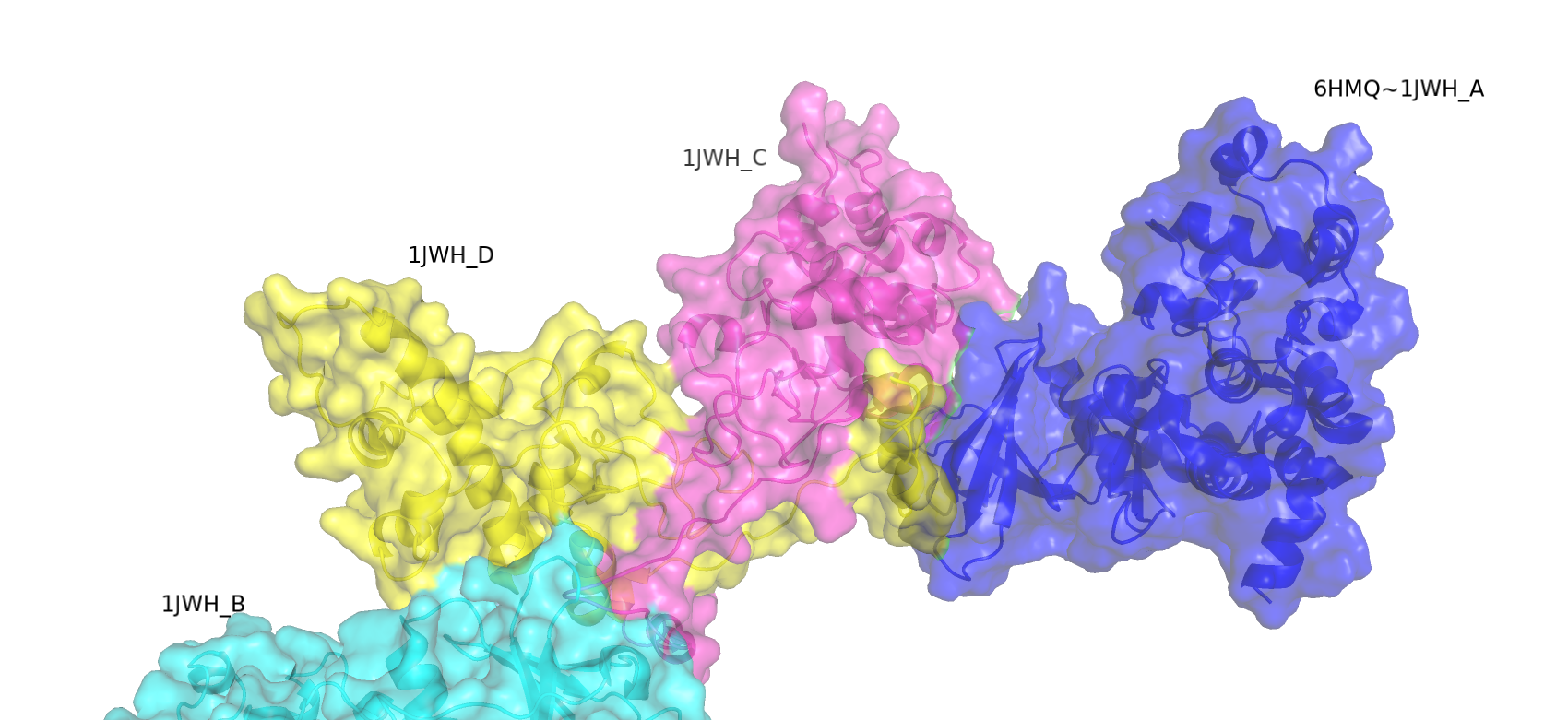
Рисунок 11. 6HMQ, выравненный с 1JWH. Цепи D и C - β-субъединицы, цепи A и B - α-субъединицы.
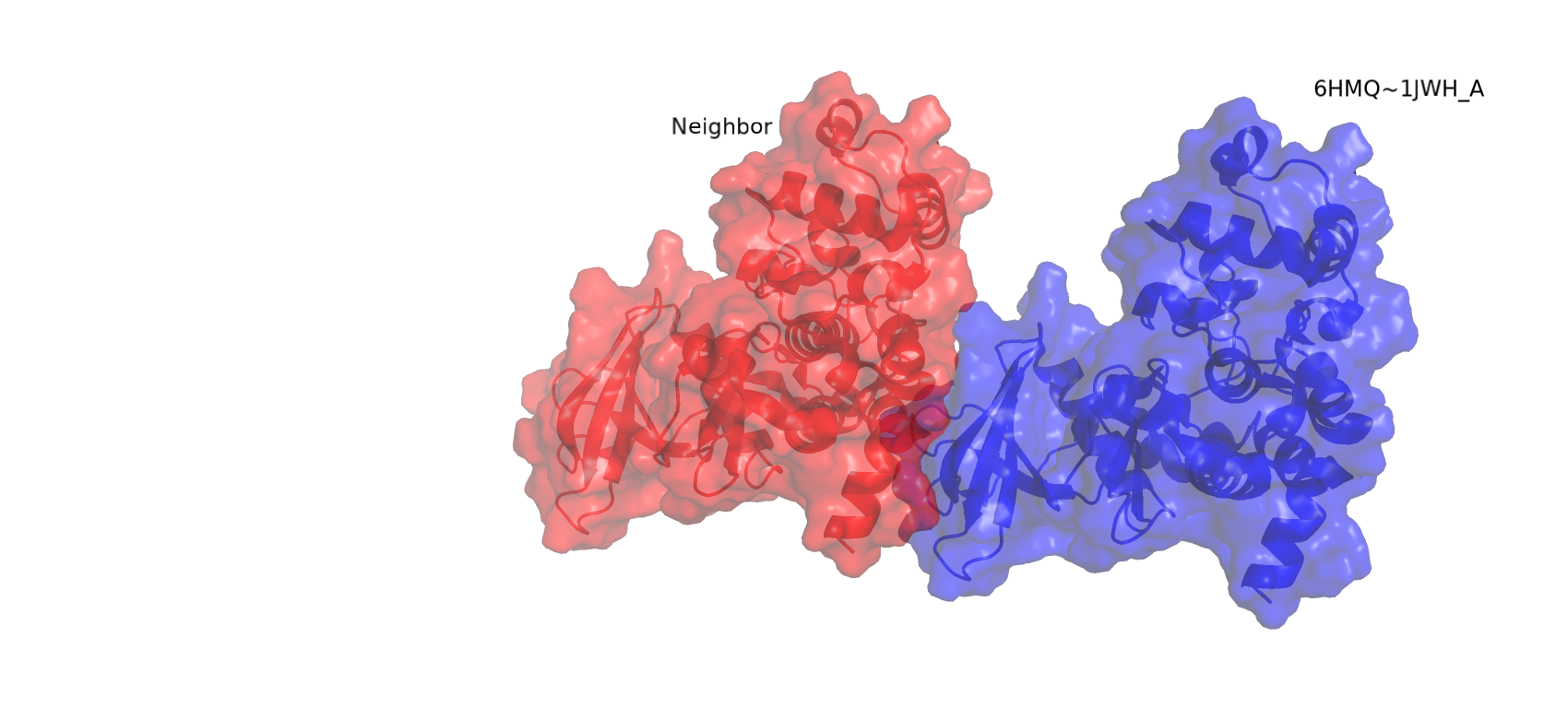
Рисунок 12. 6HMQ с одним из своих соседей.