Остовные водородные связи в α-спирали и β-листе
Водородные связи - главные взаимодействия при образовании вторичной структуры белка: α-спирали и β-листа. Для образования водородной связи необходимо наличие водорода, зажатого между двумя электроотрицательными атомами, тогда один из электроотрицательных атомов образует с ним дополнительную связь, тем самым этот атом водорода обобществляется. Схема образования водородной связи представлена на рисунке 1.
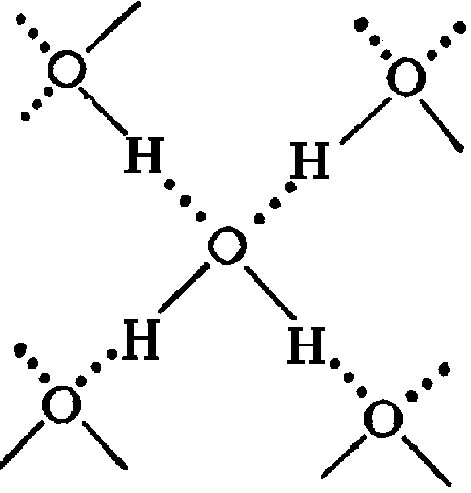
Рисунок 1. Схема образования водородной связи.
В данном белке, предполагаемой Zn-зависимлй пептидазе, также есть водородные связи, участвующие в образовании вторичной структуры белка. Сначала рассмотрим образование α-спирали. Её структура с выделенными водородными связами приведена на рисунке 2.
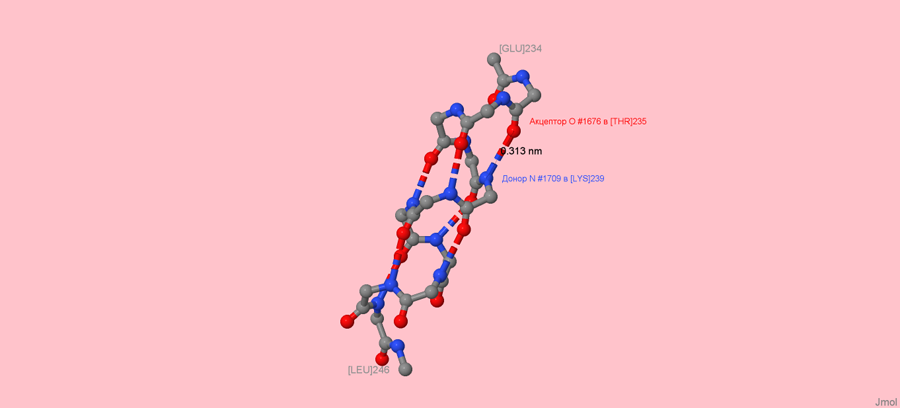
Рисунок 2. Одна из α-спиралей белка 3C37 с отмеченными водородными связами.
Из рисунка видно, что данная α-спираль образована 7-ю водородными связями. Обычно водородные связи не имеют длину более 3,5 нм. И действительно, измерив связь, обазовавшуюся между акцептором протона - кислородом треонина (Thr235) и донором - азотом лизина (Lys239), я получила результат в 0,313 нм (< 3,5 нм). Остальные водородные связи имеют примерно такую же длину.
Теперь приступим к изучения β-листа данного белка. Его структура изображена на рисунке 3.
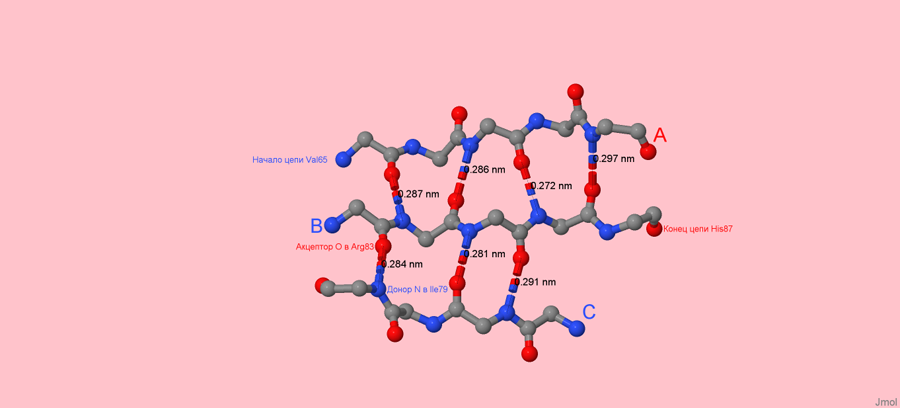
Рисунок 3. Одна из β-листов белка 3C37 с отмеченными водородными связами.
Как и в случае с α-спираль, образование вторичной структуры произошло с помощью 7-ми водородных связей. Их длины не превышают 0,3 нм. Также из рисунка можно заметить, что данный β-лист состоит из 2 паралелльных (A и B) и одного антипараллельного тяжа (С). На связь параллельных тяжей ушло 4 водородные свзи, на связь антипараллельных - 2.
В этом практикуме было дополнительное задание - вычисление шага спирали и вычисление количества аминокислотных остатков, приходящихся на виток спирали. На рисунке 4 изображена альфа-спираль, которую я выбрала для выполнения этого задания. На нём также отмечено, что шаг спирали в нм равен 0,528, что при переводе в ангстремы становится 5,28 А.
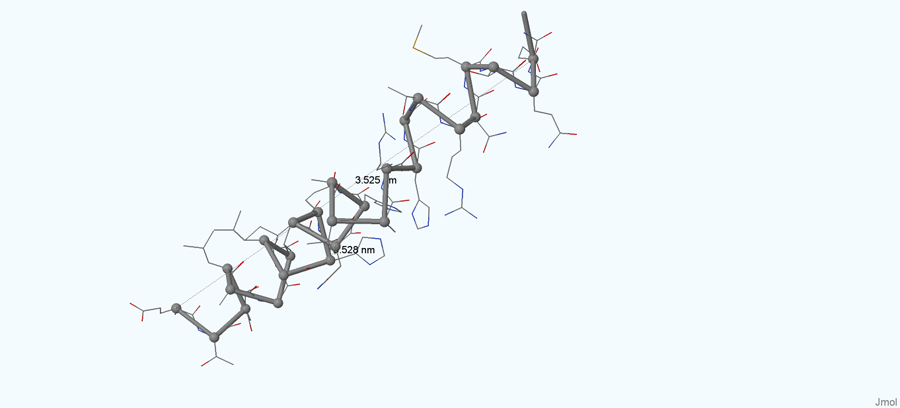
Рисунок 4.Изображение альфа-спирали с отмеченным шагом.
Шаг спирали можно рассчитать, поделив расстояние по оси спирали от первого до последнего атомов, на количество витков: 3,525/7=0,5036 нм = 5,036 А. Это среднее значение шага спирали. А чтобы найти число аминокислот на витке, нужно общее число аминокислот в спирали поделить на число витков: 27/7=3,85.
Дата последнего изменения: 17.03.2014
