Cравнение структур, полученных методами РСА и ЯМР
Выбор белка
Для выполнения этого практикума был выбран белок, для которого есть и структура, полученная методом РСА, и структура, полученная с помощью ЯМР. Этим белком стала сериновая протеаза PB92 из Bacillus alcalophilus (PСА-структура 1IAV и ЯМР-структура 1AH2). В структуре, полученной методом ЯМР описывается 18 моделей, разрешение РСА-структуры составляет 1.8 Å. Укладки для обеих рассматриваемых структур приводятся на рисунке 1, видно, что они сходны. 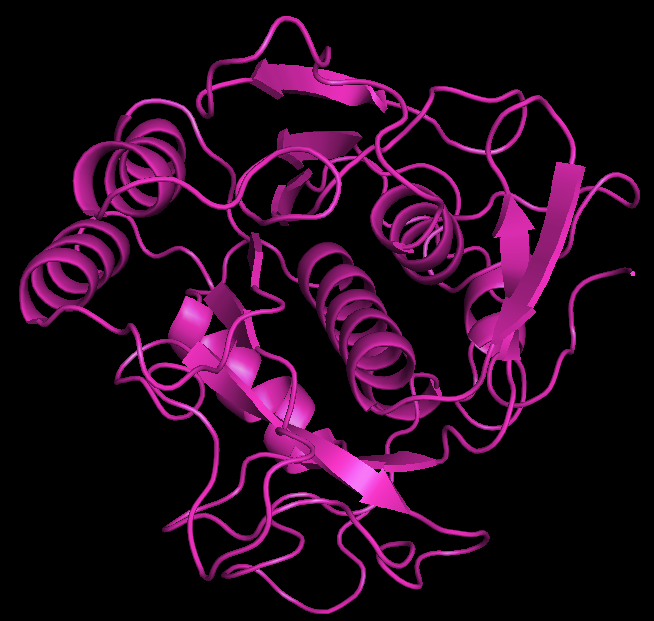 |
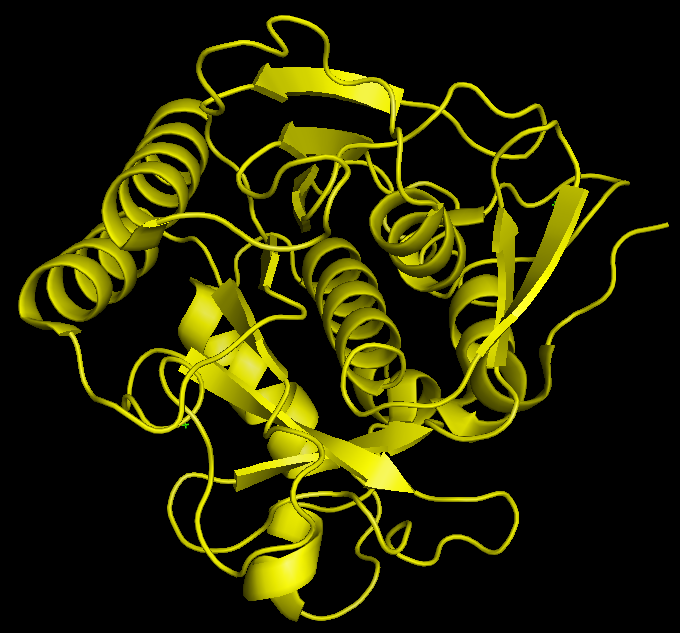 |
Рис. 1 Общий вид укладки белка в РСА-структуре (слева) и одной из ЯМР-структур (справа). |
|
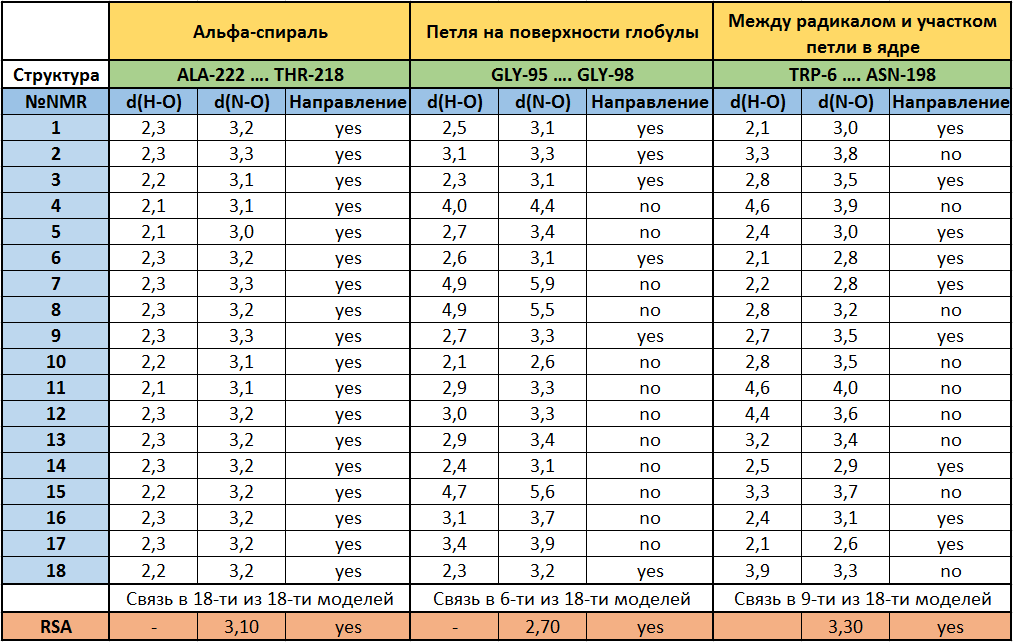
Далее были выбраны три связи, длины которых анализировались. Связи между боковыми радикалами аминокислот в ядре белка не обнаружилось, в связи с этим была выбрана связь между боковым радикалом триптофана (NH в индольном кольце) и участком основной цепи (с=о группой аспарагина), не входящим в состав ни одного элемента вторичной структуры. В таблице 1 приводится первичная информация по измерению выбранных связей во обеих структурах (18 моделей ЯМР-структуры и РСА-структура). Для каждой связи в ЯМР структуре проводили два измерения: между донором и акцептором (столбец d(N-O)) и между водородом и акцептором (столбец d(H-O)), а кроме того был визуально оценен угол отклонения предполагаемой водородной связи от оси связи H-донор. Если он был больше порядка 50-ти градусов, то считалось, что такая связь не появится и в третий столбец (направление) писалось "no". Затем данные из таблицы 1 были проанализированы и сведены в таблицу 2.
Таб. 1 Измеренные параметры трёх водородных связей в структурах белка, полученных различными методами. |
 |
Таб. 2 Сводная таблица параметров трёх водородных связей в структуре белка. |
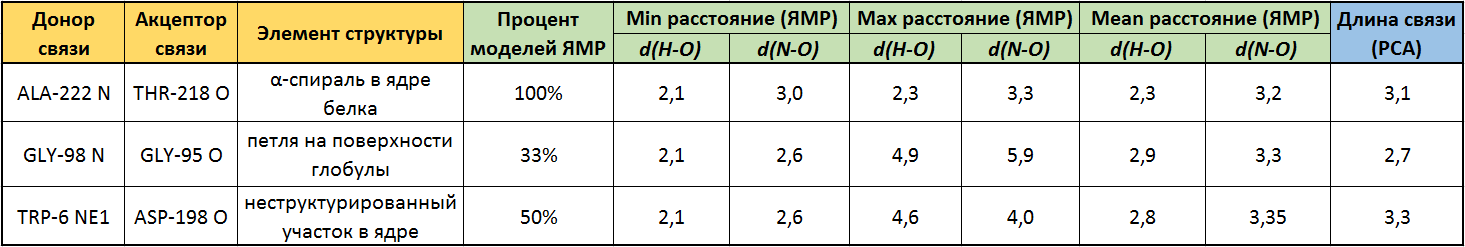 |
На основе анализа полученных данных мною были сделаны следующие выводы:
- Водородные связи значительно более точно можно описать при помощи ЯМР, поскольку в этом методе определяются атомы водорода, в методе РСА же приходится предполагать наличие связи эмпирически на основе неких априорных знаний об их длинах и характерных углах.
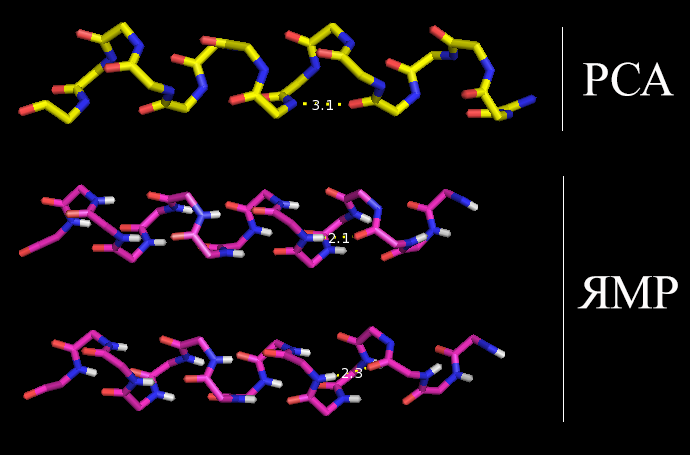
- Водородные связи во вторичных структурах внутри белка наиболее стабильны, они имеют примерно одинаковую длину во всех моделях ЯМР и в РСА-структуре. На рисунке 2 показана альфа-спираль, для которой проводилось измерение для РСА-структуры и двух ЯМР структур, давших минимальное и максимальное значения расстояния, водородная связь показана жёлтым пунктиром.
- Связи образующиеся в петлях на поверхности структуры между конкретными остатками более "подвижны", они могут возникать и исчезать при колебаниях белка в растворе, что отражено в том, что не во всех ЯМР-моделях они присутствуют. На рисунке 3 показана петля, в которой определялось наличие связи четырёх ЯМР-моделей. Видно, что изменяется положение петли и связь может исчезать и появляться.
- Связи между остатками, не входящими в элементы вторичной структуры, в ядре белка занимают некоторое промежуточное положение по подвижности по сравнению с двумя ситуациями, рассмотренными выше.
 |
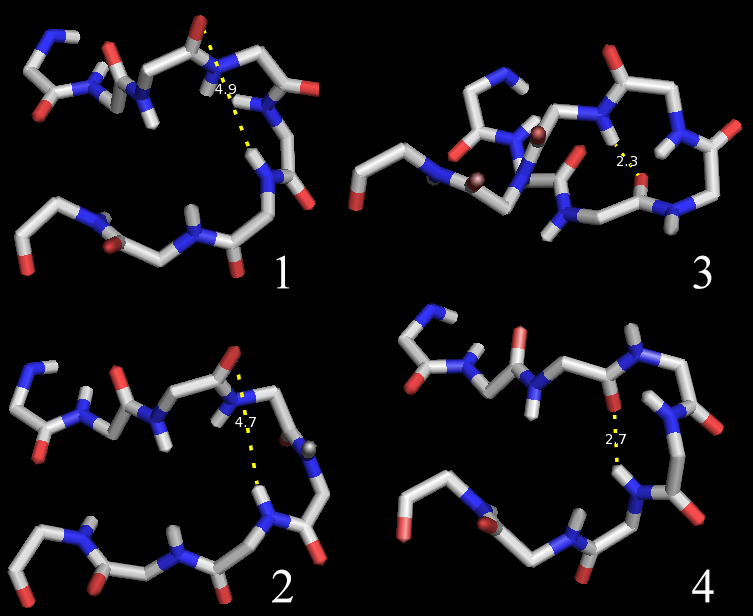 |
Рис. 2 Водородная связь внутри элемента вторичной структуры (альфа-спирали) белка. |
Рис. 3 Водородные связи в птле на поверхности белка в различных моделях ЯМР. Видны разные расстояния между акцептором и атомом водорода: 1-2 большие (не образуется водородная связь) и 3-4 малые (образуется водородная связь). |
Дата последнего обновления: 24.12.2015
© Dmitry Travin, 2015