Пространственная структура ABC-транспортерного периплазматического связывающего аминокислоты белка

|

|

|

|

|

|

|

|

|
В качестве объекта изучения мне был предложен белок - ABC-транспортерный периплазматический связывающий аминокислоты белок (ABC transporter periplasmic binding protein, amino acid), также называемый растворимым рецептором L-цистеина бактерии Neisseria gonorrhoeae (the solute receptors for L-cysteine of Neisseria gonorrhoeae). Основную информацию о нем можно почерпнуть из базы данных PDB. Ниже представлены основные сведения о нем.
- В базе данных PDB данный белок имеет идентификатор 2YJP.
- В pdb-файле, содержащем информацию по данному белку, он имеет два названия: ABC-транспортерный периплазматический связывающий аминокислоты белок (ABC transporter periplasmic binding protein, amino acid) и растворимый рецептор L-цистеина бактерии Neisseria gonorrhoeae (the solute receptors for L-cysteine of Neisseria gonorrhoeae). Согласно информации на странице этого белка на сайте PDB, первое название он получил при секвенировании его последовательности из генома Neisseria gonorrhoeae, поскольку был гомологичен ABC-транспортерным белкам, связывающим цистеин и цистин, а после рентгенструктурного анализа и подтвеждения его функций он получил второе название.
- В pdb-файле дана информация о трех цепях данного белка - A, B и C. Они идентичны по последовательности аминокислот, однако различаются по набору и расположению приписанных к ним лигандов. Следует отметить, что последовательность аминокислот в данных цепях несколько отличается от последовательности аминокислот ABC-транспортерного периплазматического связывающего аминокислоты белка, бывшего объектом изучения в первом семестре. Это заметно при проведении выравнивания последовательности аминокислот этих цепей и белка. Согласно выравниванию, у объекта изучения первого семестра и данного белка не совпедают первые 16 амнокислот, кроме самой первой (метионина). Однако, следует заметить, что при детальном изучении структуры данного белка в визуализаторе Jmol, выясняется, что каждая белковая цепь начинается вовсне не с метионина, а с аланина, причем цепи B и С не имеют аминокислотных остатков с номерами меньше чем 39, а цепь A начинается с аминокислотного остатка нормер 38. Отсюда можно сделать предположение, что первые аминокислотные остатки отрезаются от цепей белка при образовании третичной структуры после трансляции, и поэтому цепи, представленные в pdb-файле, неотличимы от белка из первого семестра.
- Согласно pdb-файлу, в белковый комплекс входят молекулы цистеина, 1,2-этандиола и ионы цинка. Цистеинов всего 3 - они находятся в центре каждной из белковых субъединиц. Ионов цинка 8, они связаны с различными частями цепей, и через некоторые из них осуществляется связь двух разных белковых субъединиц. молекулы 1,2-этандиола располагаются по переферии и не имеют связей с белком. Вероятно, они могут быть артефактами.
Ниже представлены выдержки из pdb-файла, раскрывающие ключевые особенности строения белка.
SOURCE ORGANISM_SCIENTIFIC: NEISSERIA GONORRHOEAE;
COMPND MOLECULE: PUTATIVE ABC TRANSPORTER, PERIPLASMIC BINDING PROTEIN, AMINO ACID;
COMPND CHAIN: A, B, C;
COMPND SYNONYM: SOLUTE RECEPTORS FOR L-CYSTEINE;
HETNAM CYS CYSTEINE
HETNAM ZN ZINC ION
HETNAM EDO 1,2-ETHANEDIOL
EXPDTA X-RAY DIFFRACTION
REMARK 2 RESOLUTION. 2.26 ANGSTROMS.
Как уже говорилось выше, белок состоит из трех независимых цепей. Каждая из них на сайте PDB обозначена отдельной биологической единицей. Вместе они образуют элементарную ассиметрическую ячейку.
Исследование белка проводилось методом рентгеноструктурного анализа (X-Ray diffraction) с разрешением 2.26 ангстрем.
На рис.1 представлена пространственная структура ABC-транспортерного периплазматического связывающего аминокислоты белка. Данное изображение получено при помощи скрипта Maslova.spt .

Рис.1. пространственная структура ABC-транспортерного периплазматического связывающего аминокислоты белка. 3 различные цепи белка отображены, соответственно, желтым, красным и зеленым цветом. α- и β-структуры изображены в виде широких лент, α-спирали темнее, β-структуры светлее. Участки цепи, не входящие во вторичную структуру, отображены проволочной моделью, входящие в них атомы изображены шариками. Ионы цинка - фиолетовые, молекулы 1,2-этандиола - голубые, цистеин - черный, молекулы воды - синие.
Затем при помощи Jmol были построены пространственные структуры трех биологических единиц белка. На рис.2 приведено полученное изображение.
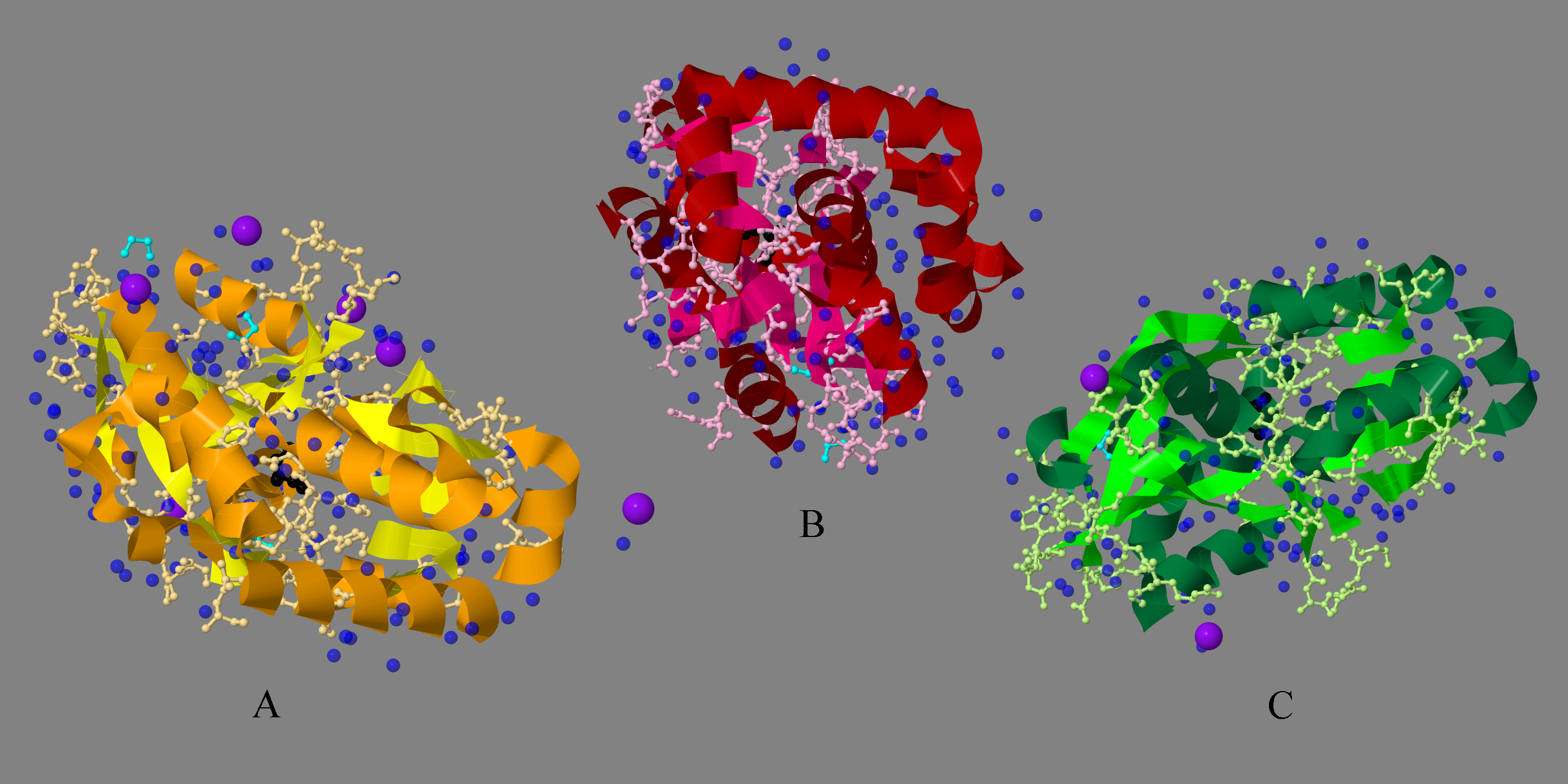
Рис.2. Биологические единицы ABC-транспортерного периплазматического связывающего аминокислоты белка. Билогическая единица №1 изображена желтым цветом, №2 - красным, №3 - зеленым. Ионы цинка - фиолетовые, молекулы 1,2-этандиола - голубые, цистеин - черный, молекулы воды - синие.
Для того, чтобы проследить направление цепей белка от N' до C' конца в каждой из биологических единиц, был написан скрипт на языке Python, создающий соответствующий spt-скрипт для получения изображения в Jmol. На рис.3 предстален результат работы данного скрипта.
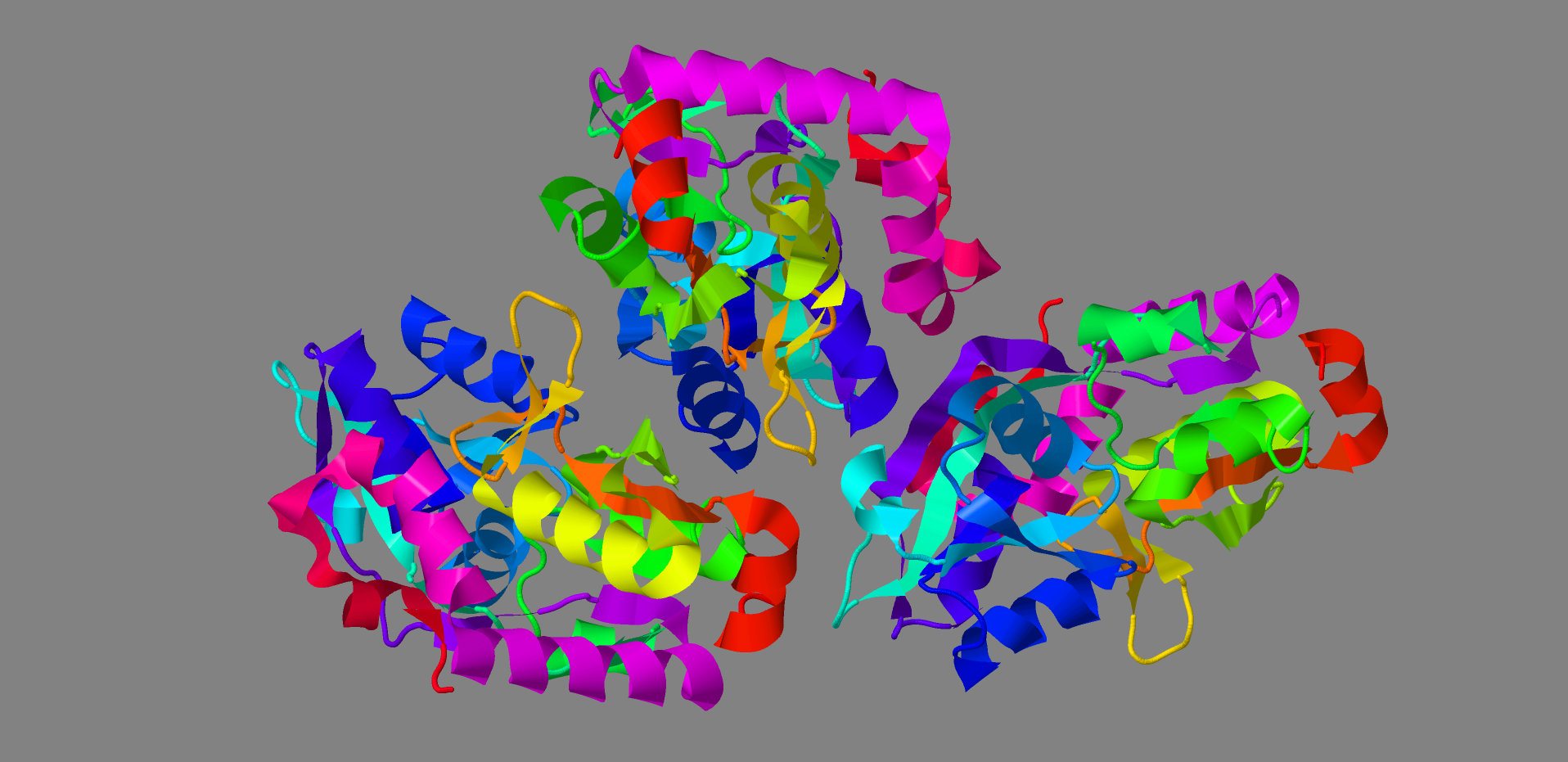
Рис.3. Направление цепей ABC-транспортерного периплазматического связывающего аминокислоты белка. За направление от N' к C' концу принят переход цвета красный-желтый-зеленый-голубой-синий-фиолетовый-красный.
Связанные отчеты:
ABC-транспортерный периплазматический связывающий аминокислоты белок
Последнее изменение: 23.02.2014