Блок 2
Отчет по структуре PDB 3FFU
1. Структура в целом
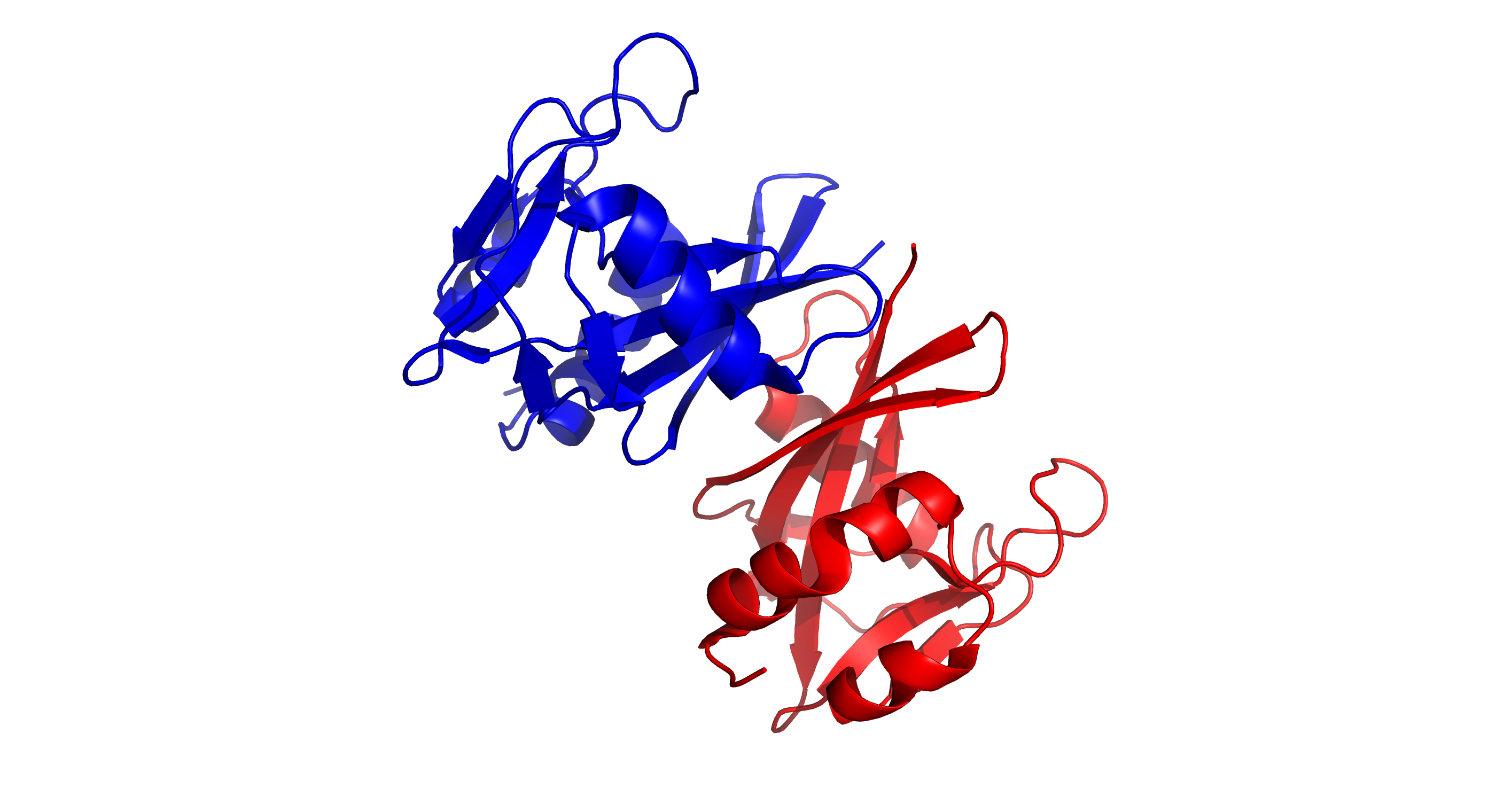
Рисунок 1. Общий вид структуры 3FFU (cartoon). Цепь А окрашена красным цветом, цепь В - синим цветом.
| Тип макромолекул | Белок (гидролаза) |
|---|---|
| Количество полимерных цепей | 2 цепи: A и B (идентичны по последовательности) |
| Биологическая единица | Димер из двух цепей (A и B) |
| Организм | Bdellovibrio bacteriovorus (штамм HD100) |
2. Вторичная структура
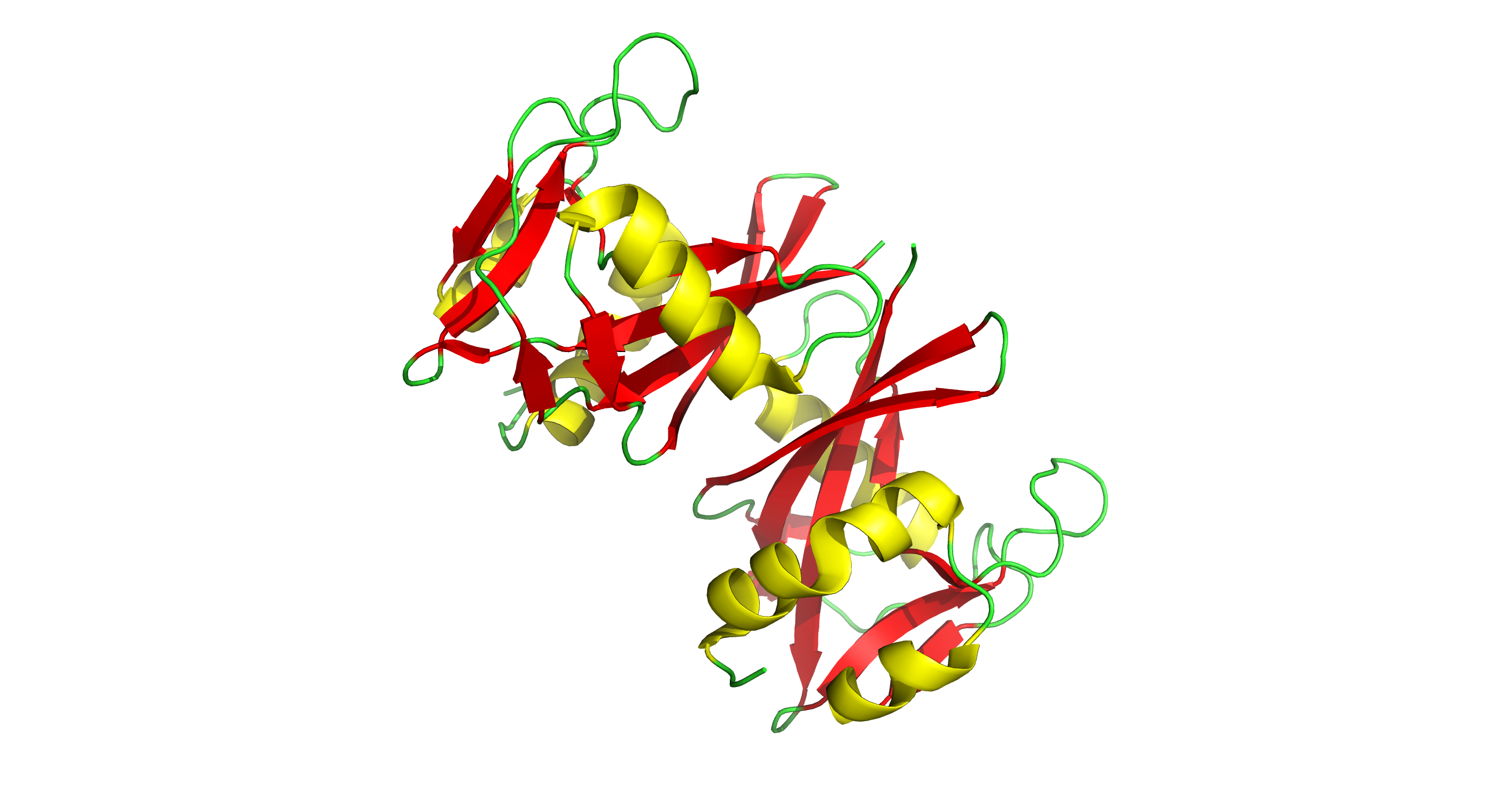
Рисунок 2. Вторичная структура белка 3FFU. Желтым цветом показаны α-спирали, красным — β-тяжи, зеленым — петли. В структуре примерно поровну представлены спирали и тяжи.
3. Отдельные цепи
- UniProt ID: Q6MPX4
- Название: BdRppH
- Функция: РНК-пирофосфогидролаза
- Мутации: Нет
- Модифицированные остатки: Нет
- UniProt ID: Q6MPX4
- Название: BdRppH
- Функция: РНК-пирофосфогидролаза
- Мутации: Нет
- Модифицированные остатки: Нет
5. Малые молекулы (лиганды)
| Краткое название | Полное название | Количество |
|---|---|---|
| GTP | GUANOSINE-5'-TRIPHOSPHATE | 2 молекулы (по одной в цепях A и B) |
| MG | MAGNESIUM ION | 6 ионов (3 в цепи A, 3 в цепи B) |
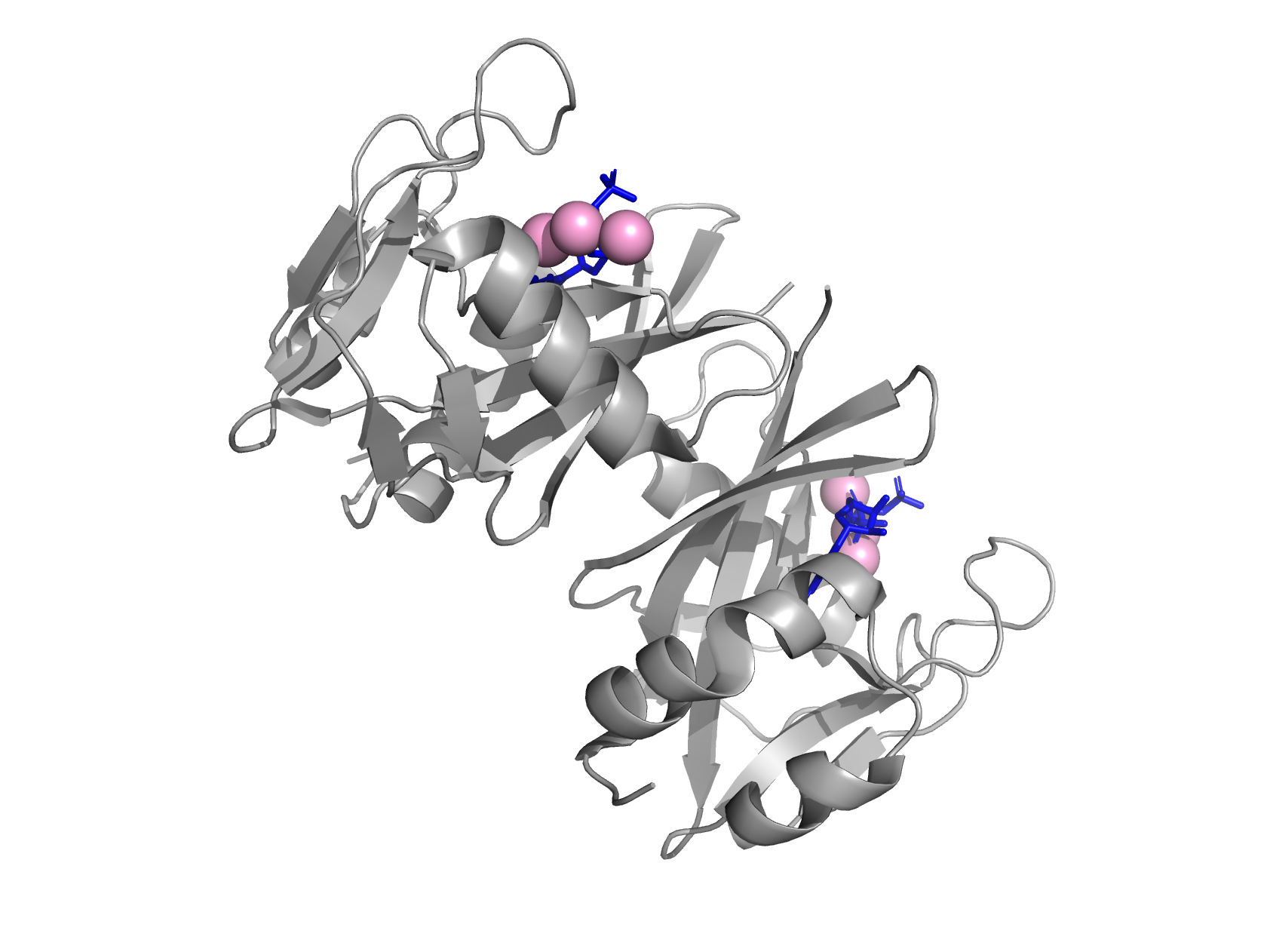
Рисунок 3а. Молекула GTP в структуре 3FFU.
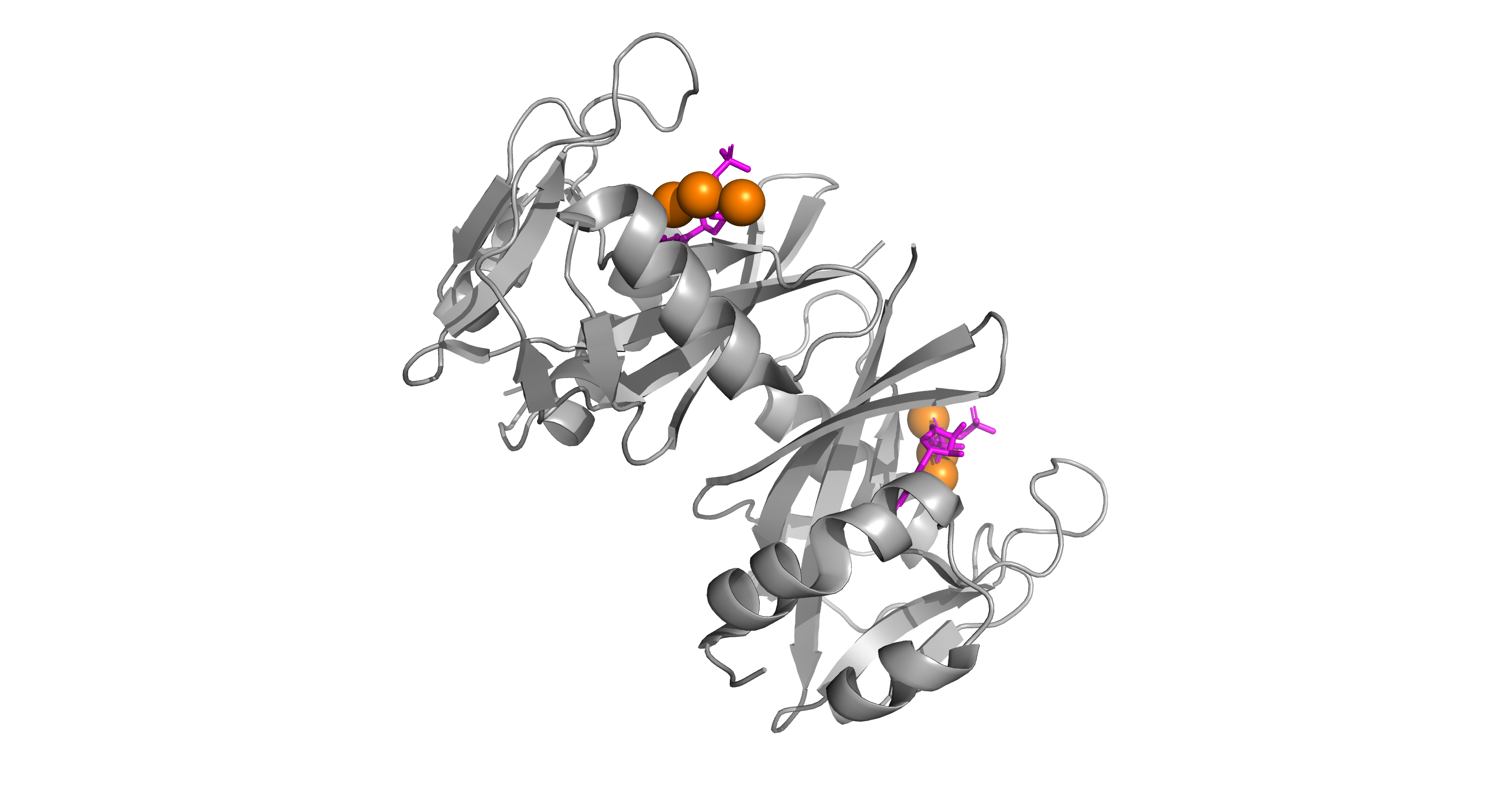
Рисунок 3б. Ионы магния в структуре 3FFU.
Файл со строками HETATM для молекул GTP и MG:
Скачать ligands_3FFU.txt4. Взаимодействия между аминокислотными остатками
4.1 Водородная связь (остов-остов)
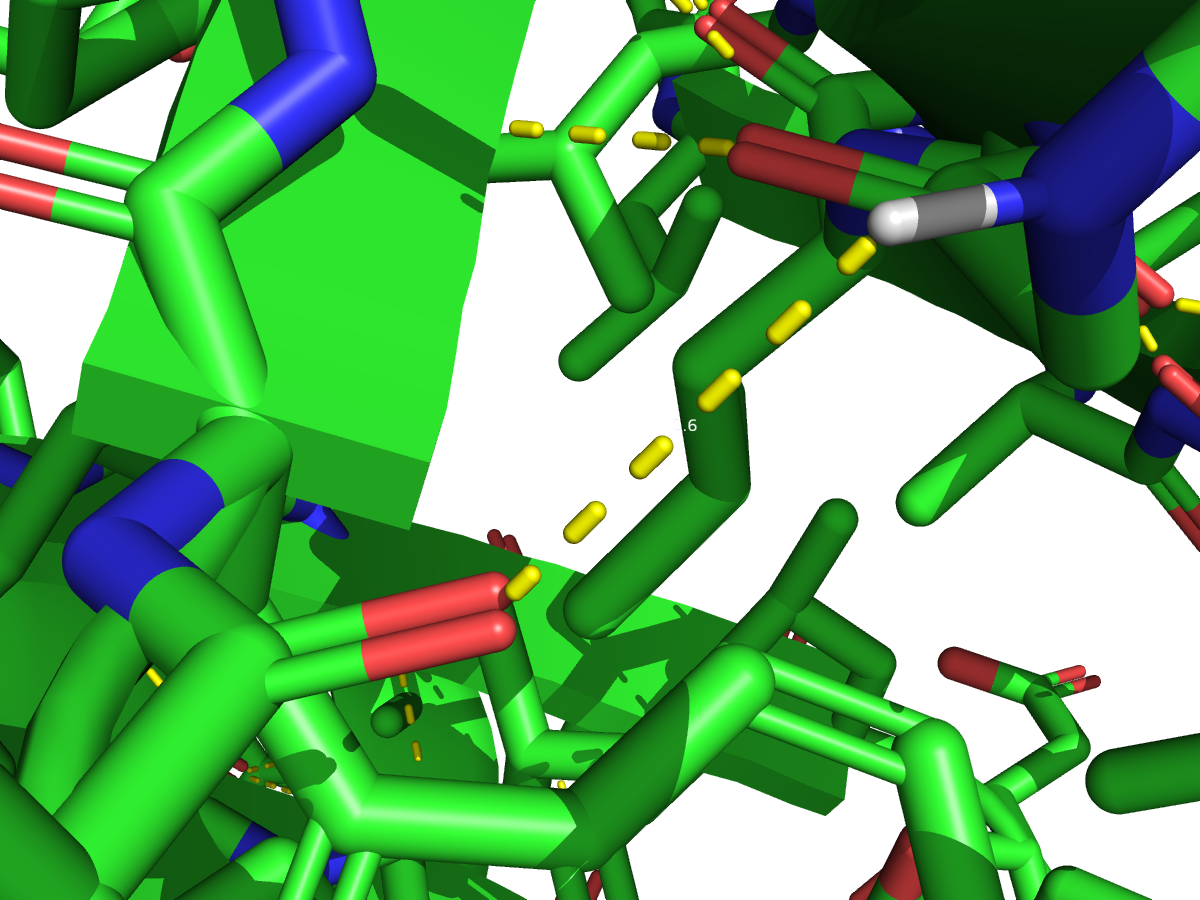
Рисунок 4. Водородная связь между атомами остова GLY 96 (H10) и HIS 20 (O). Расстояние составляет 2.6 Å.
4.2 Водородная связь (боковые радикалы)
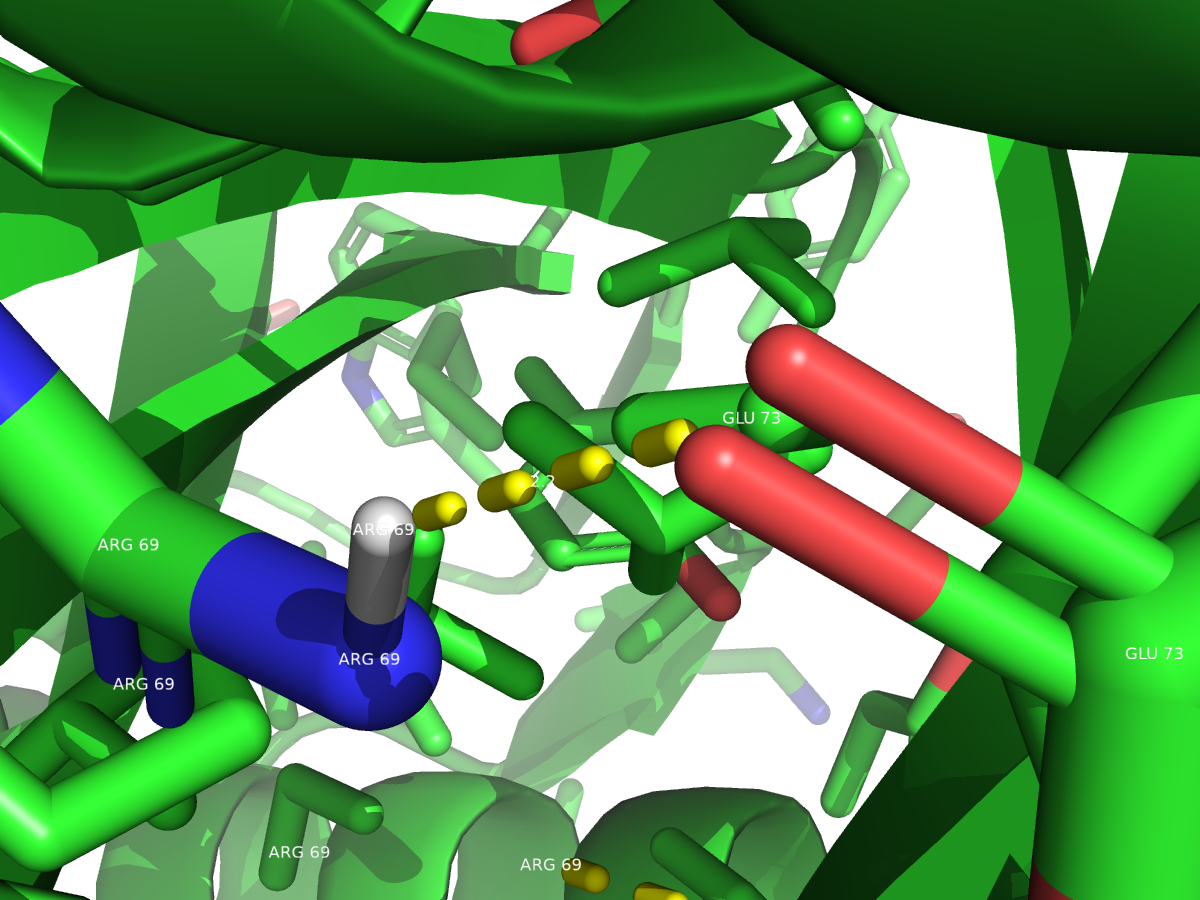
Рисунок 5. Водородная связь между боковыми радикалами ARG 69 (H11) и GLU 73 (OE1). Расстояние составляет 2.2 Å.
4.3 Солевой мостик

Рисунок 6. Солевой мостик между боковыми радикалами GLU 120 (OE1) и ARG 130 (H10). Расстояние составляет 2.2 Å.
4.4 Дисульфидная связь
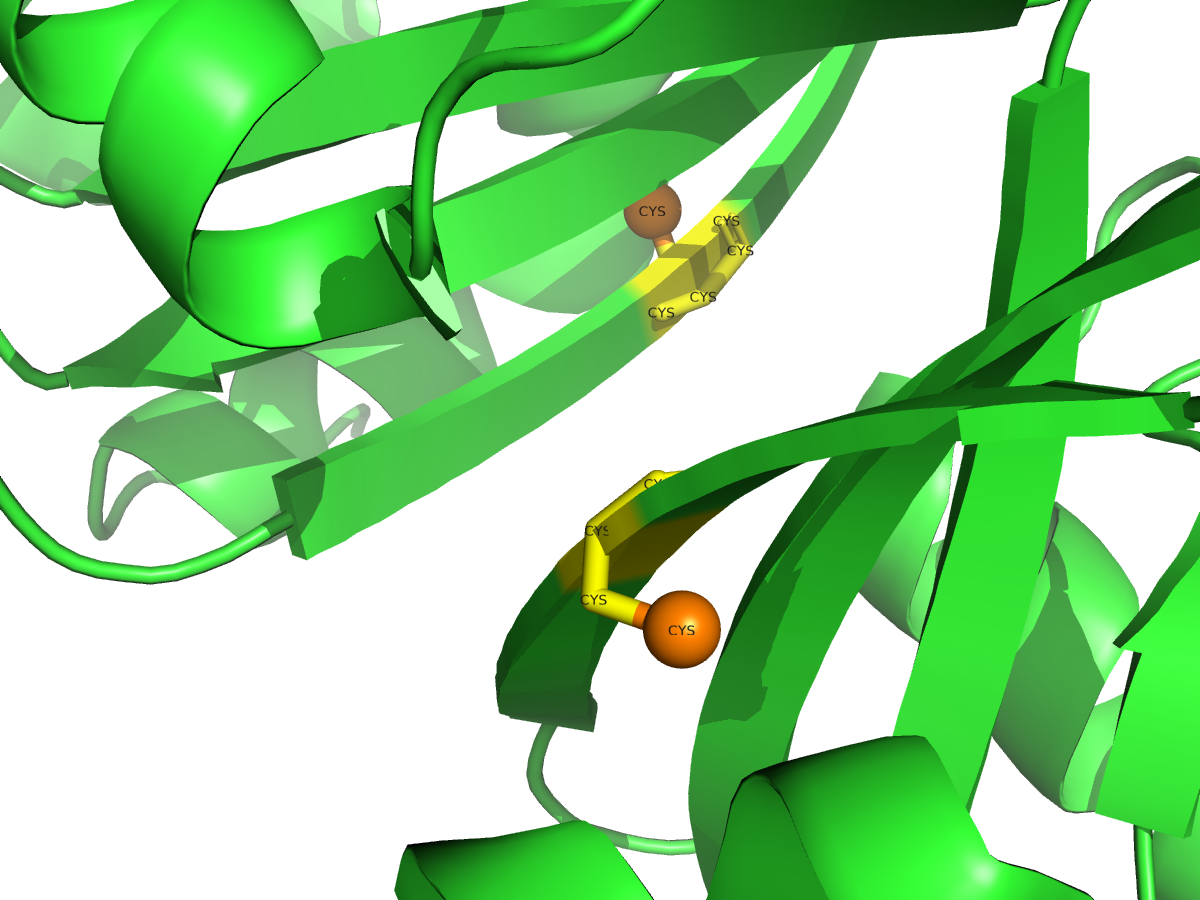
Рисунок 7. Расположение цистеинов в белке 3ffu. Атомы серы (SG) показаны оранжевыми сферами. Дисульфидные связи отсутствуют.
4.5 Стекинг (ароматическое взаимодействие)
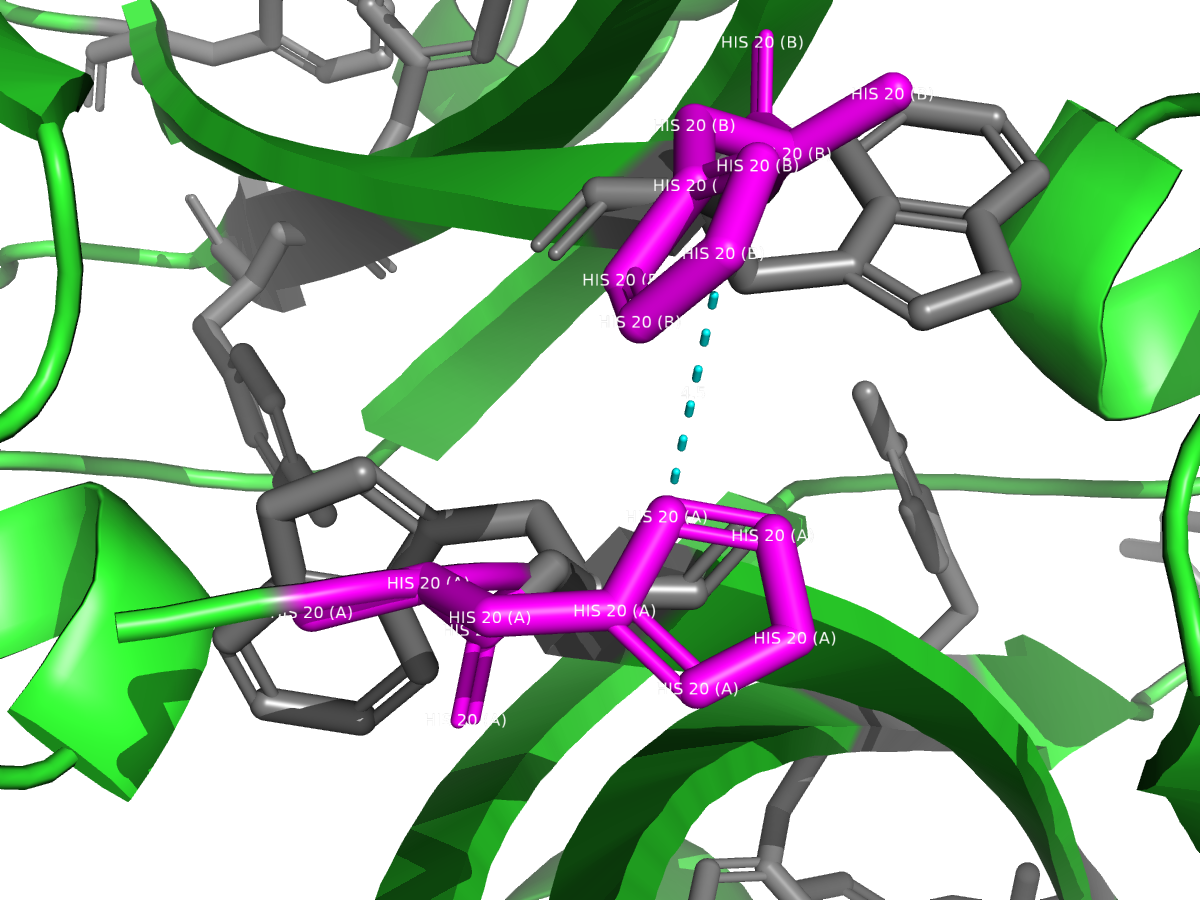
Рисунок 8. Ароматический стекинг между гистидинами HIS 20 цепи A и HIS 20 цепи B. Расстояние между центрами колец составляет 4.5 Å.