
|
Учебный сайт Алены Корягиной |

|
Главная |
Oбо мне |
Cеместры |
Cсылки |
Гидрофобное взаимодействие и гидрофобные кластеры в белке АТФазы VirB4
Гидрофобность — это физическое свойство молекулы (атома, группы) обладая которым молекула стремиться избегать контакта с водой, то есть при растворении в воде гидрофобные молекулы стремяться занять такое положение в пространстве, чтобы площадь контакта воды и этих молекул была минимальной. В молекуле белка это свойство может выражается в том, что гидрофобные боковые группы аминокислот объединяются друг с другом, образуя так называемый гидрофобный кластер, а вокруг него располагаются гидрофильные группы, которые стремятся присоединить воду, таким образом, получается, что гидрофобные молекулы изолированы от водного раствора. Это явление называется гидрофобным взаимодействием. Гидрофобное взаимодействие является одним из основных факторов, определяющих третичную и четвертичную структуру белковой молекулы, так как именно оно играет важную роль в упаковке белка и его взаимодействии с другими доменами и окружающей средой.
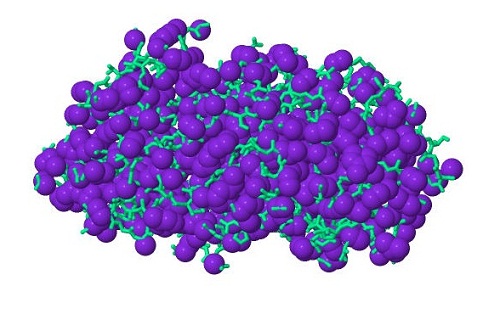
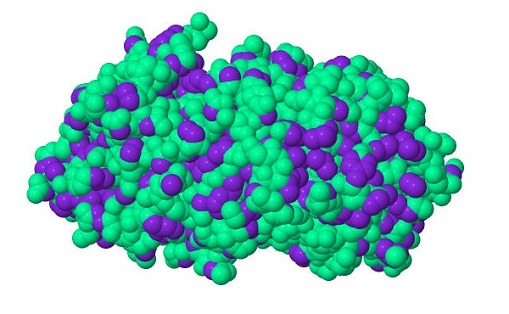
На примере цепи В из белка VirB4 АТФазы продемонстрируем гидрофобное взаимодействие. В белке гидрофобными являются все атомы углерода, не свящанные с полярными атомами, и атомы серы из цистеина и метионина. С помощью этого скрипта (скачать скрипт) были определены все гидрофобные атомы и изображены в полноатомной модели фиолетового цвета, все остальные атомы представлены в проволожной модели светло-целеного цвета (рис.1). На рисунке 1 видно, что все гидрофобные атомы сгруппированы и образуют гидрофобный кластер, состоящий из 874 атомов. Если представить негидрофобные атомы в полноатомной модели (рис.2), то станет очевидно, что гидрофобный кластер сверху покрыт гидрофильными атомами, что соответствует вышеописанной ситуации, а значит этот белок будет растворим в воде.
|
|
Рис.1. Распределение гидрофильных и гидрофобных атомов в цепи В белка VirB4 АТФазы. Гидрофобный кластер. Гидрофобные атомы представлены в виде сфер, радиус каждой сферы соответствует Ван-дер-Ваальсовому радиусу атома. Цвет гидрофобных атомов — фиолетовый. Все остальные атомы представлены светло-зелым цветом в проволочной модели. Рисунок получен с помощью программы Jmol. |
Рис.2. Распределение гидрофильных и гидрофобных атомов в цепи В белка VirB4 АТФазы. Все атомы представлены в иде сфер, радиус каждой сферы соответствует Ван-дер-Ваальсовому радиусу атома. Цвет гидрофобных атомов — фиолетовый, остальных атомов — светло-зелый. Рисунок получен с помощью программы Jmol. |
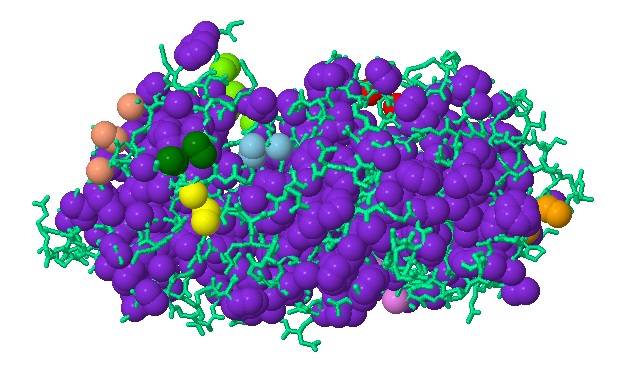
С помощью сервиса CluD была проведена аналогичная работа по выявлению гидрофобных кластеров в молекуле белка VirB4 АТФазы (цепь В). Было обнаружено 9 гидрофобных кластеров. Один из них очень большой (около 850 атомов), его называют гидрофобным ядром. Другие восемь гидрофобных кластеров имеют совсем небольшой размер: 7 атомов., два по 4 атомов и четыре по 3 атомов. (см. рис.3).
|
Рис.3. Гидрофобные кластеры в цепи В белка VirB4 АТФазы. Гидрофобные атомы представлены в виде сфер, радиус каждой сферы соответствует Ван-дер-Ваальсовому радиусу атома. Цвет гидрофобного ядра — фиолетовый. Все гидрофобные кластеры выделены различными цветами. Остальные атомы представлены светло-зелым цветом в проволочной модели. Рисунок получен с помощью сервиса CluD.
Смотрите также другие внутримолекулярные взаимодействия:
Дата последнего изменения: 29.05.2014