
|
Учебный сайт Алены Корягиной |

|
Главная |
Oбо мне |
Cеместры |
Cсылки |
Внутримолекулярные взаимодействия боковых цепей в белке АТФазы VirB4 - солевые мостики и водородные связи, не являющиеся солевыми мостиками
Благодаря таким внутримолекулярным взаимодействиям боковых цепей, как солевые мостики, водородные связи и дисульфидные мостики (рассматривается в другом разделе), формируется третичная структура белка (пространственное расположение полипептидной цепи).
Солевой мостик — химическая связь, которая образуется в белке между положительно и отрицательно заряженными атомами боковых цепей, следовательно, она может возникать между анионными группами аспартата и глутамата и катионными лизина, аргинина, гистидина.
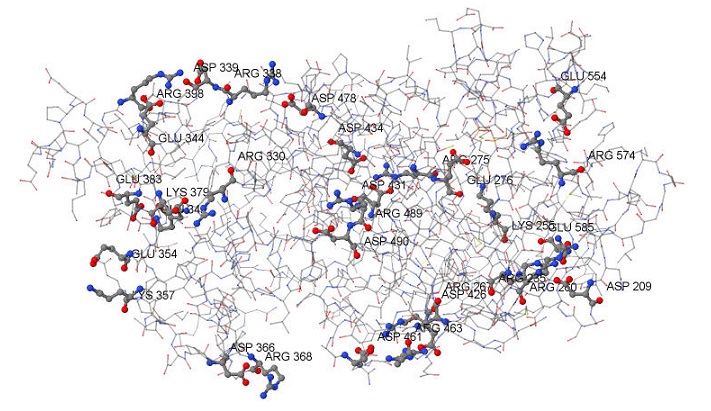
В одной цепи, цепи В, белка VirB4 АТФазы имеется 28 солевых мостиков (рис.1).
Для того чтобы найти все аминокислотные остатки, медду которыми могут возникать солевые мостики в белке VirB4 АТФазы (идентификатор в базе данных PDB 4AG5), использовался этот скрипт в программе Jmol. Вы можете скачать его здесь.
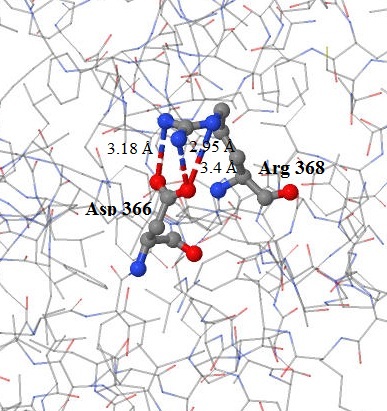
На примере взаимодействий между парой аминокислот asp 366 и arg 368, поподробнее рассмотрим строение солевых мостиков (рис.2). Здесь мы можем наблюдать 3 солевых мостика, в образовании которых участвуют все три атома азота аргининовой кислоты и два атома кислорода аспарагина. Данные солевые мостики имеют длины: 3.18 Å, 2.95 Å, 3.4 Å
|
|
Рис.1. Солевые мостики в цепи В белка VirB4 АТФазы. Раскраска атомов: серые — атомы углерода, голубые — атомы азота, красные — кислорода. Рисунок получен с помощью программы Jmol. |
Рис.2. Солевые мостики между аминокислотами asp 366 и arg 368 из белка VirB4. Раскраска атомов: серые — атомы углерода, голубые — атомы азота, красные — кислорода. Пунктиром обозначены водородные связи. Рисунок получен с помощью программы Jmol. |
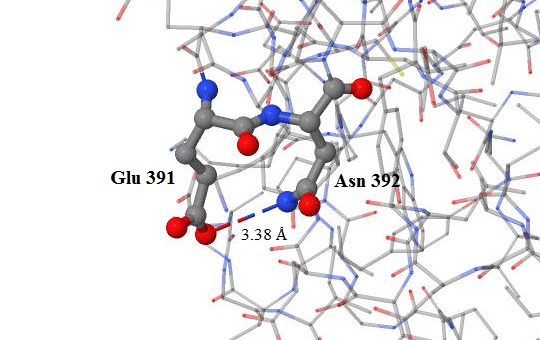
Другие внутримолекулярные взаимодействия боковых цепей,стабилизирующие третичную структуру белка, — водородные связи. Они возникают между водородом, связанным с электроотрицательным атомом, и другим электроотрицательным атомом. Например, в рассматриваемом белке VirB4 АТФазы, мы наблюдаем такую водородную связь между водородом NH2-группы аспарагина (аsn 392) и кислородом СО-группы глутаминовой кислоты (glu 391). Длина этой связи равна 3.38 А (рис.3).
Для того чтобы определить атомы, которые могут образовывать подобные водородные связи, использовалась следующая команда в программе Jmol:
select *B and sidechain and within(3.5, oxygen) and within(3.5, nitrogen)
and (oxygen or nitrogen)and not RESIDUES
|
Рис.1. Водородная связь между аминокислотами аsn 392 и glu 391 из белка VirB4 АТФазы. Раскраска атомов: серые — атомы углерода, голубые — атомы азота, красные — кислорода. Пунктиром обозначена водородная связь. Рисунок получен с помощью программы Jmol.
Смотрите также другие внутримолекулярные взаимодействия:
Дата последнего изменения: 29.05.2014