Анализ структуры PDB 2X42
1. Структура в целом
Запись 2X42 в базе PDB описывает белковую макромолекулу — фермент бета-глюкозидазу 3B (beta-glucosidase 3B), относящийся к классу гидролаз. Этот фермент катализирует гидролиз β-гликозидных связей, то есть участвует в расщеплении углеводных соединений с высвобождением глюкозы.
Структура была получена методом рентгеноструктурного анализа, разрешение структуры составляет 2,10 Å, что позволяет достаточно подробно рассматривать пространственную организацию белка и его взаимодействия с малыми молекулами.
В структуре присутствует одна полимерная цепь — цепь A. Поскольку цепь только одна, одинаковых по последовательности цепей в данной записи нет.
Биологическая единица также представлена одной цепью A, следовательно, в данной записи белок существует в виде мономера.
2. Отдельные цепи
Цепь A относится к организму Thermotoga neapolitana DSM 4359. Это термофильная бактерия, и такое происхождение хорошо согласуется со свойствами белка, поскольку изучаемая бета-глюкозидаза является термостабильным ферментом. Для получения белка в эксперименте использовали систему экспрессии Escherichia coli (кишечная палочка).
Для данной цепи указан идентификатор UniProt Q0GC07.
Название белка: beta-glucosidase / beta-glucosidase 3B (бета-глюкозидаза / бета-глюкозидаза 3B).
Функция данного белка связана с расщеплением β-гликозидных связей. Иными словами, фермент гидролизует углеводные субстраты, содержащие β-связанные остатки глюкозы, и способствует высвобождению глюкозы. Такие ферменты важны для разрушения более сложных углеводов и их дальнейшего использования клеткой.
Мутации относительно референсной последовательности UniProt: да, в структуре имеется искусственно внесённая мутация. Она обозначается как D242A, то есть в положении 242 остаток аспартата (Asp, D) заменён на аланин (Ala, A).
Это значит, что в записи представлен не белок дикого типа, а его мутантная форма. Такая замена обычно используется для изучения роли конкретного аминокислотного остатка в каталитическом механизме. В данном случае остаток Asp242 рассматривается как один из важных каталитических остатков, поэтому его замена позволяет исследовать работу активного центра.
Модифицированных аминокислотных остатков в структуре нет. В PDB-файле отсутствуют записи MODRES, следовательно, специально химически модифицированных аминокислот в составе цепи A не обнаружено.
3. Малые молекулы
В записи 2X42 присутствуют следующие малые молекулы:
- GLC — alpha-D-glucopyranose (альфа-D-глюкопираноза)
- BR — bromide ion (бромид-ион)
- HOH — вода
Это циклическая форма глюкозы. Данная молекула наиболее важна с функциональной точки зрения, так как связана с активным центром белка и позволяет анализировать особенности узнавания сахарного остатка ферментом.
Это неорганический ион брома. Он присутствует в структуре как малая молекула, однако не выглядит как обязательный природный кофактор данного фермента.
Это молекулы воды, присутствующие в кристаллической структуре. Они относятся к растворителю и характерны практически для любой структуры, полученной методом рентгеноструктурного анализа.
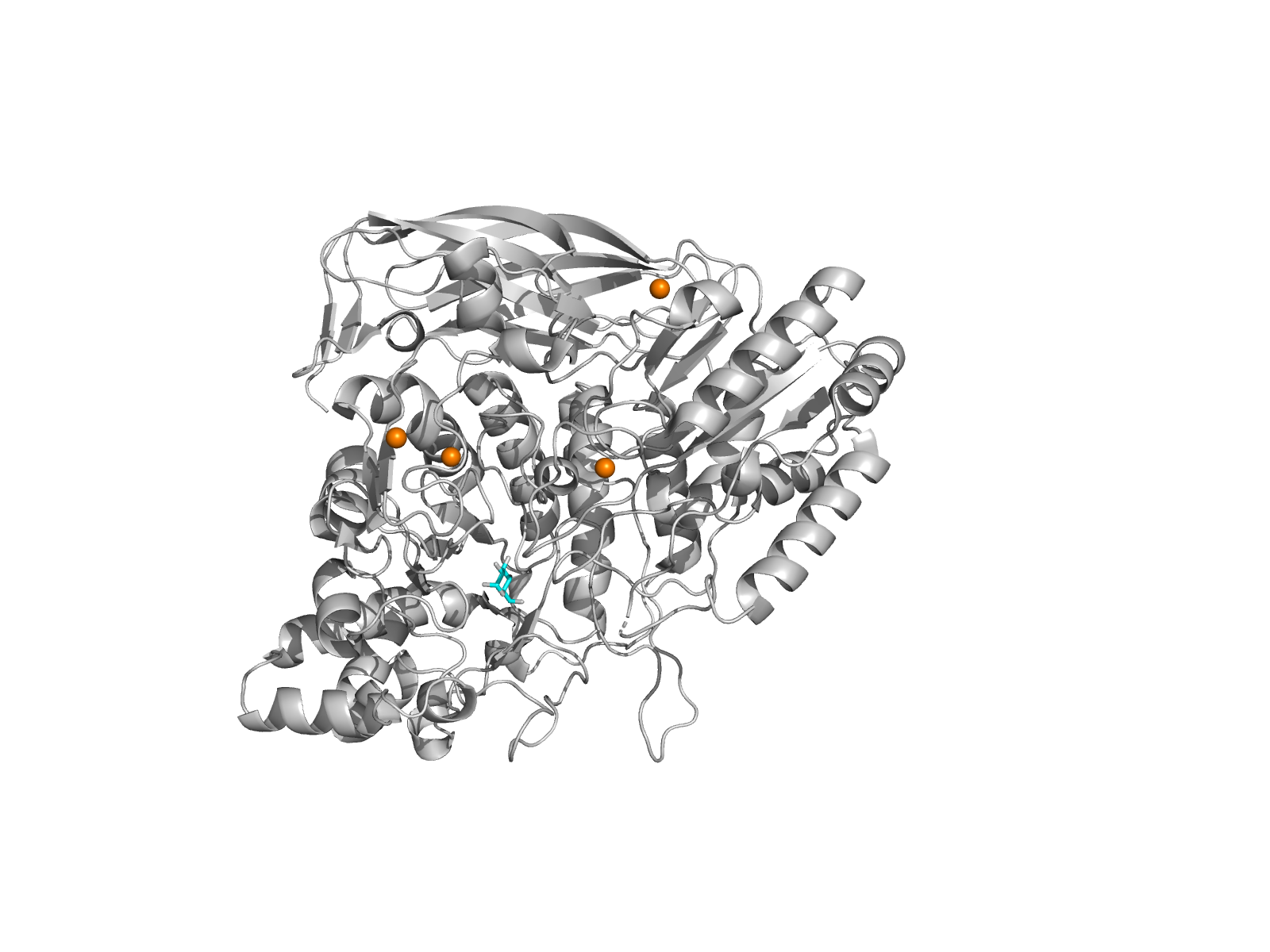
4. Файлы со строками PDB для малых молекул
- Файл со строками для GLC (альфа-D-глюкопираноза)
- Файл со строками для BR (бромид-ион)
- Файл со строками для HOH (вода)
5. Значение малых молекул в структуре
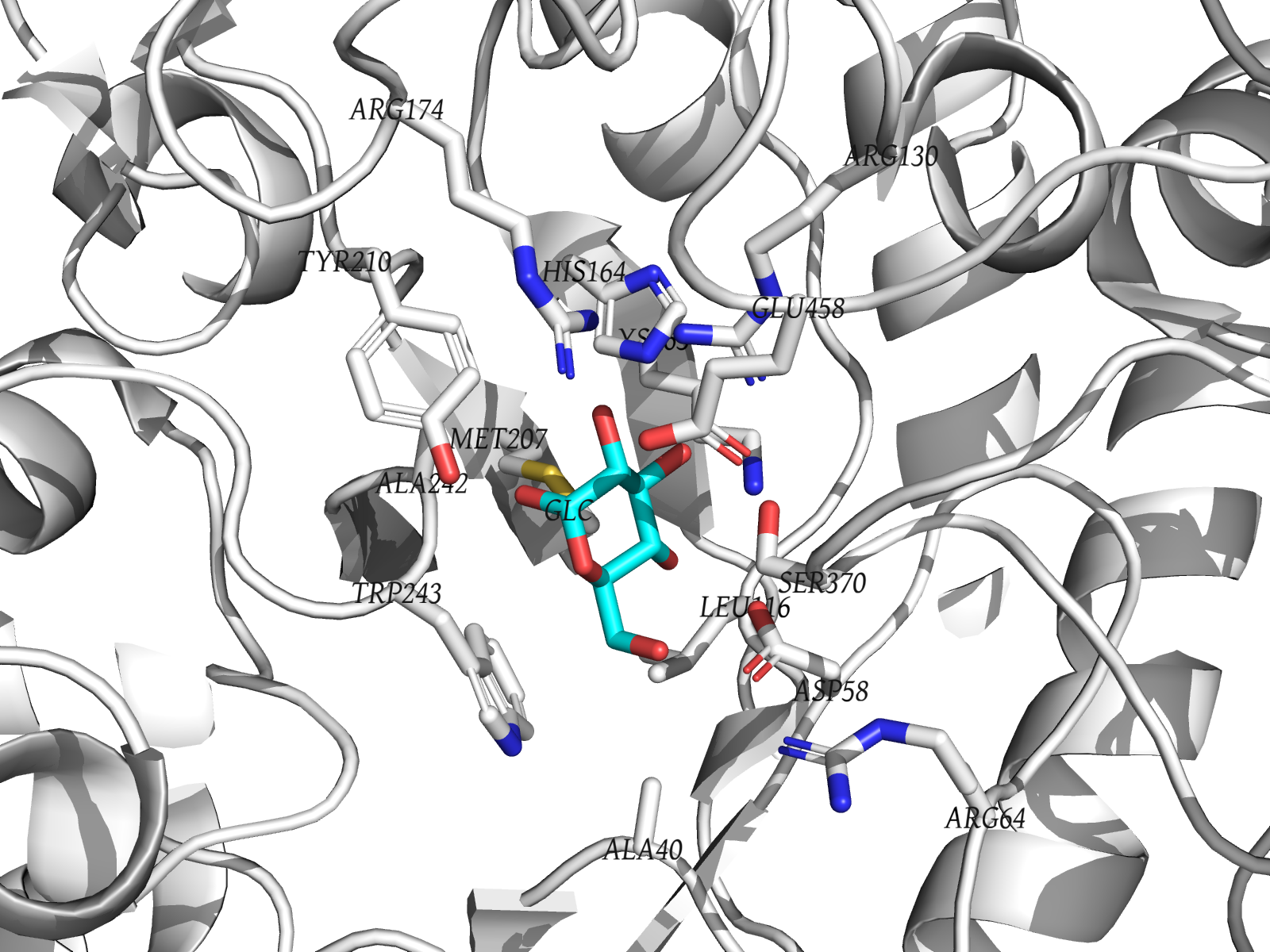
Статья, посвящённая получению и анализу данной структуры, показывает, что белок 2X42 относится к семейству GH3 (glycoside hydrolase family 3 — семейство гликозидгидролаз 3) и представляет собой термостабильную бета-глюкозидазу с трёхдоменной организацией. Активный центр белка расположен на границе доменов, а среди ключевых каталитических остатков особенно важны Asp242 и Glu458. Именно поэтому исследование мутантной формы D242A имеет особое значение: замена Asp242 на аланин позволяет оценить роль этого остатка в механизме катализа.
Теперь о малых молекулах, представленных в структуре.
GLC — альфа-D-глюкопираноза.
Эта малая молекула непосредственно связана с функцией белка. Бета-глюкозидаза катализирует расщепление соединений, в результате чего образуется глюкоза, поэтому присутствие в структуре молекулы глюкозы позволяет увидеть, как фермент связывает сахарный остаток в активном центре. Следовательно, GLC связана с выполнением функции белка и используется для анализа его субстратной специфичности и строения активного центра. При этом сама молекула глюкозы в данной структуре, вероятно, присутствует не как постоянный клеточный компонент, а как молекула, специально использованная для получения комплекса белка с лигандом. То есть она функционально осмысленна, но в кристалл, по сути, была введена искусственно для исследования связывания.
BR — бромид-ион.
Бромид-ион, скорее всего, не связан напрямую с биологической функцией белка и не является его естественным кофактором. Для бета-глюкозидаз не характерна обязательная зависимость от ионов брома. Поэтому наиболее вероятно, что BR был добавлен искусственно в процессе очистки, кристаллизации или формирования условий получения структуры.
HOH — вода.
Молекулы воды являются типичным компонентом кристаллических структур белков. Они могут участвовать в стабилизации локальных контактов, формировании водородных связей и иногда — в каталитическом механизме, однако в рамках данной записи HOH в первую очередь отражает присутствие растворителя, а не отдельный специфический лиганд.
Следовательно, среди малых молекул наиболее функционально значимой является GLC, тогда как BR и HOH в большей степени отражают экспериментальные условия получения структуры.