| Остовые водородные связи белка AHBA synthase | |
| Главная |
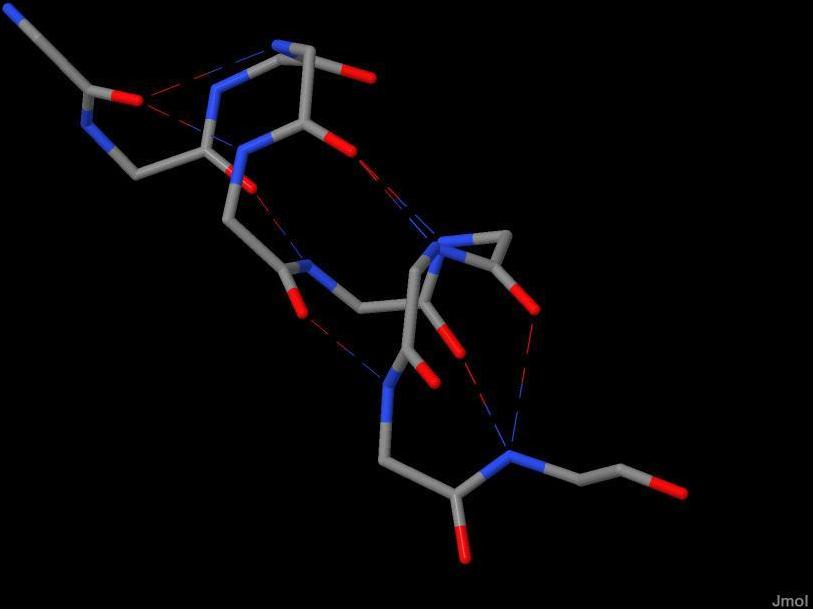
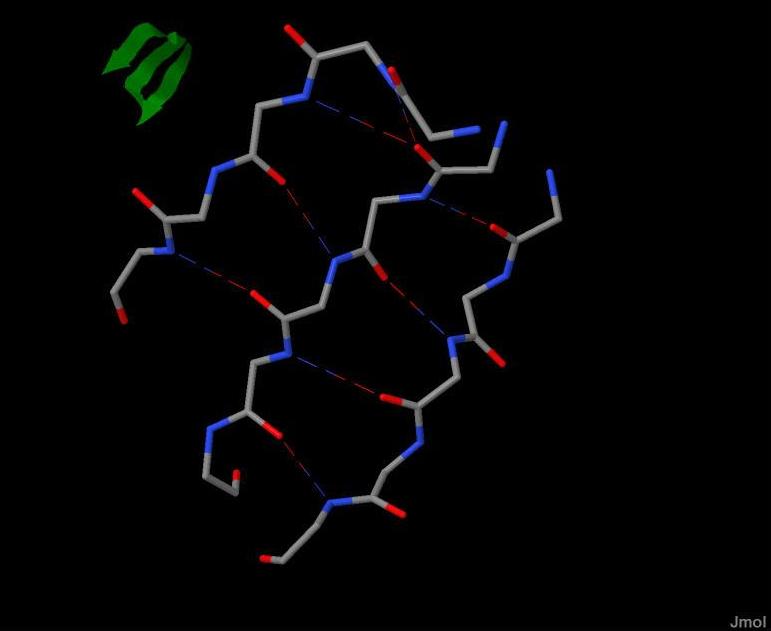
Водородные связи в α-спирали Рассмотрим водородную связь между двумя атомами в составе α-спирали (рис.1). В данном случае доноры водорода - атомы азота, а акцептопры - атомы кислорода. Разница между номерами остатков, участвующих в образовании одной водородной связи равна трем или четырём. Водородные связи в β-листе Рассмотрим водородные связи в β-листе (рис.2). Аминокислотные цепочки ориентированы друг относительно друга параллельно. При этом достигается меньшая прочность связей, чем при антипараллельной ориентации, из-за их меньшего числа на единицу длины. |
| Обо мне | |
| Ссылки | |
|
|
|
© Denis Moshensky, 2013
Дата последнего изменения: 26.05.2014
Задавайте вопросы по электронной почте