Анализ пространственной структуры белка (PDB: 3LUY)
Исследование кристаллографической структуры белка — вероятной хоризматмутазы из Bifidobacterium adolescentis с разбором общего вида структуры, числа цепей, биологической единицы, вторичной структуры и окружения лиганда PPY.
Общий вид структуры
Для анализа была использована кристаллографическая структура белка — вероятной хоризматмутазы из Bifidobacterium adolescentis, депонированная в базе Protein Data Bank под идентификатором 3LUY.
Для визуализации структуры использовалась программа PyMOL. Общий вид структуры белка был показан в представлении cartoon, которое удобно для отображения хода полипептидной цепи и элементов вторичной структуры.
Скрипт для создания изображений вы можете скачать тут:
render_3luy

ㅤㅤㅤРисунок 1.Общий вид структуры 3LUY (cartoon-представление)
Количество цепей
В асимметрической единице структуры присутствует одна белковая цепь (цепь A). Для наглядности цепь показана в едином цвете, но биологическая единица требует дополнительной сборки (см. ниже).
| Параметр | Значение |
|---|---|
| PDB ID | 3LUY |
| Белок | Вероятная хоризматмутаза |
| Число цепей в асимметрической единице | 1 |
| Обозначение цепи | A |
Биологическая единица
Согласно описанию биологической сборки (раздел REMARK 350 PDB-файла), биологическая единица белка является димером, то есть состоит из двух белковых цепей.
Таким образом:
- асимметрическая единица содержит 1 цепь;
- биологическая единица содержит 2 цепи.
Следовательно, биологическая единица отличается от асимметрической единицы: для формирования функционального димера необходимо применить операции симметрии, указанные в PDB-файле.
Для иллюстрации биологической единицы был построен димер с использованием преобразований BIOMT, после чего показаны две цепи, окрашенные в разные цвета.
ㅤㅤㅤРисунок 2. Биологическая единица белка 3LUY — димер (синий — цепь A, пурпурный — цепь B)
Вторичная структура
Для анализа вторичной структуры белок был окрашен по типу вторичной структуры (опция color by ss в PyMOL).
В результате видно, что в структуре белка присутствуют:
- α-спирали (синий);
- β-тяжи (красный);
- петли и неупорядоченные участки (жёлтые).
При визуальном анализе структуры видно, что α-спирали представлены значительно более широко, чем β-тяжи. Таким образом, спиральные элементы вторичной структуры преобладают в данной структуре белка.
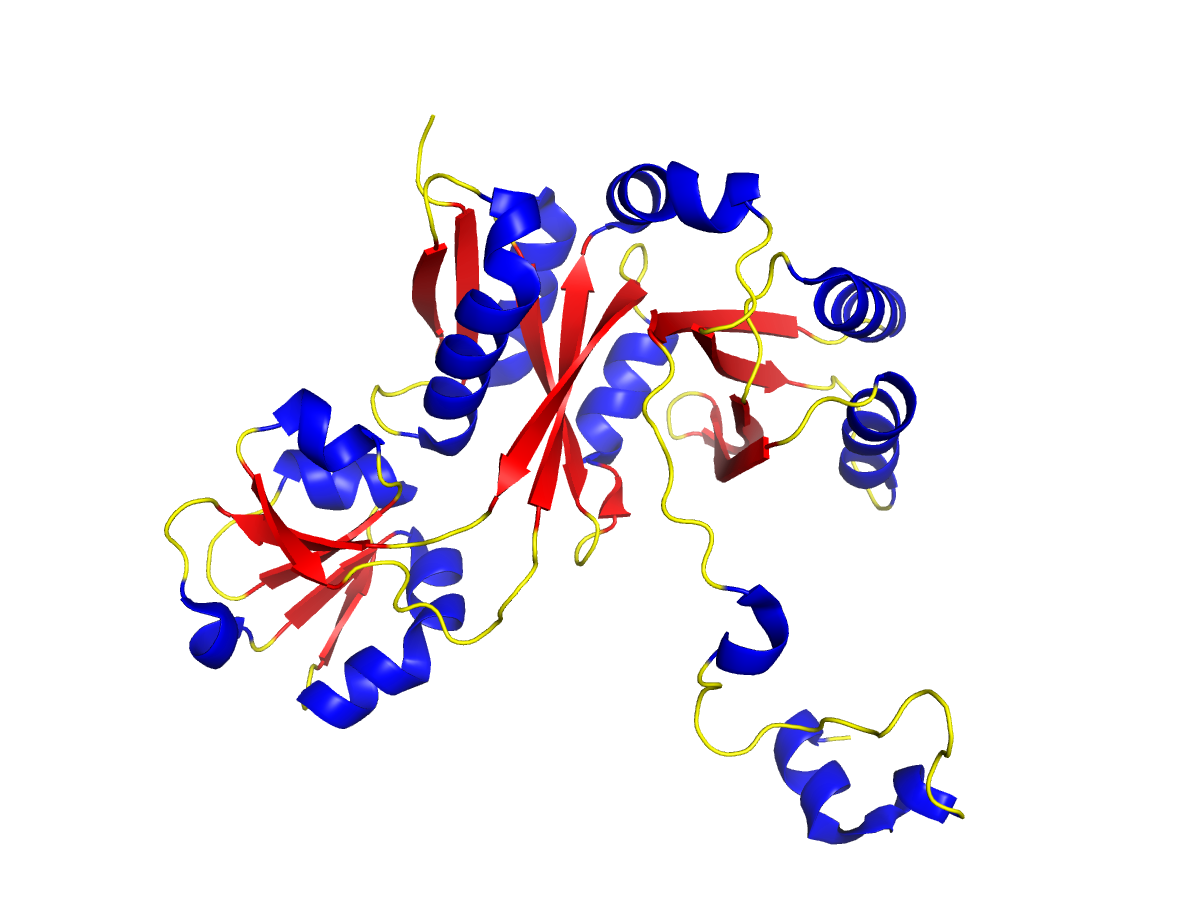
ㅤㅤㅤРисунок 3. Раскраска белка по типу вторичной структуры: синий — α-спирали, красный — β-тяжи, жёлтый — петли
Малые молекулы в структуре
В записи PDB 3LUY присутствуют несколько типов малых молекул (не считая воды):
- PPY — 3-фенилпировиноградная кислота (лиганд);
- MSE — селенометионин (модифицированный аминокислотный остаток, введённый для фазирования).
Для анализа лигандного окружения была выбрана молекула PPY, так как она является продуктом метаболического пути и, предположительно, участвует в регуляции активности фермента.
Белковое окружение лиганда
Для исследования взаимодействий лиганда с белком были выделены аминокислотные остатки белка, находящиеся на расстоянии до 5 Å от молекулы PPY.
К таким остаткам относятся (номер аминокислоты по последовательности PDB-файла):
| Остаток | Позиция |
|---|---|
| GLU | 196 |
| LEU | 197 |
| GLY | 215 |
| GLY | 217 |
| VAL | 218 |
| LEU | 219 |
| ASN | 232 |
| MSE | 233 |
| THR | 234 |
| SER | 235 |
| TYR | 248 |
| PHE | 250 |
| VAL | 218 |
| LEU | 219 |
| ASN | 232 |
| MSE | 233 |
| THR | 234 |
| SER | 235 |
| TYR | 248 |
| PHE | 250 |
| PHE | 250 |
Эти остатки формируют окружение активного центра, в котором расположен лиганд PPY.
Для наглядности лиганд был показан в представлении sticks, а окружающие аминокислотные остатки также отображены в виде sticks и подписаны.

ㅤㅤㅤРисунок 4. Лиганд PPY (жёлтый) и аминокислотные остатки в радиусе 5 Å (зелёные) с подписями
📌 Примечание: В структуре также присутствуют остатки селенометионина (MSE), которые были введены для фазирования методом SAD и не влияют на функциональные свойства белка.
Вывод
В ходе работы была исследована структура вероятной хоризматмутазы (PDB ID: 3LUY). Было показано, что асимметрическая единица содержит одну белковую цепь, однако биологическая единица является димером.
Анализ вторичной структуры показал преобладание α-спиралей. Также были выявлены малые молекулы, присутствующие в структуре, и проанализировано белковое окружение лиганда PPY, который, вероятно, участвует в регуляции фермента по принципу обратной связи.