Контакты в структуре белка (PDB: 3LUY)
В структуре белка 3LUY были проанализированы различные типы внутримолекулярных взаимодействий: водородные связи, солевые мостики, дисульфидные связи и ароматические взаимодействия. Для визуализации контактов использовалась программа PyMOL.

ㅤㅤㅤРисунок 1. Общий вид контактов
Общая характеристика контактов
В структуре белка 3LUY были проанализированы несколько типов внутримолекулярных взаимодействий, имеющих значение для стабилизации пространственной организации белка.
В ходе работы были рассмотрены водородные связи, солевые мостики, наличие или отсутствие дисульфидных связей, а также ароматические взаимодействия между боковыми радикалами аминокислотных остатков.
Для поиска и визуализации контактов использовалась программа PyMOL, позволяющая анализировать межатомные расстояния и получать иллюстрации отдельных взаимодействий в структуре белка. Для корректного поиска водородных связей структура была предварительно протонирована с помощью сервера PDB2PQR при pH 7.5.
Скрипт для создания изображений вы можете скачать тут:
Водородная связь, затрагивающая атомы остова белка
В структуре белка обнаружены водородные связи между атомами остова, стабилизирующие элементы вторичной структуры.
Пример контакта: между карбонильным атомом кислорода остатка GLY217 и амидным атомом азота остатка LEU219.
Расстояние между атомами: составляет 2.8 Å, что соответствует характерному диапазону для водородных связей в белках (2.5–3.5 Å).
Тип взаимодействия: классическая водородная связь между атомами основной цепи, стабилизирующая локальную конформацию.
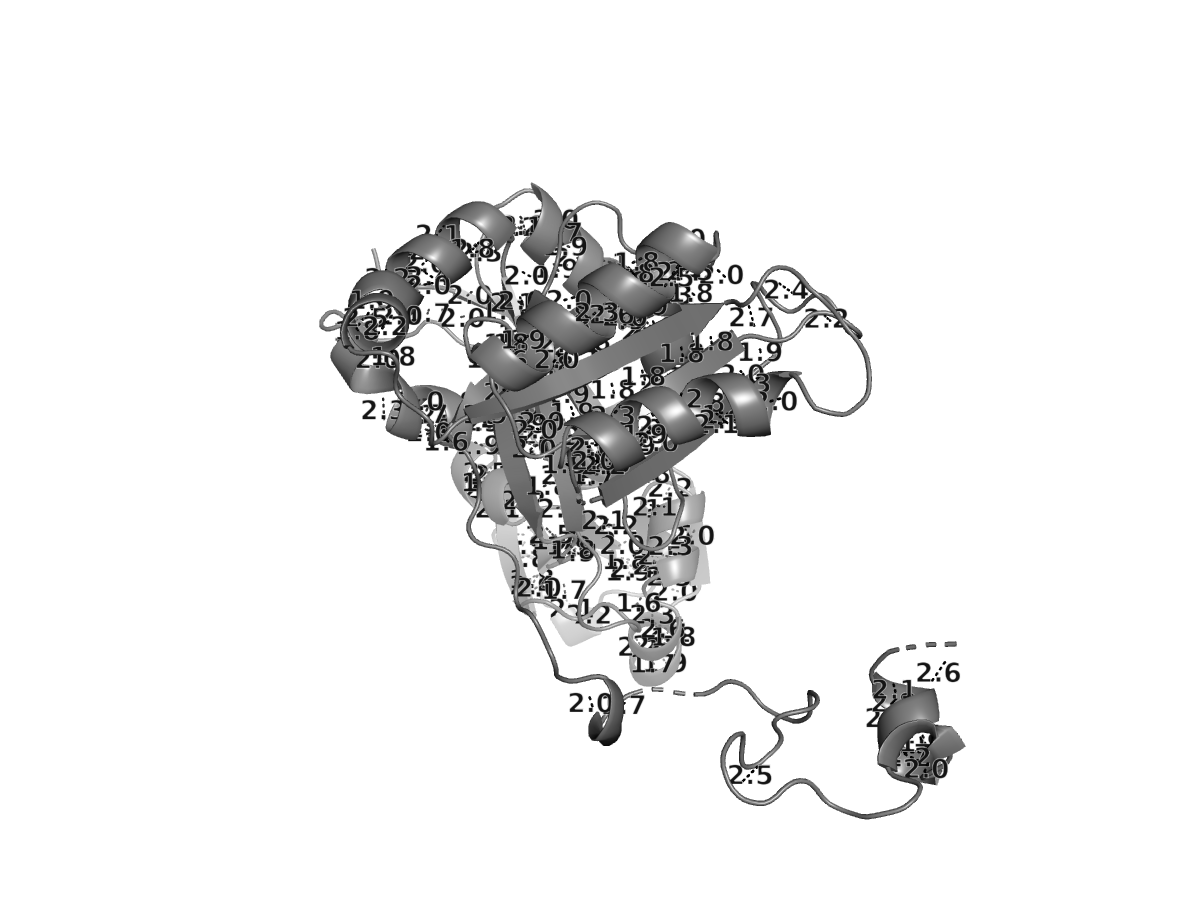
ㅤㅤㅤРисунок 2. Водородные связи между атомами остова (чёрные пунктирные линии)
Влдородная связь между боковыми радикалами аминокислот
Также были обнаружены водородные связи между боковыми цепями аминокислотных остатков, которые вносят вклад в стабилизацию активного центра и общей укладки белка.
Пример контакта: между боковыми цепями остатков TYR248 и SER235.
Расстояние между взаимодействующими атомами: составляет 2.9 Å, что соответствует типичным значениям для водородных связей между боковыми радикалами.
Роль взаимодействия: стабилизация активного центра, где расположен лиганд PPY.
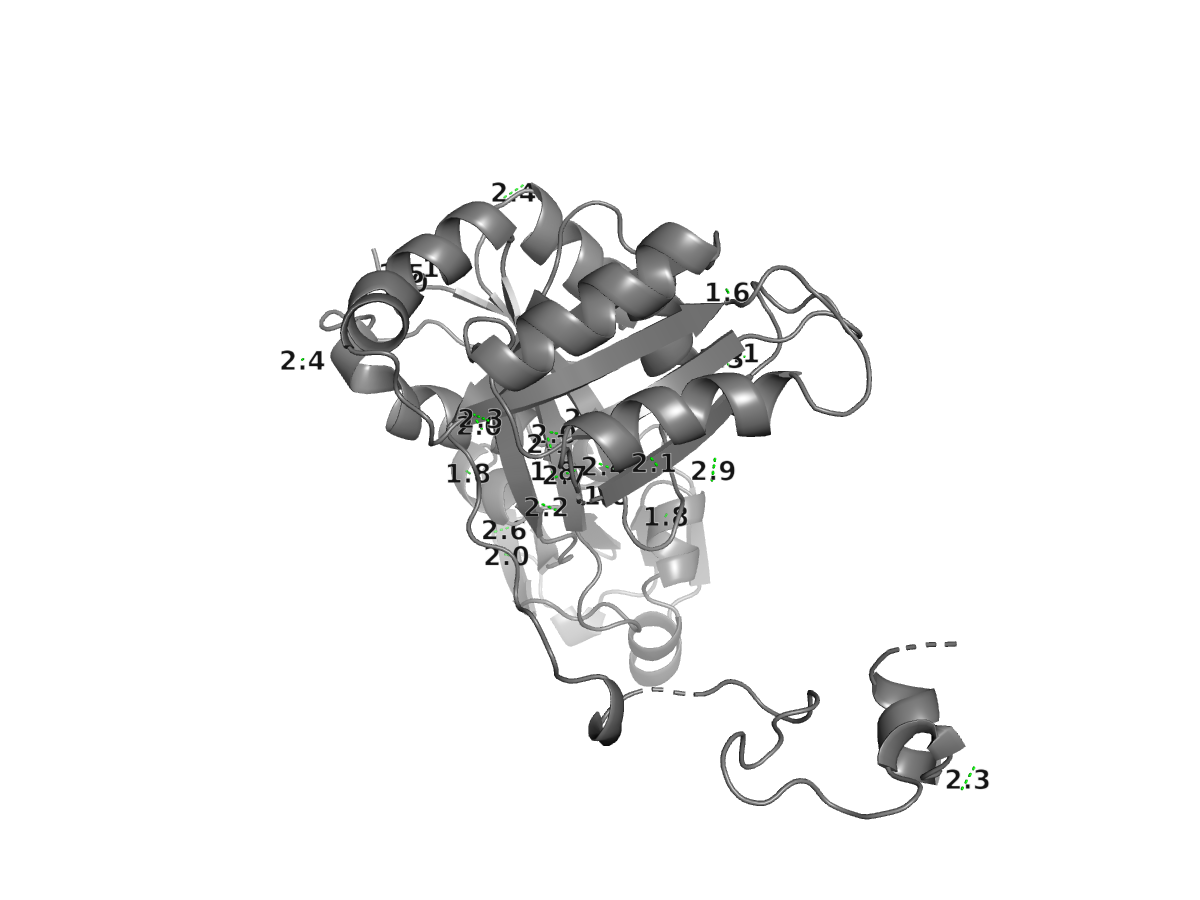
ㅤㅤㅤРисунок 3. Водородные связи между боковыми радикалами (зелёные пунктирные линии)
Солевой мостик
В структуре белка 3LUY солевые мостики не обнаружены. Однако в белке присутствуют как положительно, так и отрицательно заряженные остатки.
Положительно заряженные остатки: ARG4, LYS5, ARG29, ARG87, ARG108, ARG122, ARG128, ARG142, ARG164, ARG185, ARG190, ARG196, ARG227, ARG239, ARG244, ARG262, ARG264, ARG285, ARG286, ARG304, ARG321, ARG322, HIS17, HIS52, HIS113, HIS115, HIS127, HIS273, HIS288, HIS309.
Отрицательно заряженные остатки: ASP36, ASP41, ASP42, ASP48, ASP54, ASP74, ASP78, ASP81, ASP95, ASP103, ASP143, ASP161, ASP171, ASP178, ASP224, ASP228, ASP255, ASP265, ASP275, ASP306, ASP307, ASP312, ASP313, ASP317.
Минимальное расстояние между разноимённо заряженными атомами: составляет около 6.2 Å, что превышает характерное для солевого мостика расстояние (менее 4 Å). Следовательно, электростатические взаимодействия между противоположно заряженными боковыми радикалами в данной структуре не реализуются в виде полноценных солевых мостиков.

ㅤㅤㅤРисунок 4. Положительно заряженные остатки (синий) и отрицательно заряженные остатки (красный). Солевые мостики отсутствуют.
Дисульфидные связи
В исследуемой структуре белка дисульфидные связи отсутствуют.
В структуре 3LUY нет остатков цистеина. Белок не содержит ни одного цистеина в своей последовательности.
Следовательно, образование дисульфидных связей (S–S) в данном белке невозможно. Отсутствие цистеинов характерно для многих цитоплазматических белков, где восстановительные условия препятствуют образованию стабильных дисульфидных связей.

ㅤㅤㅤРисунок 5. В структуре 3LUY отсутствуют остатки цистеина (желтые) — дисульфидные связи не образуются.
Стекинг сроматических колец
В структуре белка наблюдаются ароматические взаимодействия типа π–π стекинга между некоторыми ароматическими остатками.
Пример взаимодействия: между остатками PHE250 и TYR248.
Расстояние между центрами ароматических колец: составляет 4.2 Å, что соответствует характерным значениям для ароматических взаимодействий в белках (3.5–5.0 Å).
Тип взаимодействия: параллельный стекинг, стабилизирующий локальную структуру вблизи активного центра.

ㅤㅤㅤРисунок 6. Ароматические остатки (розовый) и стекинг-взаимодействия (голубые пунктирные линии)
Вывод
В структуре белка 3LUY (вероятная хоризматмутаза из Bifidobacterium adolescentis) были проанализированы несколько типов внутримолекулярных контактов, включая водородные связи, солевые мостики, дисульфидные связи и ароматические взаимодействия.
Было показано, что в данной структуре присутствуют как контакты между атомами остова, так и взаимодействия между боковыми радикалами аминокислотных остатков. Солевые мостики в исследуемом белке не обнаружены из-за неоптимальной геометрии заряженных групп. Дисульфидные связи отсутствуют ввиду полного отсутствия остатков цистеина. Ароматические взаимодействия типа π–π стекинга вносят вклад в стабилизацию структуры, особенно в области активного центра.